Clear Sky Science · it
Effetti dell’affollamento molecolare sulla stabilità delle proteine in un proteoma batterico
Perché la vita affollata delle proteine conta
All’interno di ogni cellula vivente, le proteine svolgono i loro compiti in uno spazio così pieno di altre molecole che quasi metà del volume può essere occupato. Eppure la maggior parte degli esperimenti di laboratorio studia le proteine in soluzioni diluite, quasi vuote. Questo articolo pone una domanda semplice ma importante: come modifica questa realtà affollata la stabilità e il comportamento delle proteine, e cosa significa ciò per il funzionamento della vita a scala molecolare?
Uno sguardo in un mondo cellulare affollato
Per esplorare la questione, i ricercatori hanno lavorato con un batterio chiamato Cupriavidus necator, un microrganismo di interesse per tecnologie verdi come la cattura del carbonio e la produzione di bioplastiche. Hanno lacerato le cellule con delicatezza, mantenendo centinaia di diverse proteine vicine alle loro forme naturali. Poi hanno aggiunto alte concentrazioni di grandi polimeri idrofilici — comuni “agenti d’affollamento” chiamati PEG, dextrano e Ficoll — spesso usati per imitare l’interno denso delle cellule.
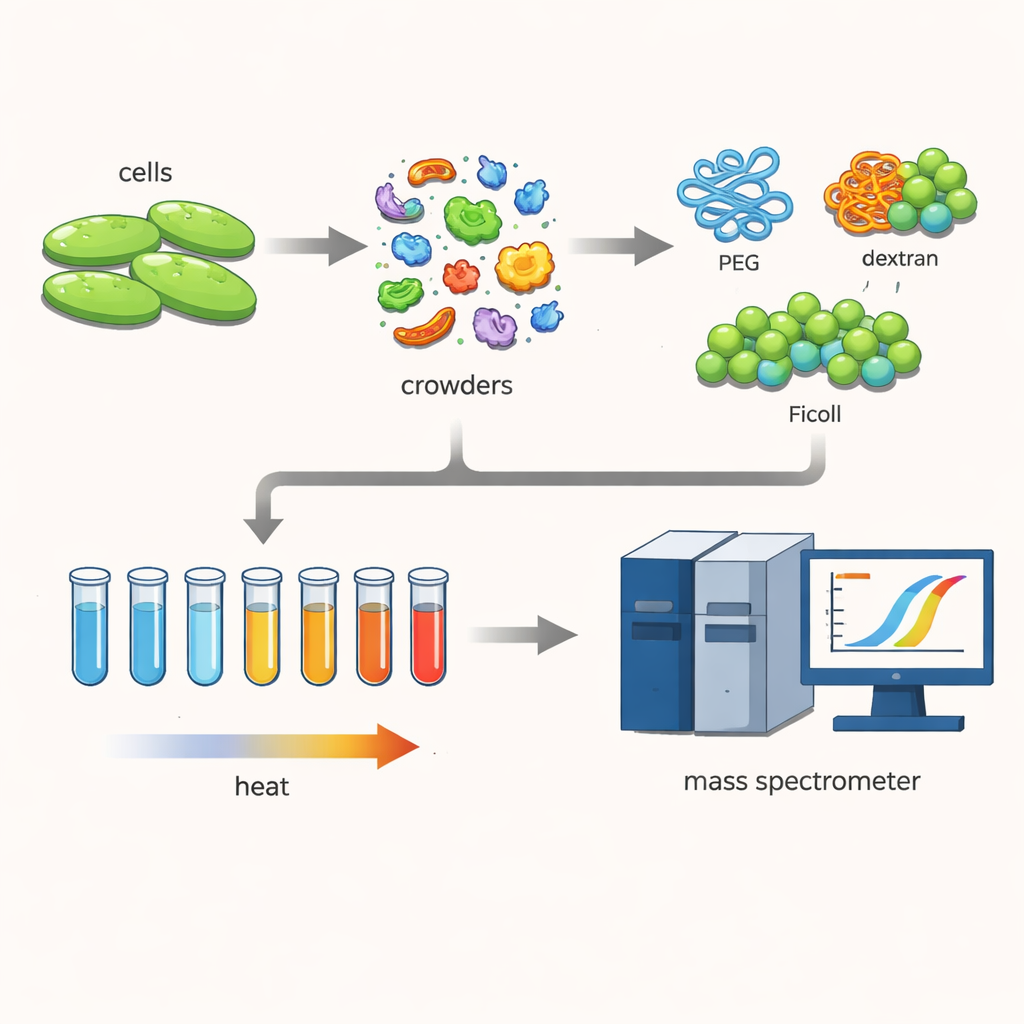
Guardare le proteine fondersi
Il gruppo ha utilizzato una tecnica nota come thermal proteome profiling. Hanno riscaldato numerosi piccoli campioni della miscela proteica a tappe da 30 a 70 °C. Con l’aumentare della temperatura, le proteine meno stabili si denaturavano e aggregavano, precipitando fuori soluzione. Marcando le proteine rimaste solubili e misurandole con uno spettrometro di massa sensibile, gli scienziati hanno potuto ricostruire curve di fusione per ciascuna proteina e determinarne la temperatura di fusione — il punto in cui metà della proteina ha lasciato lo stato solubile e funzionale. Confrontando queste temperature con e senza agenti d’affollamento, hanno rivelato come l’ambiente affollato sposti la stabilità delle proteine.
Un quadro misto: alcune proteine più solide, altre più fragili
In media, l’aggiunta di uno qualsiasi dei sei polimeri riduceva le temperature di fusione nell’intero proteoma batterico, implicando un lieve effetto destabilizzante globale. Ma questa tendenza generale nascondeva una storia molto più sfumata. Per dozzine di singole proteine, gli agenti d’affollamento aumentavano o diminuivano chiaramente la stabilità, talvolta di diversi gradi. La maggior parte delle proteine era influenzata da uno solo dei sei reagenti, ma alcune rispondevano a più agenti, e quasi tutte queste mostravano una stabilizzazione o una destabilizzazione coerente, suggerendo caratteristiche comuni sottostanti nel modo in cui interagiscono con gli agenti d’affollamento.
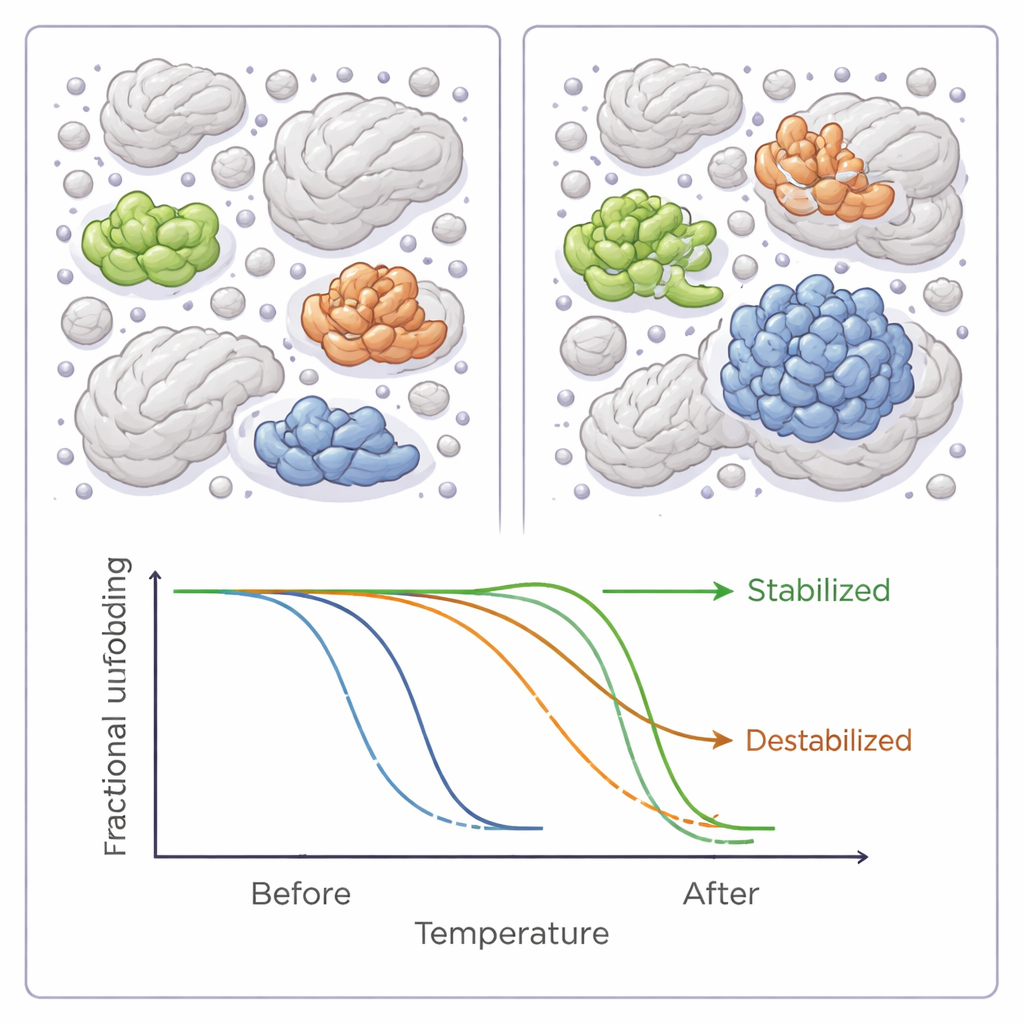
Cosa fa vincere o perdere una proteina in una folla
Quando gli autori hanno esaminato più da vicino le proprietà di queste proteine sensibili, sono emersi dei modelli. Le proteine che diventavano più stabili in condizioni affollate tendevano a essere più idrofobiche — cioè presentavano superfici più che respingono l’acqua — ed erano più spesso enzimi classici con siti attivi ben definiti. Erano anche più propense a essere coinvolte in interazioni proteina‑proteina o a portare modifiche chimiche che ne regolano la funzione. Le proteine destabilizzate, al contrario, erano in media più piccole e meno “decorate” da tali modifiche. Questi risultati rispecchiano modelli computazionali e altri esperimenti che suggeriscono che l’affollamento può avvantaggiare alcune proteine rendendone altre più vulnerabili, a seconda di dimensione, forma e delle interazioni abituali con i partner.
Oltre la semplice compressione: come agiscono veramente gli agenti d’affollamento
Le spiegazioni tradizionali per l’affollamento molecolare si concentrano sul “volume escluso”, l’idea che le grandi molecole lascino semplicemente meno spazio, spingendo le proteine a restare ripiegate. Se questa fosse tutta la storia, ci si aspetterebbe che gli agenti d’affollamento stabilizzino principalmente le proteine e che vi siano forti legami con l’ingombro o la viscosità dei polimeri. Invece, gli autori hanno osservato solo deboli connessioni con la dimensione e la “spessore” dei polimeri. I loro dati si adattano meglio a un quadro di “esclusione preferenziale”: agenti d’affollamento e proteine si evitano chimicamente, il che favorisce indirettamente certi stati ripiegati ma può anche disturbare interazioni delicate che mantengono stabili altre proteine. In breve, non è solo una compressione fisica, ma una sottile spinta e attrazione chimica che modella il comportamento proteico.
Cosa significa questo per comprendere la chimica della vita
Per i non specialisti, il messaggio chiave è che le proteine all’interno delle cellule non possono essere pienamente comprese in isolamento, immerse in un tampone trasparente. La giungla molecolare densa intorno a loro può rendere alcune proteine più robuste e altre più fragili, modificando il comportamento di intere reti di reazioni. Questo studio, misurando i cambiamenti di stabilità per centinaia di proteine contemporaneamente, mostra che gli effetti dell’affollamento sono complessi e specifici per singola proteina, e probabilmente guidati da interazioni dirette tanto quanto dal semplice imballaggio. Mentre i ricercatori progettano farmaci, enzimi industriali o microrganismi ingegnerizzati, riconoscere questa realtà affollata sarà cruciale per prevedere come le proteine si comportano realmente nei sistemi viventi.
Citazione: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Parole chiave: affollamento molecolare, stabilità delle proteine, profiling termico del proteoma, proteoma batterico, ambiente cellulare