Clear Sky Science · it
Aggregazione sopramolecolare dell’acquaporina-4 modella la migrazione collettiva e la meccanica degli astrociti
Come le cellule cerebrali si muovono insieme per riparare
Quando il cervello è danneggiato o infiammato, le sue cellule di supporto—gli astrociti—intervengono rapidamente per proteggere, riparare o isolare le aree lese. Questo studio esplora un fattore sorprendente che influenza quanto bene queste cellule si muovono in gruppo: minuscoli canali per l’acqua chiamati acquaporina-4 (AQP4). Osservando come le molecole di AQP4 si aggregano o si disperdono nelle membrane degli astrociti, i ricercatori mostrano come la “plumberia” acquatica del cervello contribuisca a coordinare il movimento collettivo cellulare e come l’infiammazione cronica possa compromettere questo processo.
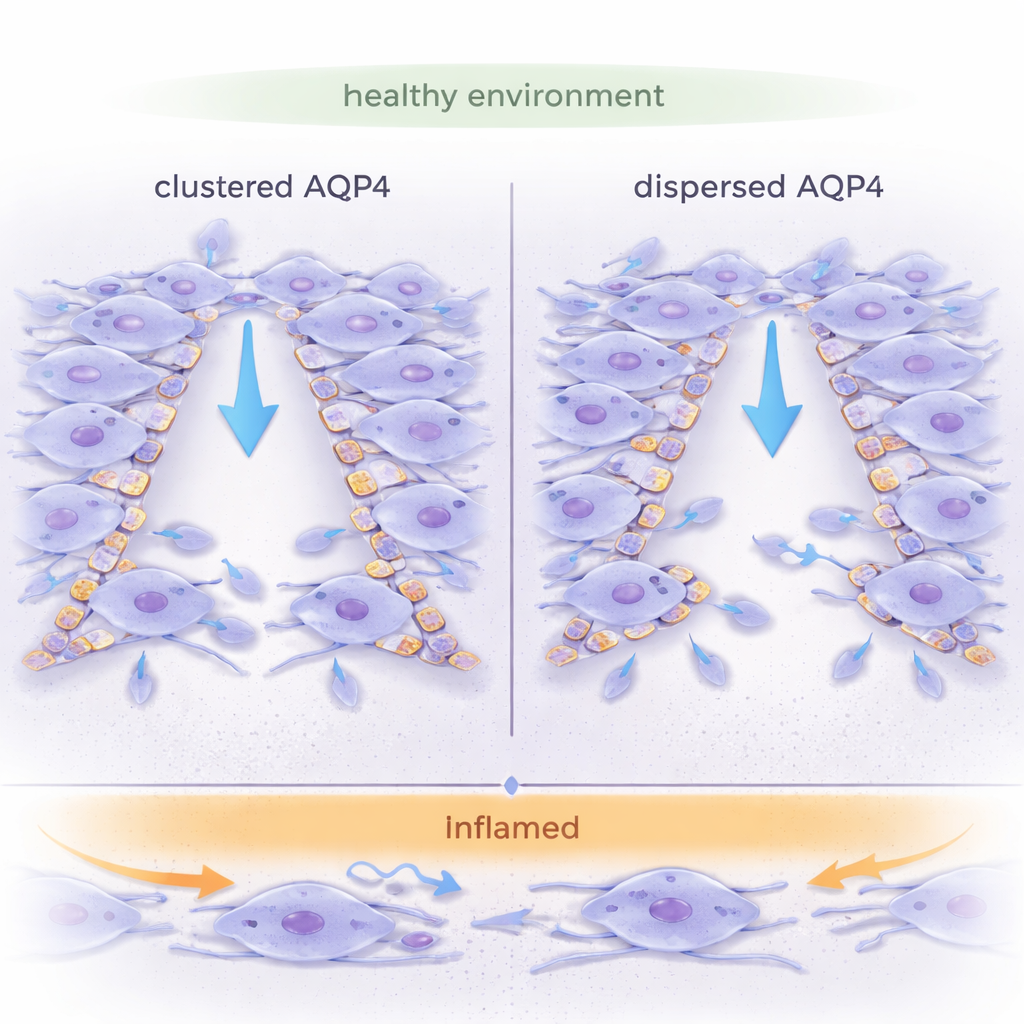
Passaggi d’acqua sulle cellule cerebrali
Gli astrociti sono cellule a forma di stella che aiutano a mantenere l’equilibrio cerebrale, guidano lo sviluppo e rispondono alle lesioni. Sono ricchi di AQP4, una proteina che forma pori che permettono all’acqua di entrare e uscire rapidamente dalla cellula. A differenza di molti altri canali per l’acqua, AQP4 può assemblarsi in grandi patch cristalline chiamate matrici ortogonali di particelle (OAP) oppure rimanere come unità più piccole e disperse (tetrameri). Si pensa che l’organizzazione di AQP4 influenzi il modo in cui le cellule cambiano forma e si muovono, ma la maggior parte dei lavori precedenti si è concentrata su cellule singole. Questo studio si è posto una domanda più realistica: come influenza l’organizzazione di AQP4 il modo in cui intere lastre di astrociti migrano insieme, come avverrebbe per chiudere una ferita nel tessuto cerebrale?
Testare il movimento cellulare in salute e in infiammazione
I ricercatori hanno coltivato due tipi di astrociti murini: cellule normali in grado di formare matrici di AQP4 e cellule geneticamente modificate (OAP-null) prive della principale variante che forma le matrici e quindi caratterizzate principalmente da tetrameri dispersi. Hanno poi creato un “graffio” in uno strato denso di cellule, mimando una ferita, e osservato quanto rapidamente e quanto uniformemente le cellule chiudevano il gap. Per simulare un cervello cronicamente lesionato, hanno anche esposto alcune colture a due molecole infiammatorie, IL-1β e TNF-α, per una settimana prima dei test. Utilizzando immagini time-lapse e un metodo di visione artificiale chiamato velocimetria delle immagini particellari, hanno quantificato non solo quanto lontano e quanto velocemente le cellule si muovevano, ma anche quanto rettilineo, coordinato o soggetto a deformazioni fosse il loro moto su tutta la lastra.
Canali dispersi, movimento più fluido
In condizioni non infiammate, gli astrociti con AQP4 dispersa (OAP-null) migravano collettivamente in modo nettamente migliore: chiudevano le ferite più velocemente e si muovevano in modo più diretto e lineare rispetto alle cellule con grandi matrici di AQP4. Il loro fronte avanzante era liscio e continuo, e le cellule vicine si muovevano in modo coeso, «a foglio». Al contrario, gli astrociti con AQP4 raggruppata (tipo selvatico) mostravano un fronte più irregolare, con molte protrusioni individuali e distorsioni interne, suggerendo che le cellule tiravano in direzioni leggermente diverse. Le misure di deformazione all’interno dello strato cellulare confermarono che le lastre OAP-null sperimentavano meno conflitti interni e un moto più uniforme e coordinato.
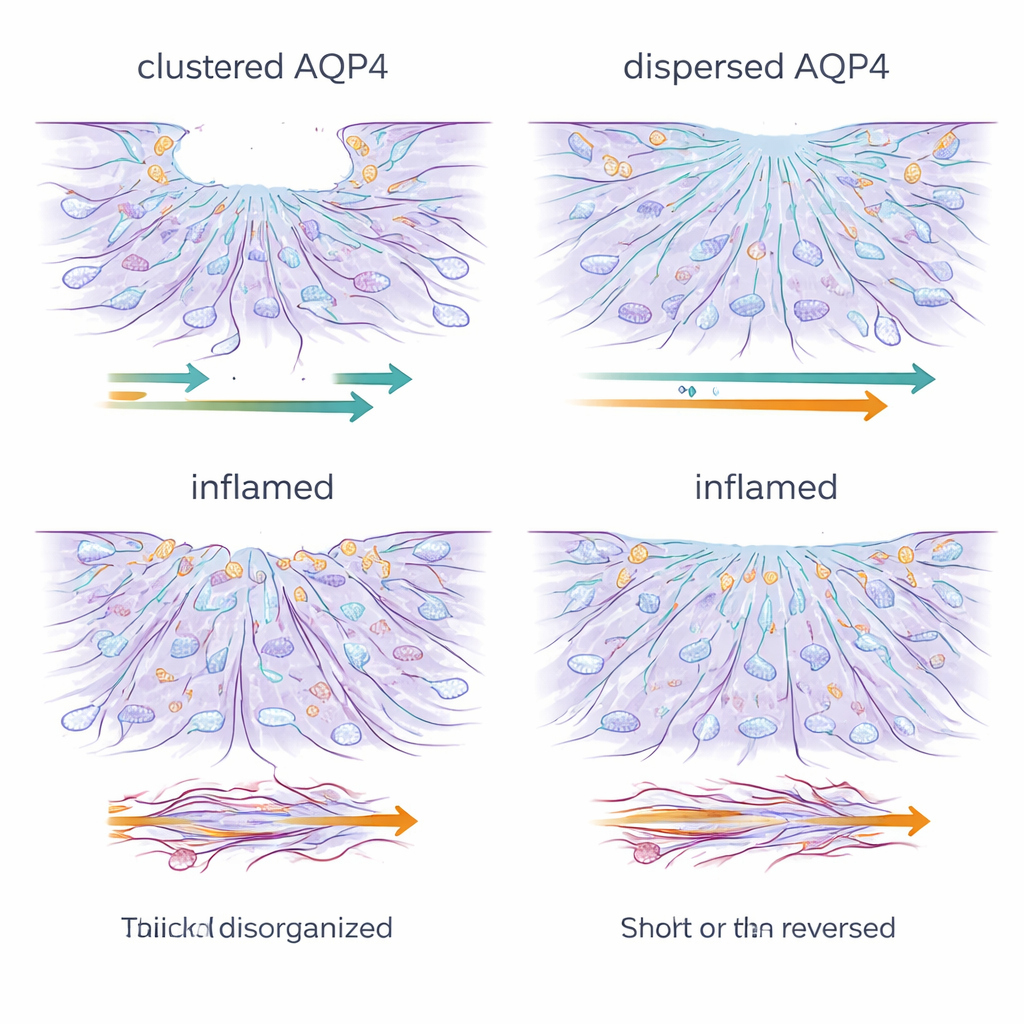
L’infiammazione rallenta e scombina la squadra di riparazione
L’esposizione cronica a segnali infiammatori ha profondamente modificato questo quadro. Indipendentemente dall’organizzazione di AQP4, gli astrociti trattati divennero scarsi nel chiudere le ferite: si muovevano a malapena e in alcuni casi retrocedevano, ampliando il gap. La microscopia mostrò che le sottili strutture dinamiche al margine cellulare necessarie al movimento in avanti—lamellipodi e filopodi—venivano perdute e sostituite da spessi e rigidi filamenti di stress di actina, la principale proteina strutturale della cellula. Allo stesso tempo, i livelli di AQP4 e di connessina-43, una proteina chiave che forma canali di comunicazione tra astrociti, calarono drasticamente. La rete di giunzioni comunicanti che normalmente aiuta gli astrociti ad agire come un’unità coordinata fu compromessa, e esperimenti di trasferimento di colorante confermarono che la comunicazione cellula–cellula a lungo raggio era fortemente indebolita.
Perché questo è importante per la salute del cervello
Questi risultati suggeriscono che non è solo la quantità di AQP4 presente in una cellula, ma anche come essa è organizzata, a facilitare lo spostamento efficiente degli astrociti come gruppo. L’AQP4 dispersa sembra ridurre la resistenza interna tra le cellule e favorire un movimento più rettilineo e coordinato, mentre grandi ammassi sono associati a uno stile di movimento più erratico e soggetto a tensioni. L’infiammazione cronica sovrascrive in gran parte questi vantaggi rimodellando lo scheletro cellulare, silenziando i canali d’acqua e di comunicazione e trasformando una squadra di riparazione organizzata in un foglio rigido e poco connesso. Per i non specialisti, il messaggio è che i canali d’acqua del cervello e i sistemi di comunicazione cellula–cellula fanno molto più che supportare passivamente i neuroni: plasmano attivamente il modo in cui le cellule di supporto si mobilitano dopo una lesione. Capire e, in futuro, modulare l’organizzazione di AQP4 e i segnali infiammatori potrebbe aprire nuove strade per migliorare la riparazione cerebrale, limitare la cicatrizzazione o persino influenzare la diffusione dei tumori cerebrali.
Citazione: Barile, B., Mennona, N.J., Mola, M.G. et al. Supramolecular aggregation of aquaporin-4 shapes astrocyte collective migration and mechanics. Sci Rep 16, 6021 (2026). https://doi.org/10.1038/s41598-026-35900-z
Parole chiave: astrociti, acquaporina-4, infiammazione cerebrale, migrazione cellulare, cicatrice gliale