Clear Sky Science · it
Rilevazione della malattia falciforme in condizioni a risorse limitate usando transfer learning e contrastive learning con XAI
Perché sono importanti esami del sangue più intelligenti
L’anemia falciforme è una malattia ematica cronica che può causare dolori intensi, infezioni e morte prematura, soprattutto in alcune zone dell’Africa e dell’India dove le risorse sanitarie sono scarse. Una diagnosi precoce può salvare vite, ma i test tradizionali richiedono personale qualificato, macchinari specializzati e tempo che molte cliniche non hanno. Questo articolo esplora come l’intelligenza artificiale (IA) possa trasformare semplici immagini al microscopio del sangue in strumenti di screening veloci e affidabili, facilitando l’individuazione dell’anemia falciforme anche in contesti a risorse limitate.
Uno sguardo più attento a una pericolosa malattia del sangue
Nell’anemia falciforme, una piccola variazione nel gene dell’emoglobina — la proteina che trasporta l’ossigeno — fa sì che i globuli rossi si pieghino in forme rigide a mezzaluna o “a falce” invece di rimanere morbidi e rotondi. Queste cellule deformate possono ostruire i piccoli vasi sanguigni, bloccando il flusso e danneggiando gli organi. 
Dai laboratori sovraccarichi agli assistenti IA
I metodi tradizionali per confermare l’anemia falciforme — come l’elettroforesi dell’emoglobina o i test genetici — sono accurati ma spesso costosi, richiedono apparecchiature e sono lenti. Al contrario, molte cliniche dispongono già di microscopi di base, e le fotocamere moderne possono acquisire immagini ad alta risoluzione degli strisci del sangue. Gli autori sfruttano questa realtà: invece di modificare il modo in cui il sangue viene raccolto, cambiano il modo in cui le immagini vengono analizzate. Alimentano immagini digitalizzate degli strisci nel sangue in modelli di IA che hanno già imparato a riconoscere schemi a partire da milioni di fotografie di uso quotidiano, quindi rifiniscono questi modelli per distinguere i globuli rossi normali da quelli falciformi. Questo riuso di conoscenza preesistente, chiamato transfer learning, è cruciale quando sono disponibili solo poche centinaia di immagini mediche per l’addestramento.
Insegnare alle macchine a distinguere forme sottili
Non tutti i metodi di addestramento dell’IA sono uguali, soprattutto quando i dati sono limitati. I ricercatori confrontano tre popolari reti di riconoscimento delle immagini — ResNet-50, DenseNet-121 ed EfficientNet-B0 — e tre modalità di addestramento. Due dei metodi trattano il problema come una semplice domanda sì/no (falciforme o no) e cercano di migliorare l’accuratezza di classificazione grezza del modello. Il terzo, chiamato triplet loss, invece insegna alla rete a disporre le immagini in uno “spazio delle forme” in cui le immagini delle cellule falciformi si raggruppano e si allontanano da quelle delle cellule normali. Questo addestramento incentrato sul contrasto trasforma il modello in uno specialista nel riconoscere piccole differenze basate sulla forma, che è esattamente ciò che conta nella microscopia dell’anemia falciforme.
Rendere visibile il processo decisionale
I medici e gli operatori di laboratorio devono poter avere fiducia in qualsiasi sistema automatizzato che influenzi la cura del paziente. Per aprire la “scatola nera” dell’IA, gli autori utilizzano un metodo di intelligenza artificiale spiegabile chiamato Grad-CAM, che sovrappone una mappa di calore all’immagine originale del microscopio per mostrare quali regioni hanno influenzato maggiormente la decisione. 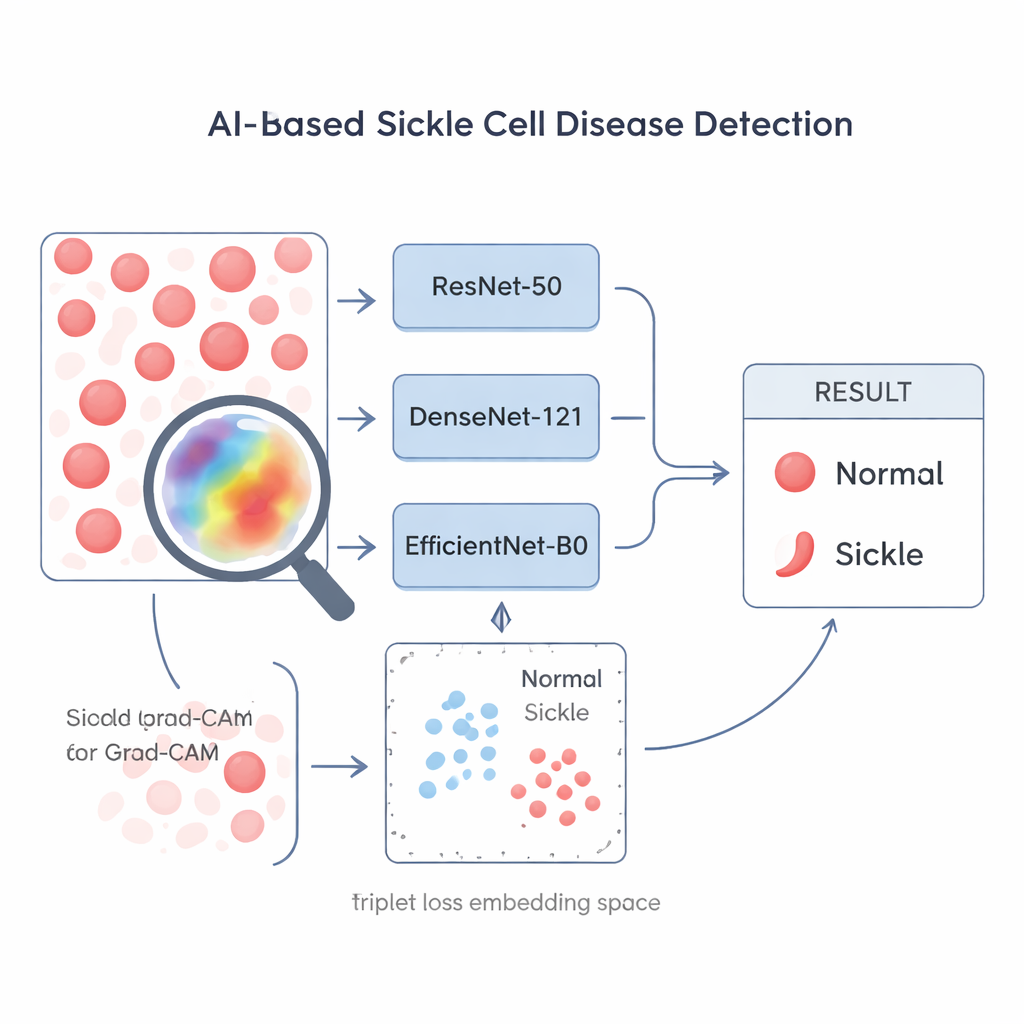
Dalla ricerca alle cliniche sul campo
Lo studio conclude che il riuso intelligente di reti di riconoscimento delle immagini esistenti, combinato con l’addestramento a triplet loss e spiegazioni visive, può fornire una rilevazione dell’anemia falciforme accurata e trasparente a partire da un numero relativamente ridotto di immagini. In termini semplici, un microscopio standard più una fotocamera e un laptop potrebbero aiutare le cliniche di prima linea a segnalare rapidamente i pazienti che probabilmente hanno l’anemia falciforme, anche senza test di laboratorio avanzati. Pur richiedendo set di dati più grandi e diversificati prima di una diffusione su larga scala, questo lavoro mostra una strada chiara verso uno screening assistito da IA a basso costo che potrebbe fare la differenza in regioni dove l’anemia falciforme è comune ma le risorse diagnostiche sono limitate.
Citazione: Patel, J., Muralikrishna, H., Chadaga, K. et al. Sickle cell disease detection in low-resource conditions using transfer-learning and contrastive-learning coupled with XAI. Sci Rep 16, 6104 (2026). https://doi.org/10.1038/s41598-026-35831-9
Parole chiave: anemia falciforme, imaging medico, deep learning, diagnostica a risorse limitate, intelligenza artificiale spiegabile