Clear Sky Science · it
Comunià nelle variazioni di espressione genica e metilazione attraverso due modelli di ratto di epilessia acquisita
Perché cambiare i geni conta per le crisi
L’epilessia colpisce milioni di persone e, per circa un paziente su tre, i farmaci attuali non riescono a controllare completamente le crisi. La maggior parte dei farmaci attenua semplicemente le tempeste elettriche nel cervello ma non impedisce lo sviluppo dell’epilessia. Questo studio esplora se marchi chimici duraturi sul DNA e il modo in cui i geni vengono attivati o disattivati possano spiegare come un cervello sano diventi epilettico — e se tali cambiamenti siano condivisi tra diverse forme della malattia.
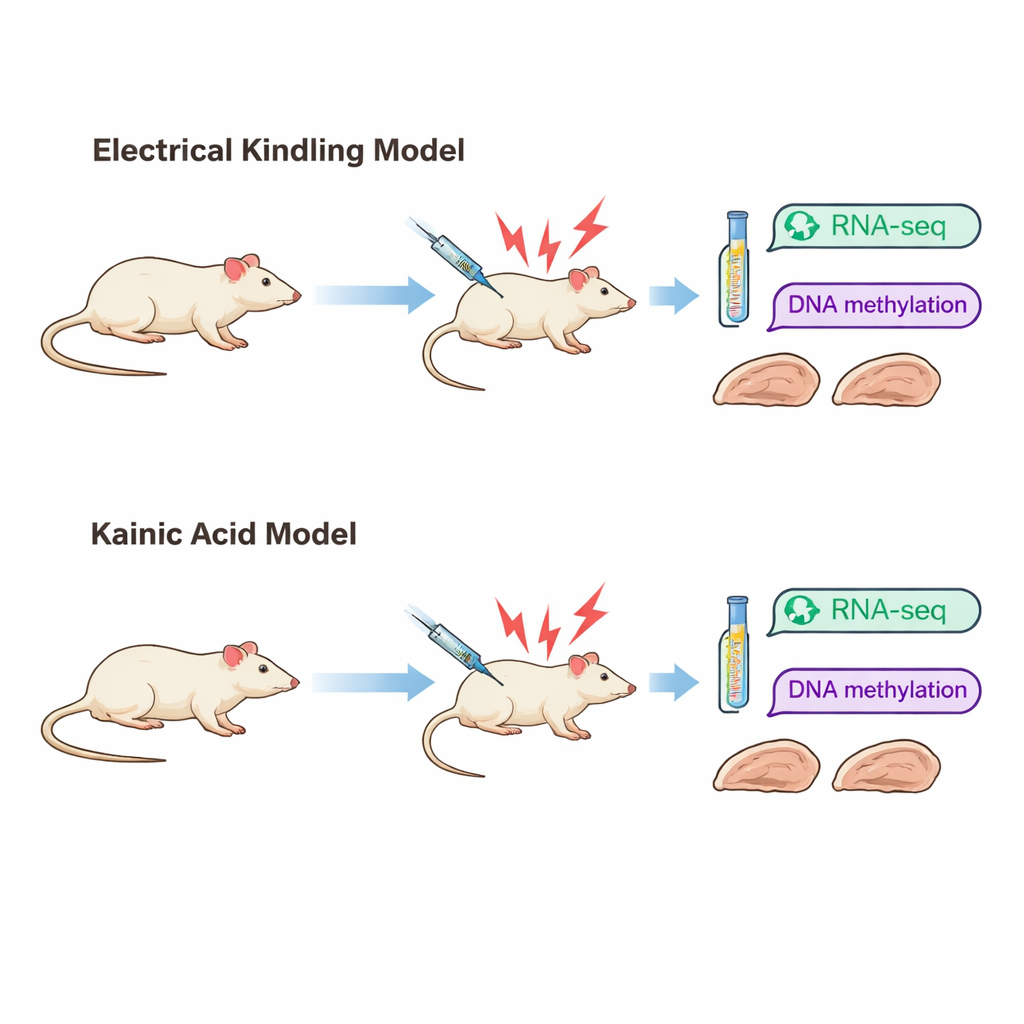
Due strade diverse verso la stessa malattia
I ricercatori si sono concentrati sull’epilessia del lobo temporale, una forma comune della condizione che spesso resiste al trattamento. Hanno utilizzato due modelli di ratto ben consolidati che imitano modi diversi in cui l’epilessia può insorgere. Nel modello di “kindling”, vengono somministrati nel tempo brevi impulsi elettrici a una parte dell’ippocampo finché le crisi non diventano facilmente evocabili. Nel modello con “acido kainico”, una sostanza chimica provoca un intenso episodio di crisi, dopo il quale compaiono più tardi crisi spontanee. Sebbene entrambi i modelli producano alla fine comportamenti esteriori simili — crisi convulsive gravi — il danno cerebrale appare molto diverso. I ratti kindled mostrano una struttura tessutale in gran parte preservata, mentre i ratti trattati con acido kainico presentano una perdita cellulare pronunciata e cicatrici in regioni chiave dell’ippocampo.
Leggere l’attività genetica del cervello
Per vedere come questi diversi percorsi verso l’epilessia modificano il cervello a livello molecolare, il gruppo ha esaminato l’ippocampo dopo che i ratti di ciascun modello avevano sperimentato tre crisi severe. Hanno misurato quali geni erano più o meno attivi usando il sequenziamento dell’RNA e hanno mappato i marchi chimici chiamati gruppi metilici sul DNA impiegando un metodo noto come sequenziamento bisolfito a rappresentazione ridotta. I cambiamenti nell’attività genica riflettono come le cellule rispondono e si adattano, mentre i marchi di metilazione sono spesso considerati una “memoria” a più lungo termine che può influenzare se i geni vengono attivati o repressionati.
I cambiamenti nell’attività genica superano i marchi del DNA
I due modelli hanno prodotto schemi di attività genica sorprendentemente diversi. Il modello di kindling ha mostrato cambiamenti in più di dieci volte il numero di geni rispetto al modello con acido kainico. Tuttavia, quando i ricercatori hanno sovrapposto le due liste, hanno comunque trovato oltre cento geni che si modificavano in entrambi i modelli, e la maggior parte si spostava nella stessa direzione. Un esempio è Mmp9, un gene collegato a come le cellule cerebrali rimodellano le loro connessioni e al danno associato alle crisi; era fortemente aumentato in entrambi i modelli. Questi cambiamenti condivisi suggeriscono che esistono risposte genetiche fondamentali all’epilettogenesi, anche quando il trigger iniziale e il danno cerebrale visibile differiscono.
I marchi del DNA raccontano una storia diversa
Quando il team ha analizzato la metilazione del DNA, il quadro è cambiato. Entrambi i modelli hanno mostrato molti geni con metilazione alterata, e c’è stata una sovrapposizione considerevole tra essi. Tuttavia, solo un sottoinsieme modesto di geni mostrava sia metilazione alterata sia attività alterata all’interno dello stesso modello, e ancora meno si comportava in questo modo in entrambi i modelli. In alcuni di questi geni condivisi, come Nedd9 e Ptpre, l’espressione aumentava in entrambi i modelli, ma la direzione del cambiamento della metilazione del DNA in singoli siti poteva essere opposta tra i modelli. Nel complesso, non è emersa una regola semplice del tipo “più metilazione significa meno attività genica” o viceversa. Ciò suggerisce che, in questi modelli di epilessia, la maggior parte degli spostamenti nell’attività genica non è direttamente guidata da ampi cambiamenti nella metilazione del DNA.
Cosa significa per i trattamenti futuri
Per chi spera in terapie migliori per l’epilessia, questi risultati offrono sia cautela che indicazioni. Il lavoro mostra che i programmi genetici attivati durante lo sviluppo dell’epilessia possono essere piuttosto specifici del modello, e che la metilazione del DNA è solo una parte di un quadro regolatorio più ampio e complesso. I bersagli genici promettenti identificati in un singolo modello animale potrebbero non essere generalizzabili, quindi dovrebbero essere testati in più modelli prima di avanzare verso trattamenti umani. Allo stesso tempo, il piccolo insieme di geni che cambiano sia in espressione sia in metilazione attraverso i modelli può rappresentare punti di partenza particolarmente robusti per sviluppare terapie modificanti la malattia che mirino non solo a sedare le crisi, ma a prevenire l’instaurarsi dell’epilessia.
Citazione: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Parole chiave: epileptogenesi, metilazione del DNA, espressione genica, epilessia del lobo temporale, modelli di ratto