Clear Sky Science · it
La perdita muscolare associata alla sepsi è attenuata dall’inibizione farmacologica della via di segnalazione STAT3 nei topi
Perché le infezioni gravi possono rubare la tua forza
Sopravvivere a un’infezione potenzialmente letale come la sepsi è solo metà della battaglia. Molti pazienti lasciano la terapia intensiva così deboli che camminare, salire le scale o anche sollevare le braccia diventa faticoso. Questo studio pone una domanda semplice ma urgente: possiamo impedire al corpo di smantellare i propri muscoli durante la sepsi e, in tal caso, come? Usando topi, cellule muscolari in coltura e osservazioni su persone in terapia intensiva, i ricercatori tracciano una via di segnalazione chiave che guida la perdita muscolare—e mostrano che un farmaco mirato può in parte bloccare il danno.
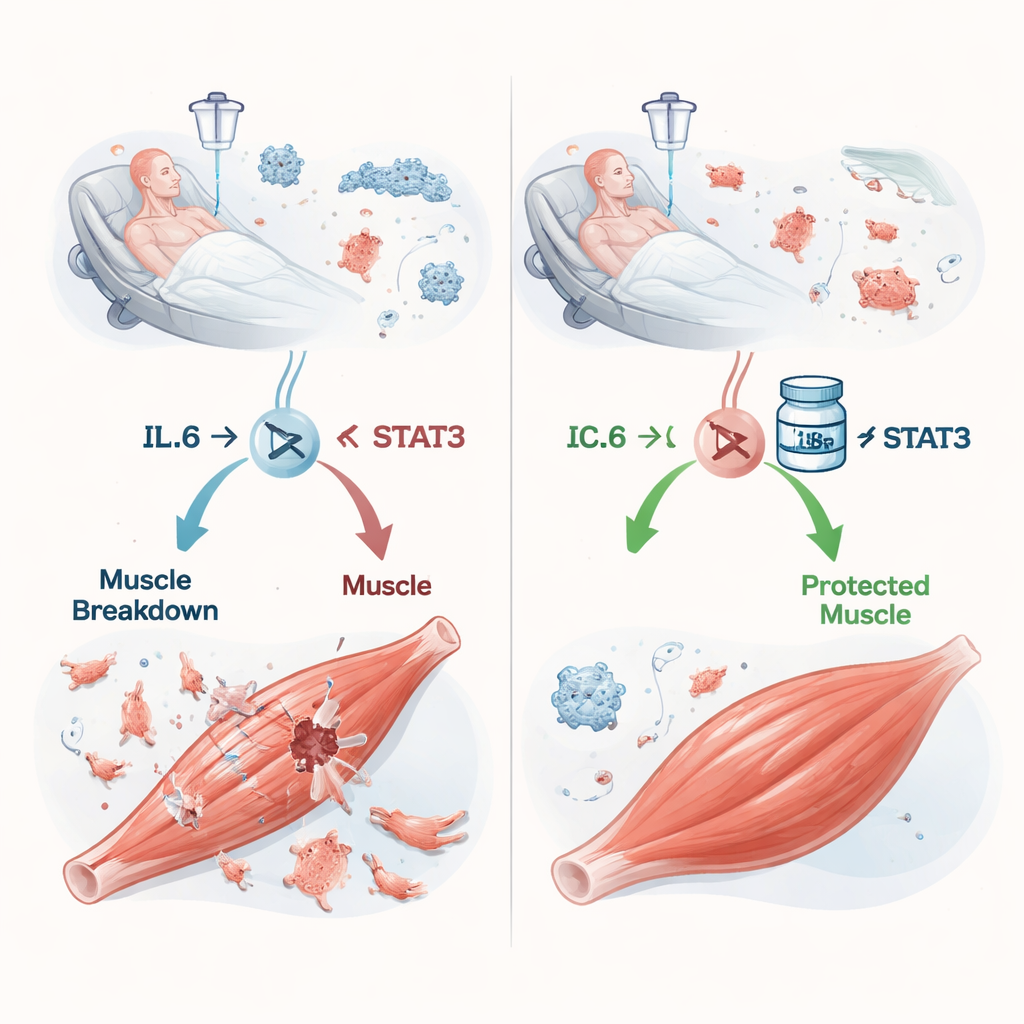
Una reazione a catena dall’infezione alla perdita muscolare
La sepsi si verifica quando la risposta del corpo all’infezione sfugge al controllo, inondando il sangue di molecole infiammatorie. Una delle più importanti è l’interleuchina‑6 (IL‑6). Lavori precedenti suggerivano che l’IL‑6 possa indurre i muscoli a degradare le proprie proteine, ma i dettagli erano poco chiari. Gli autori si sono concentrati su STAT3, una proteina intracellulare che trasmette il messaggio dell’IL‑6 al nucleo, dove i geni vengono attivati o disattivati. Nei topi ai quali è stato somministrato un slurry cecale—essenzialmente un’infezione mista controllata—i livelli di IL‑6 nel sangue e nei muscoli delle zampe aumentavano rapidamente con il peggiorare della sepsi. Contemporaneamente STAT3 si attivava nei muscoli e gli animali perdevan peso, massa muscolare e forza di presa in modo dipendente dalla gravità, molto simile a quanto osservato nei pazienti critici.
Come la sepsi riprogramma le cellule muscolari
Per capire cosa la sepsi stesse facendo all’interno delle fibre muscolari, il gruppo ha analizzato l’attività genica nel tibiale anteriore, un importante muscolo della gamba. Migliaia di geni hanno modificato la loro espressione nei topi settici rispetto ai controlli sani. Sono state attivate vie coinvolte nell’infiammazione, nello stress cellulare e, in particolare, nella segnalazione IL‑6/STAT3. Si sono intensificati due principali sistemi di smaltimento proteico: il sistema ubiquitina‑proteasoma, che marca specifiche proteine muscolari per la distruzione, e l’autofagia, un processo di riciclo più generale. Gli enzimi chiave della “distruzione muscolare”, MuRF1 e atrogin‑1, sono aumentati nettamente, mentre le vie che promuovono la crescita e i segnali classici di morte cellulare sono rimasti in gran parte invariati. In esperimenti paralleli, cellule muscolari murine in coltura esposte al lipopolisaccaride (LPS), un componente delle pareti batteriche Gram‑negative, hanno mostrato lo stesso schema: attivazione di IL‑6 e STAT3, aumento di MuRF1 e atrogin‑1, incremento dell’autofagia e assottigliamento visibile delle fibre muscolari.
Bloccare un interruttore chiave per proteggere il muscolo
L’esperimento centrale ha testato se spegnere STAT3 potesse risparmiare i muscoli. Topi con sepsi hanno ricevuto un piccolo inibitore molecolare di STAT3 chiamato C188‑9, a partire da un’ora dopo l’infezione e poi quotidianamente. Il farmaco non ha attenuato tempestivamente la «tempesta di citochine»: i livelli ematici di IL‑6 e di un altro fattore infiammatorio, TNF‑α, sono rimasti elevati, e peso corporeo e appetito non si sono ripresi rapidamente. Tuttavia C188‑9 ha protetto chiaramente il muscolo scheletrico: i topi trattati mantenevano più massa del tibiale, avevano presa più forte e presentavano fibre muscolari più grandi al microscopio rispetto ai topi settici non trattati. Nei muscoli, C188‑9 ha ridotto nettamente STAT3 attivato e abbassato i livelli di MuRF1 e atrogin‑1, ma ha lasciato i marcatori dell’autofagia sostanzialmente invariati. Negli esperimenti in vitro, il pretrattamento delle cellule muscolari con C188‑9 ha attenuato similmente l’attivazione di STAT3 e l’aumento di MuRF1 e atrogin‑1, e ha impedito il restringimento delle fibre indotto da LPS, sempre senza sopprimere l’autofagia.
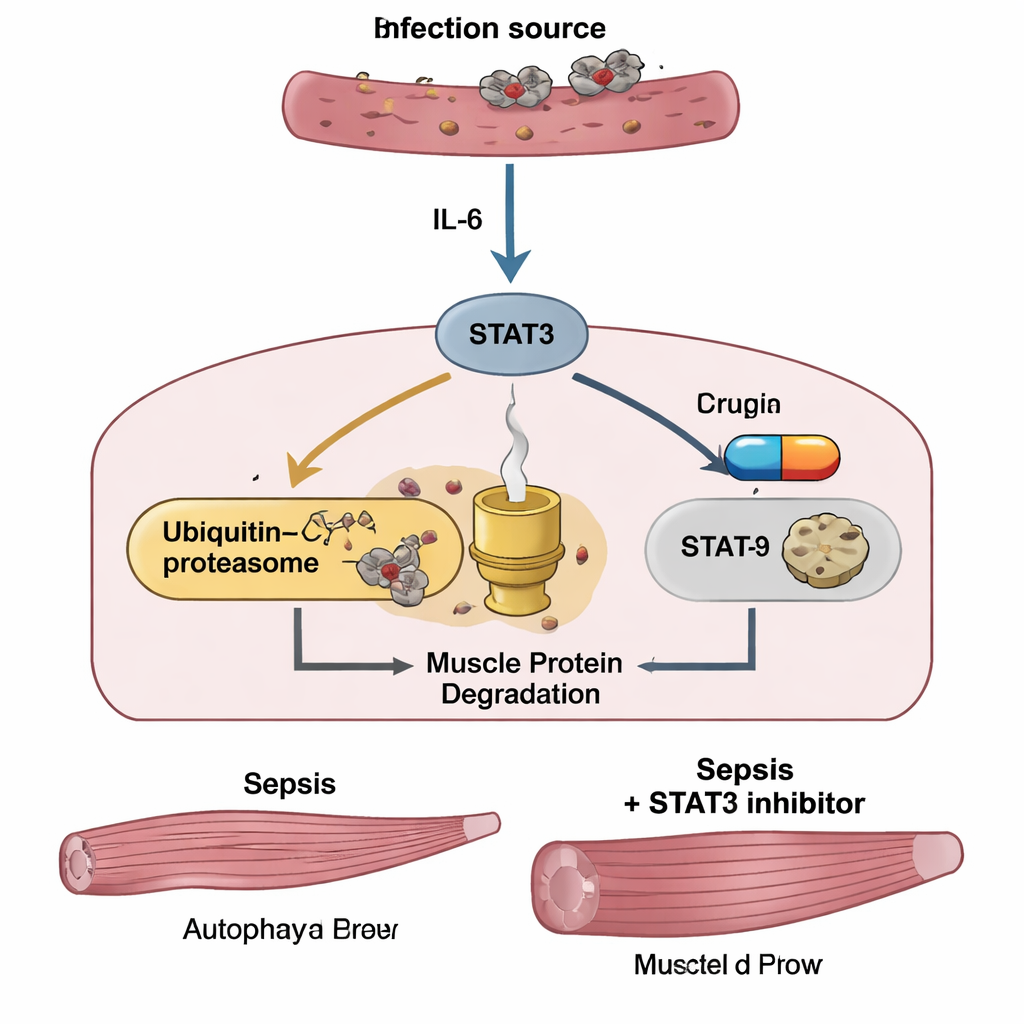
Indizi dai pazienti in terapia intensiva
Per verificare se questi meccanismi sono rilevanti nell’uomo, i ricercatori hanno seguito 67 adulti con sepsi ricoverati in terapia intensiva in Giappone. Gli esami del sangue all’ammissione hanno mostrato che i pazienti con shock settico avevano livelli di IL‑6 particolarmente elevati. Nel gruppo, l’IL‑6—ma non il TNF‑α—correlava strettamente con i punteggi di gravità della sepsi e con i marcatori ematici di infiammazione e danno muscolare. In un sottogruppo di 45 pazienti sottoposti a due TC dell’addome, i livelli di IL‑6 all’ammissione hanno predetto quanto il muscolo psoas a livello lombare si sarebbe ridotto nelle successive una‑tre settimane. Coloro che hanno perso più massa muscolare avevano una sopravvivenza a due anni nettamente peggiore rispetto a chi ne aveva mantenuta di più, sottolineando che l’atrofia legata alla sepsi non è solo estetica—è associata a mortalità a lungo termine.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, i dati da topi, cellule e pazienti delineano una storia plausibile: durante la sepsi, l’aumento di IL‑6 attiva STAT3 nei muscoli, che a sua volta stimola un sistema di degradazione proteica che spoglia le fibre muscolari del loro apparato contrattilе. Anche l’autofagia aumenta ma sembra meno direttamente controllata da STAT3. Bloccando farmacologicamente STAT3 con C188‑9, i ricercatori sono riusciti a interrompere questa via di “auto‑cannibalizzazione” nei topi e nelle cellule muscolari in coltura, preservando la forza pur in presenza di infezione e infiammazione. Sebbene questo lavoro sia ancora preclinico e non provi che gli inibitori di STAT3 saranno utili nei pazienti umani, indica l’asse IL‑6/STAT3 come un promettente bersaglio farmacologico per prevenire o ridurre la profonda debolezza muscolare che affligge molti sopravvissuti alla sepsi.
Citazione: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Parole chiave: sepsi, atrofia muscolare, STAT3, infiammazione, recupero da malattia critica