Clear Sky Science · it
Varianti di splicing di KChIP1 modulano i canali Kv4 promuovendo caratteristiche di inattivazione di tipo P/C
Come minuscoli pori modellano il ritmo elettrico del cervello
Ogni pensiero, ricordo e movimento nel cervello dipende da rapidi segnali elettrici nelle cellule nervose. Questi segnali sono finemente regolati da pori microscopici—i canali ionici—che permettono il passaggio di particelle cariche dentro e fuori la cellula. Questo articolo esplora come sottili variazioni di una proteina ausiliaria, KChIP1, possano cambiare in modo significativo il comportamento di una di queste famiglie di canali (i Kv4), modificando la facilità con cui i neuroni possono generare raffiche ripetute di attività elettrica.
I canali del potassio come pedale del freno del cervello
I canali Kv4 trasportano una cosiddetta corrente di potassio di tipo A che si attiva e disattiva rapidamente nel corpo cellulare e nei rami dei neuroni. Questa corrente contribuisce a determinare quanto facilmente un neurone si attiva e quanto fedelmente può seguire segnali in ingresso, specialmente a bassi tassi di scarica. I canali Kv4 non agiscono da soli: si assemblano con proteine ausiliarie in un complesso a tre componenti che include proteine DPP e proteine KChIP. Questi partner influenzano la rapidità con cui i canali si chiudono e quanto rapidamente ritornano pronti ad aprirsi. Finora la maggior parte degli studi suggeriva che i KChIP generalmente rendessero i canali Kv4 più rapidi nel recuperare dopo la disattivazione, permettendo ai neuroni di rispondere rapidamente a input ripetuti.
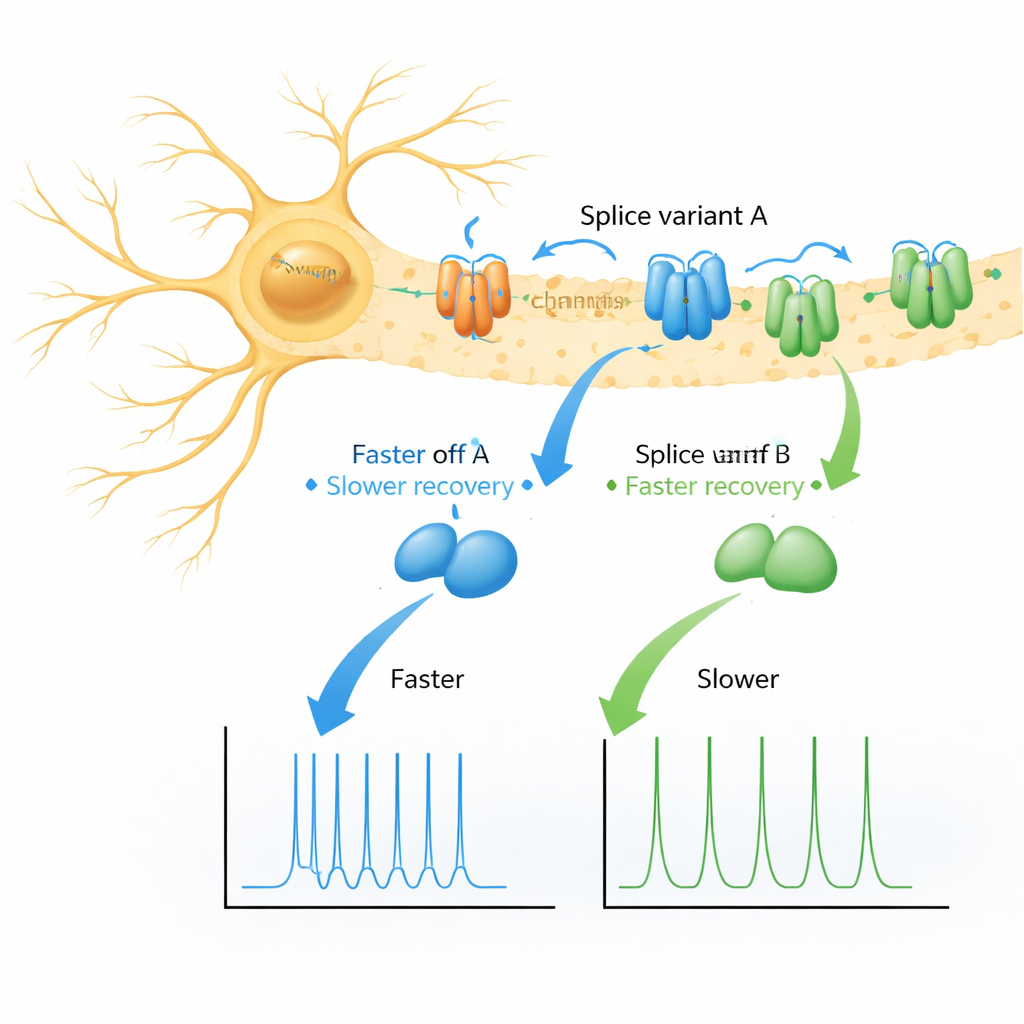
Due varianti proteiche, due modalità di recupero
Gli autori si sono concentrati su due versioni quasi identiche (varianti di splicing) di KChIP1, chiamate 1a e 1b, che differiscono solo per una breve “coda” aromatica all’inizio di 1b. Usando ovociti di rana come sistema sperimentale controllato, hanno espresso diversi tipi di canali Kv4 da soli, con ciascuna variante di KChIP1, con DPP o con entrambi gli ausiliari insieme. Come previsto, sia 1a sia 1b hanno lievemente rimodellato il modo in cui i canali si spegnevano durante un passo di tensione, senza effetti drammatici. La sorpresa è arrivata quando hanno esaminato il recupero dei canali dopo la disattivazione: invece di un singolo ritorno uniforme alla prontezza, i canali associati a 1a o 1b mostravano due fasi distinte di recupero—una rapida e una molto più lenta—con la via lenta molto più marcata per 1b.
Rivelata una via lenta nascosta
Quando i canali Kv4 venivano espressi senza KChIP1, recuperavano lungo un semplice percorso rapido, e la presenza di DPP accelerava ulteriormente questo processo. L’aggiunta di KChIP1 cambiava questo schema. Con 1a, la maggior parte dei canali recuperava ancora rapidamente, ma una piccola frazione faceva un lento deviazione verso lo stato pronto. Con 1b, una frazione molto più ampia entrava in questa via lenta, allungando il recupero su scale di secondi. Questo effetto è apparso in tutti i sottotipi di Kv4 testati e persisteva anche in presenza di DPP, indicando che la via lenta è una caratteristica intrinseca dei complessi contenenti KChIP1, non un artefatto di un particolare canale o della configurazione sperimentale. Gli autori hanno anche osservato che 1b spostava l’intervallo di voltaggio di “spegnimento” dei canali verso valori più negativi, favorendo ulteriormente la loro indisponibilità durante l’attività continua.
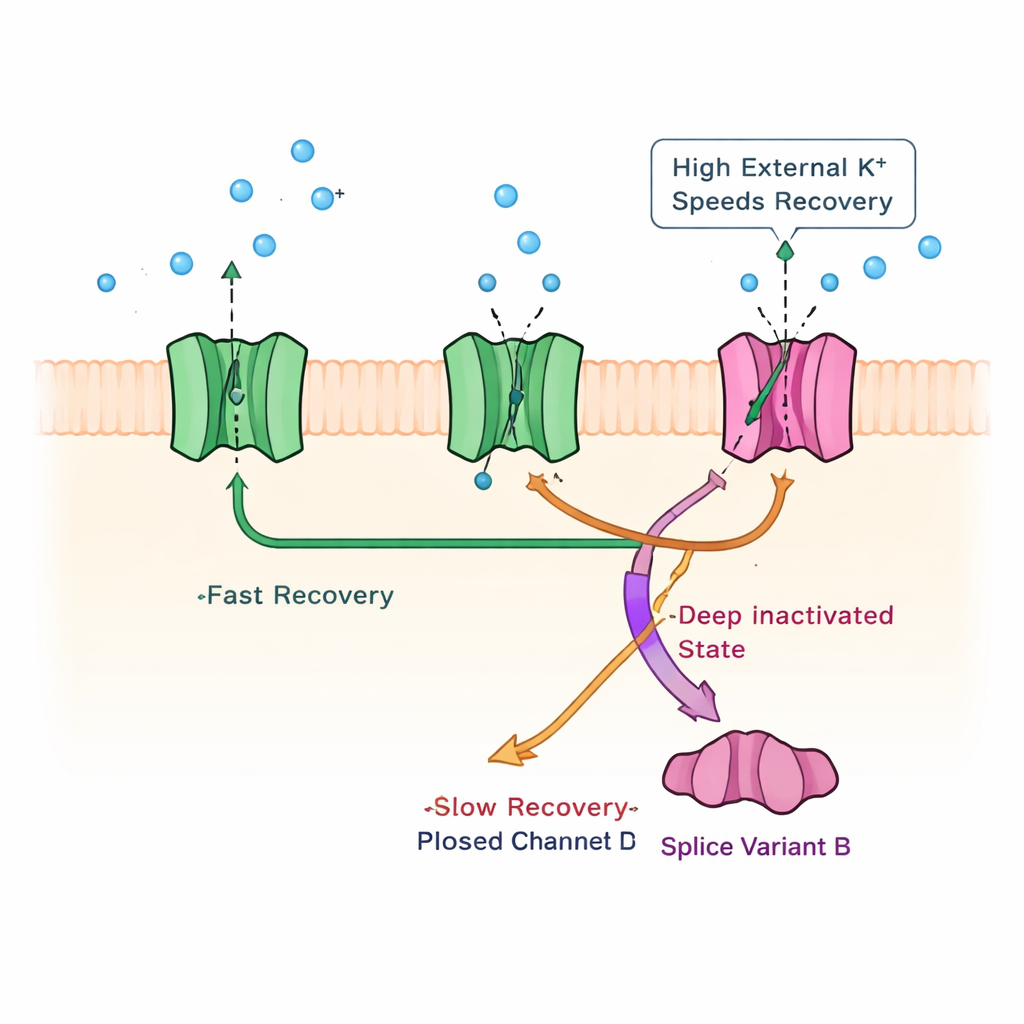
Scoprire un meccanismo di inattivazione dormiente
Per capire quale cambiamento fisico all’interno del canale fosse alla base di questo recupero lento, il gruppo ha indagato meccanismi di inattivazione noti in altri canali del potassio. Hanno escluso un classico blocco “palla-e-catenina” all’imbocco interno del canale tagliando parte della coda interna del canale; la fase lenta persisteva. Hanno poi usato alti livelli di potassio esterno, una tecnica nota per modificare un processo di inattivazione centrato sul poro in altri canali. In queste condizioni, la disattivazione della corrente divenne più rapida, ma, cosa cruciale, la fase di recupero lenta accelerò specificamente, come se l’elevato potassio liberasse i canali da uno stato bloccato profondo e di lunga durata. Mutazioni mirate in un segmento di gating del canale hanno ulteriormente supportato l’idea che KChIP1b promuova una via di inattivazione centrata sul poro—normalmente debole nei canali Kv4—che coesiste con la loro abituale, più veloce inattivazione nello stato chiuso.
Perché questo è rilevante per l’attività cerebrale
I risultati suggeriscono che scegliendo tra KChIP1a, KChIP1b o miscele di entrambi, i neuroni possono regolare finemente la velocità con cui le correnti di tipo A recuperano tra gli spike. Nelle cellule ricche di KChIP1b, una frazione significativa dei canali Kv4 viene “parcheggiata” in uno stato inattivato profondo e a lenta inversione, limitandone la disponibilità durante scariche rapide. Questo potrebbe permettere a certi interneuroni—cellule che coordinano e modulano l’attività nei circuiti cerebrali—di sparare a frequenze più alte o con schemi temporali distinti. In sostanza, una piccola differenza di splicing in una proteina ausiliaria sblocca una modalità di frenata nascosta nei canali del potassio, aggiungendo un nuovo livello di flessibilità al modo in cui il cervello controlla i propri ritmi elettrici.
Citazione: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
Parole chiave: Canali del potassio Kv4, Varianti di splicing di KChIP1, Corrente di tipo A, Eccitabilità neuronale, Inattivazione dei canali