Clear Sky Science · it
Forme fisiologicamente rilevanti dei traccianti radioattivi Tc‑ e Re‑pirofosfato e la base della loro sensibilità all’amiloide transtiretina
Perché questa storia sull’imaging cardiaco è importante
Molte persone sviluppano, con l’età, depositi silenti di proteine malripiegate chiamati amiloidi nel cuore. Alcuni di questi depositi, in particolare quelli derivati da una proteina plasmaticaper chiamata transtiretina, possono irrigidire il cuore e portare a malattia grave. I medici fanno sempre più affidamento su un tracciante radioattivo noto come pirofosfato di tecnetio‑99m (99mTc‑PYP) per visualizzare questi depositi nelle scansioni. Eppure, sorprendentemente, la forma esatta di questo tracciante nell’organismo e il motivo per cui sembra “preferire” certi tipi di amiloide non erano chiari. Questo articolo combina teoria ed esperimento per scoprire quale sia effettivamente la forma del tracciante in condizioni fisiologiche e come questa conformazione possa permettergli di riconoscere i fibrilli tossici di transtiretina.
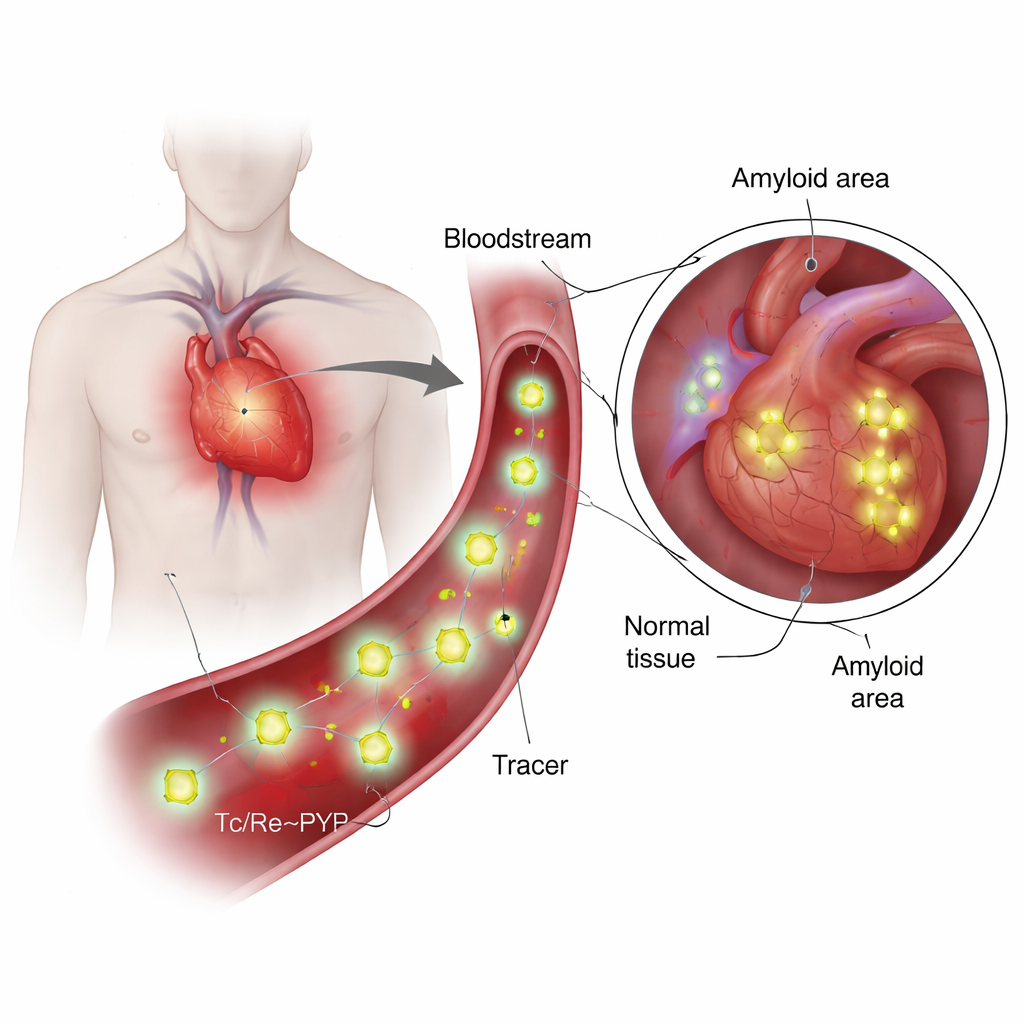
Che cosa sono questi traccianti e perché sono speciali?
Il 99mTc‑PYP è stato usato per decenni per l’imaging osseo, perché tende ad accumularsi dove il turnover di calcio e minerali è elevato. Più recentemente i medici hanno scoperto che può anche distinguere tra due principali tipi di amiloidosi cardiaca: una costituita da catene leggere di anticorpi (AL) e una dalla transtiretina (ATTR). Nell’ATTR, il cuore spesso appare fortemente positivo alle scansioni PYP, mentre i casi AL tendono a rimanere deboli, anche quando l’accumulo di calcio sembra simile. Questa discrepanza ha sollevato una domanda chiave: il tracciante si lega solo al calcio o interagisce direttamente con la proteina amiloide? Rispondere richiede di conoscere la vera struttura chimica del tracciante in condizioni simili a quelle del sangue, un aspetto che i lavori precedenti avevano delineato solo in modo sommario.
Usare un sostituto più sicuro per vedere l’invisibile
Poiché il tecnetio è radioattivo ed è presente in quantità minime nelle preparazioni mediche, è difficile studiarlo direttamente con molte tecniche di laboratorio. Gli autori hanno quindi utilizzato il renio, un elemento strettamente correlato per dimensioni e preferenze di legame ma con chimica più comoda da analizzare, come sostituto. Hanno preparato miscele di renio‑pirofosfato in condizioni che imitano i kit clinici PYP e le hanno quindi indagate con una batteria di strumenti: calcoli di chimica quantistica di alto livello, spettroscopia UV‑visibile, varie spettroscopie vibrazionali (infrarosso e Raman), risonanza magnetica nucleare, spettrometria di massa e spettroscopia Mössbauer dello stagno. Insieme, questi metodi hanno permesso di testare molte strutture candidate e di restringere quali specie siano probabili a pH neutro, come quello del sangue.
Una forma molecolare flessibile ma riconoscibile
Le evidenze combinate indicano un “nucleo” comune: un complesso ottaedrico in cui un atomo di tecnetio o renio nello stato di ossidazione +4 è legato a due gruppi pirofosfato e a due molecole d’acqua. In termini semplici, il metallo si trova al centro di una gabbia quasi ottaedrica formata da atomi di ossigeno, con i pirofosfati che fungono da ancore multidentate e le molecole d’acqua che occupano le posizioni rimanenti. Questa unità diaqua dipirofosfato non è rigida. Poiché i bracci del pirofosfato possono ruotare e formare legami idrogeno interni con le acque legate, la molecola esplora molte forme leggermente diverse in soluzione. Calcoli e spettri suggeriscono che queste variazioni spostano le sue impronte di assorbimento della luce e le bande vibrazionali, spiegando perché i segnali sperimentali risultano larghi e perché studi precedenti hanno faticato a identificare una singola struttura netta.
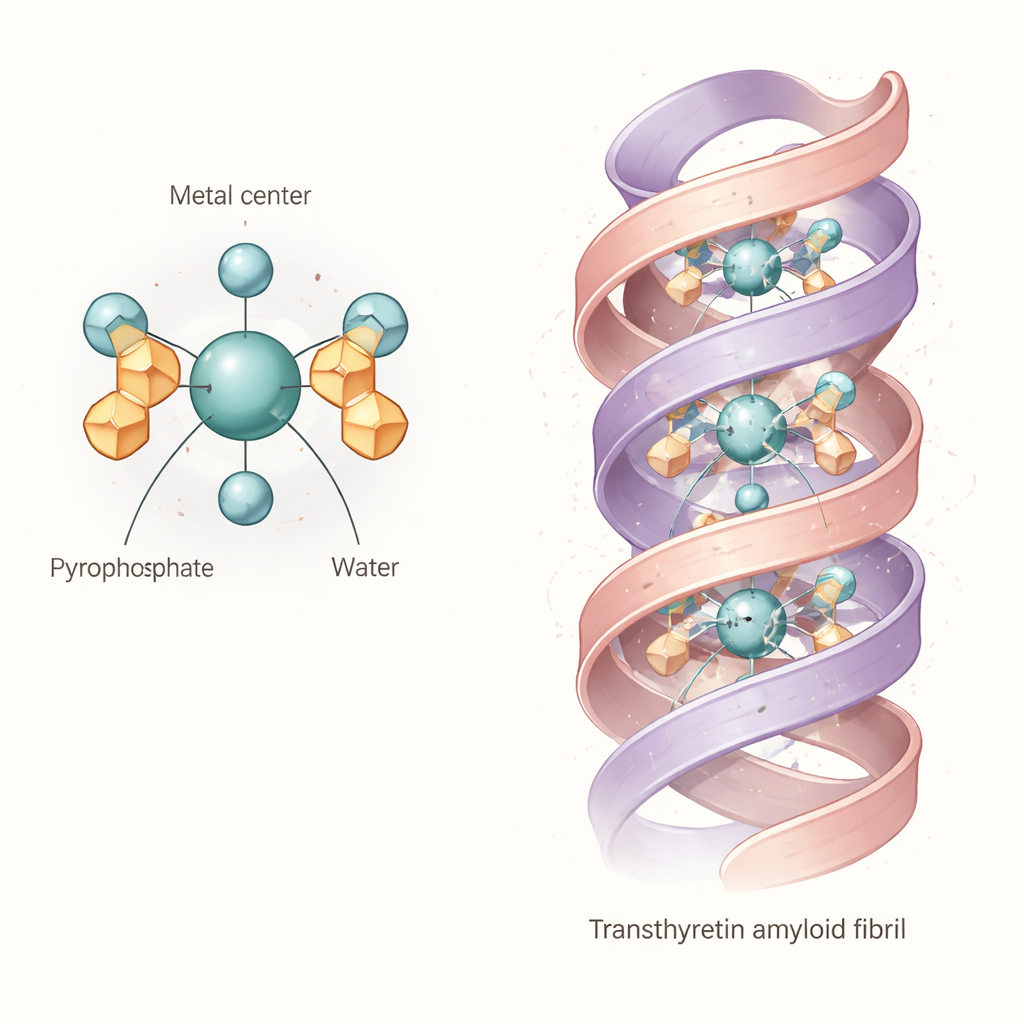
Cosa significa per il legame con l’amiloide cardiaca
Gli autori si sono poi chiesti se questo complesso flessibile potesse plausibilmente inserirsi direttamente nei fibrilli di transtiretina. Utilizzando una struttura criomicroscopica dettagliata di un fibrillo umano di transtiretina, hanno effettuato ricerche di docking computazionale con il complesso modellato di tecnetio‑pirofosfato. I risultati mostrano che l’unità diaqua dipirofosfato può adattarsi in un canale centrale che corre lungo il fibrillo, formando molteplici legami idrogeno e ponti salini con catene laterali cariche che fiancheggiano la cavità. Ciò suggerisce che, almeno per alcune conformazioni dei fibrilli di transtiretina, il tracciante non si limita a marcare depositi minerali vicini; può essere effettivamente trattenuto dallo scheletro proteico stesso. La “cedevolezza” strutturale del tracciante probabilmente lo aiuta ad adattarsi a tasche e pattern di carica leggermente diversi nei fibrilli reali dei pazienti.
Implicazioni per la diagnosi e per futuri traccianti
Per il lettore non tecnico, la conclusione è che la diffusamente usata scansione cardiaca PYP si basa su un tracciante più sottile e sensibile alle proteine di quanto si pensasse in precedenza. In condizioni fisiologiche, è meglio considerarlo come una piccola gabbia metallica‑pirofosfato contenente acqua, capace di flettersi e di stabilire molteplici punti di contatto con i canali dell’amiloide transtiretina. Questa intuizione aiuta a spiegare perché il tracciante fornisce segnali forti in alcune malattie da amiloide ma non in altre, e perché piccole variazioni nella proteina o nel suo ambiente possono causare perdite di sensibilità difficili da interpretare. Chiarendo la forma di lavoro e la distribuzione di carica del tracciante, lo studio pone le basi per progettare agenti di imaging o terapeutici di nuova generazione che riconoscano in modo più selettivo i fibrilli responsabili della malattia nel cuore e oltre.
Citazione: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Parole chiave: amiloidosi cardiaca, transtiretina, pirofosfato di tecnetio, imaging molecolare, chimica dei radiotraccianti