Clear Sky Science · it
Attività sinergiche anti-persister, inibitorie dell’efflusso e antibiofilm dei postbiotici vaginali derivati da Lactobacillus contro UPEC: verso una nuova terapia per le IVU
Perché le infezioni urinarie ostinate sono importanti
Le infezioni del tratto urinario (IVU) sono tra le infezioni batteriche più comuni, soprattutto nelle donne, e molte persone le sperimentano ripetutamente nonostante l’uso di antibiotici. Questo studio esplora un nuovo approccio che limita l’uso di antibiotici per affrontare quelle infezioni recidivanti e resistenti: sfruttare i batteri vaginali benefici e i loro prodotti chimici per fermare l’Escherichia coli problematico prima che si insedi, si nasconda e ricompaia.
I sopravvissuti nascosti dietro le recidive
Gli antibiotici standard possono eliminare la maggior parte dei batteri, ma una piccola sottopopolazione nota come “cellule persister” sopravvive entrando in uno stato dormiente a bassa attività. Questi «dormienti» non sono resistenti dal punto di vista genetico, ma tollerano dosi estremamente elevate di antibiotici e possono riattivarsi più tardi, causando IVU croniche e ricorrenti. I ricercatori hanno lavorato con un ceppo comune responsabile di IVU, E. coli UTI89, e hanno dimostrato che potenti antibiotici come colistina e meropenem inducono facilmente queste cellule persister. Nei test di laboratorio che imitano le condizioni urinarie, piccole frazioni di E. coli hanno resistito a esposizioni antibiotiche estreme, confermando quanto facilmente possano emergere i persister e perché i regimi farmacologici standard spesso non danno sollievo duraturo.
Trasformare i batteri vaginali amichevoli in una terapia
Una vagina sana è di solito dominata da specie di Lactobacillus, che aiutano a mantenere sotto controllo i microrganismi dannosi. Invece di usare batteri vivi “probiotici”, questo studio si è concentrato sul loro surnatante privo di cellule—essenzialmente il cocktail di molecole che secernono, chiamato postbiotici. Da ceppi vaginali di Lactobacillus raccolti da donne sane, il team ha separato e analizzato questi composti secretati. Due metaboliti chiave, l’anfidride itaconica e il (−)-terpinen-4-olo, si sono distinti per la loro capacità di agire insieme e ridurre drasticamente il numero di cellule persister di E. coli quando combinati con antibiotici. Un terzo composto, la triptamina, precedentemente dimostrata capace di degradare la matrice vischiosa del biofilm che i batteri costruiscono per proteggersi, è stato aggiunto per rafforzare l’azione antibiofilm.
Come la nuova miscela indebolisce i batteri difficili da uccidere
Gli scienziati hanno rilevato che queste molecole derivate da Lactobacillus attaccano le persister di E. coli su più fronti contemporaneamente. Primo, aumentano la produzione di specie reattive dell’ossigeno—forme chimiche altamente reattive dell’ossigeno che danneggiano componenti batterici—rendendo gli antibiotici molto più letali per le cellule dormienti. Quando sono stati aggiunti antiossidanti, questo effetto letale è diminuito, sottolineando il ruolo dello stress ossidativo. Secondo, i composti rendono la membrana esterna batterica più “permeabile”, come dimostrato da coloranti fluorescenti che penetrano più facilmente nelle cellule dopo il trattamento. Terzo, inibiscono le «pompe di efflusso» cellulari, i piccoli macchinari che normalmente espellono gli antibiotici dalla cellula. Con le pompe bloccate, più farmaco rimane all’interno dei batteri e sopravvivono meno persister. Insieme, questi cambiamenti hanno ridotto biofilm preformati di E. coli fino a dieci ordini di grandezza nei test in vitro, senza danneggiare le cellule immunitarie dei mammiferi alle dosi testate.
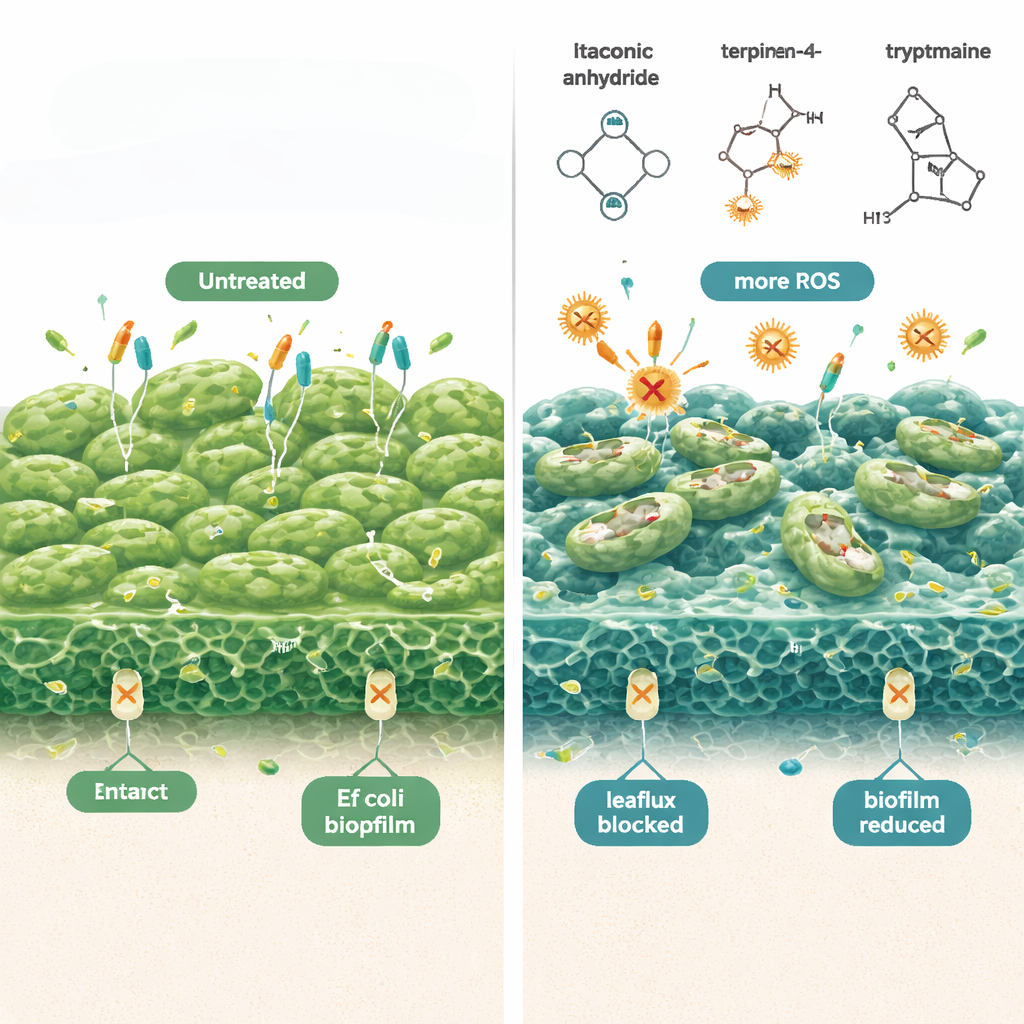
Dal banco di laboratorio a un lavaggio vaginale pratico
Per tradurre questi risultati in qualcosa di utilizzabile nella vita quotidiana, il team ha progettato un lavaggio vaginale personalizzato usando una base in gel termosensibile chiamata poloxamero 407. A temperatura ambiente si comporta come un fluido per facilitare l’applicazione, quindi si addensa delicatamente a temperatura corporea per migliorare il contatto con le pareti vaginali. Il gel contiene una combinazione definita e sicura di anidride itaconica, (−)-terpinen-4-olo e triptamina. Nei piatti di laboratorio, questa formulazione ha funzionato su un intervallo di valori di pH simile a quello vaginale, sopprimendo fortemente la formazione del biofilm di E. coli e riducendo il numero di batteri vitali di circa nove ordini di grandezza. È rimasta stabile e biologicamente attiva per almeno tre mesi in conservazione fredda e ha mostrato anche un’azione ampia contro altri batteri problematici come Klebsiella, MRSA e Pseudomonas.
Testare sicurezza e protezione nei topi
Successivamente, i ricercatori hanno valutato il lavaggio in un modello murino di infezione vaginale da E. coli. I topi sono stati inoculati con E. coli marcato con GFP e poi trattati con il nuovo lavaggio a base di metaboliti, un lavaggio probiotico contenente Lactobacillus vivi, un lavaggio vaginale commerciale o un placebo. Gli animali che hanno ricevuto il lavaggio metabolico personalizzato hanno mostrato un’infiammazione vaginale notevolmente ridotta, hanno mantenuto il peso corporeo e avevano conte batteriche nel secreto vaginale drasticamente inferiori rispetto agli altri gruppi. Più sorprendente, nei topi trattati non è stata rilevata E. coli nelle urine, nella vescica, nei reni o nei tessuti vaginali e la funzione renale è rimasta normale, indicando che la formulazione non solo ha ridotto l’infezione locale ma ha anche prevenuto la diffusione al tratto urinario superiore.
Cosa potrebbe significare per le persone con IVU ricorrenti
Lo studio conclude che un lavaggio vaginale costruito a partire da metaboliti precisi prodotti da specie di Lactobacillus naturalmente protettive può indebolire l’E. coli responsabile delle IVU in modi multipli: riducendo le popolazioni di persister, disgregando i biofilm e rendendo gli antibiotici standard più efficaci. Poiché l’approccio si basa su molecole non vive piuttosto che su batteri vivi o su lunghi cicli di farmaci sistemici, potrebbe essere più sicuro, più stabile e più facile da regolamentare. Pur essendo ancora necessari studi clinici sull’uomo, questo lavaggio a base di metaboliti indica un futuro in cui le IVU ricorrenti si prevengono non solo con antibiotici più potenti, ma potenziando in modo intelligente le difese microbiche naturali del corpo alla fonte.
Citazione: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Parole chiave: infezione del tratto urinario, microbioma vaginale, postbiotici di Lactobacillus, tolleranza agli antibiotici, biofilm batterici