Clear Sky Science · it
Impatto prognostico delle nicchie spaziali nel cancro della prostata
Perché il “quartiere” del tumore conta
Il cancro della prostata è comune, ma non tutti i tumori si comportano allo stesso modo. Alcuni crescono lentamente, mentre altri progrediscono rapidamente e minacciano la vita dei pazienti. I medici si basano attualmente su marcatori come i livelli di PSA e la classificazione al microscopio per stimare quali tumori siano pericolosi. Questo studio pone una domanda nuova: il punto preciso in cui le cellule cancerose si trovano all’interno del tumore — il bordo esterno più attivo rispetto al nucleo più profondo — può aiutare a prevedere l’evoluzione clinica di un paziente?
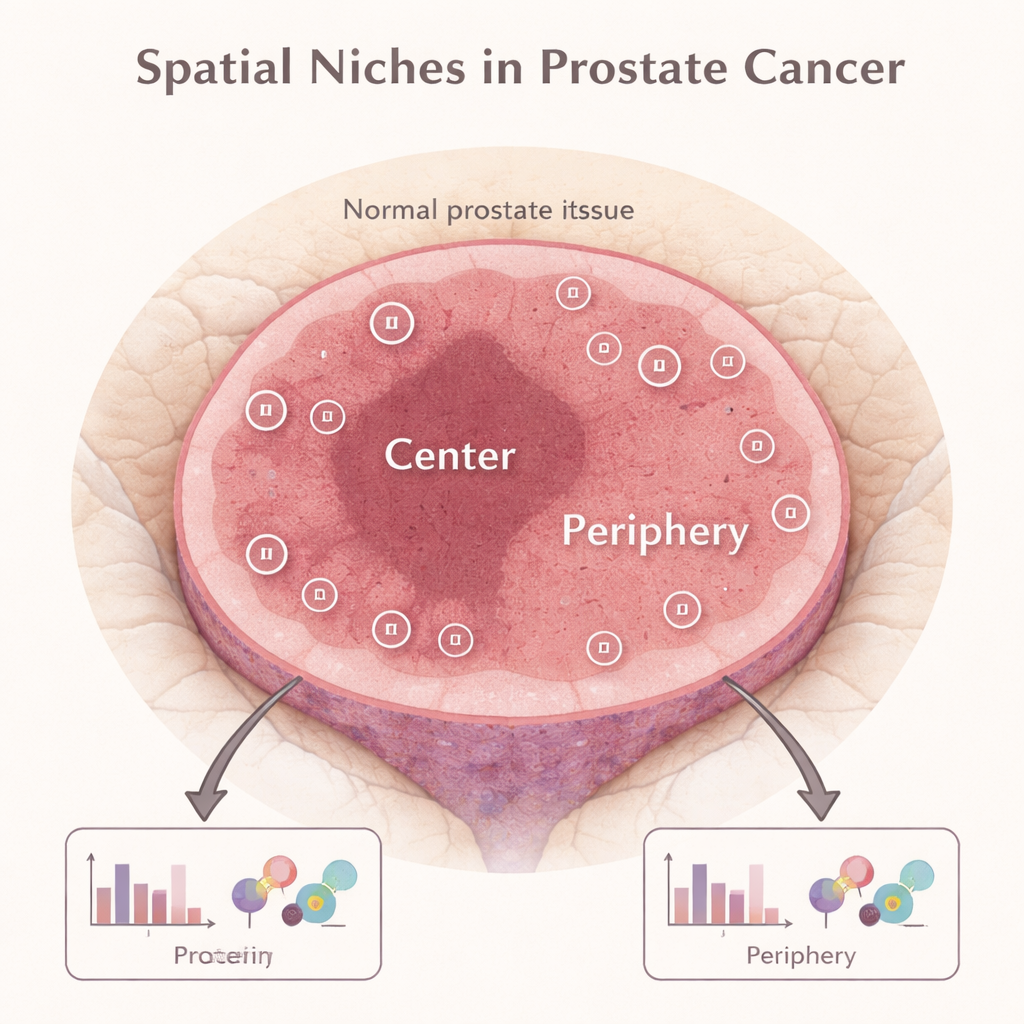
Vedere il tumore come un piccolo ecosistema
La ricerca moderna mostra che un tumore non è una palla uniforme di cellule identiche. Piuttosto, assomiglia a un piccolo ecosistema con “quartieri” distinti, o nicchie spaziali. Nel cancro della prostata, il nucleo interno del tumore e il margine esterno dove il cancro incontra il tessuto normale possono ospitare miscele diverse di cellule tumorali, cellule immunitarie e strutture di supporto. Gli autori hanno utilizzato una tecnologia chiamata profilazione spaziale digitale, che consente di misurare dozzine di proteine direttamente in sottili sezioni di tessuto tumorale conservato, mantenendo traccia del punto esatto del tumore da cui proviene ogni misurazione.
Misurare le proteine nel centro e nel bordo del tumore
Il gruppo ha analizzato campioni tumorali di 49 uomini con carcinoma prostatico ad alto rischio sottoposti a intervento chirurgico. Per ogni tumore hanno selezionato regioni nel centro e al perimetro e hanno misurato i livelli di 46 diverse proteine correlate a cellule immunitarie, morte cellulare e segnali di crescita. Ciò ha prodotto decine di migliaia di punti dati. Analizzando separatamente centro e perimetro del tumore, hanno confermato che queste aree si comportano in modo diverso: molte proteine, specialmente quelle legate all’attività immunitaria, erano più abbondanti al margine esterno del tumore, mentre alcuni regolatori della morte cellulare risultavano più elevati nel centro.
Quando le visuali separate non bastano
I ricercatori hanno quindi verificato se i pattern proteici osservati solo nel centro o solo al perimetro potessero prevedere per quanto tempo i pazienti sarebbero rimasti liberi da progressione della malattia dopo l’intervento. Usando metodi statistici per raggruppare i pazienti in base ai pattern proteici in ciascun compartimento preso singolarmente, hanno identificato due principali cluster sia per il centro sia per il perimetro. Tuttavia, nessuno di questi insiemi di cluster si è allineato con l’effettivo andamento clinico dei pazienti nel tempo, né ha mostrato una correlazione chiara con fattori di rischio classici come il punteggio di Gleason o mutazioni genetiche note come BRCA1/2 e TP53. In altre parole, osservare uno solo dei “quartieri” in isolamento non ha fornito un nuovo marcatore prognostico utile.
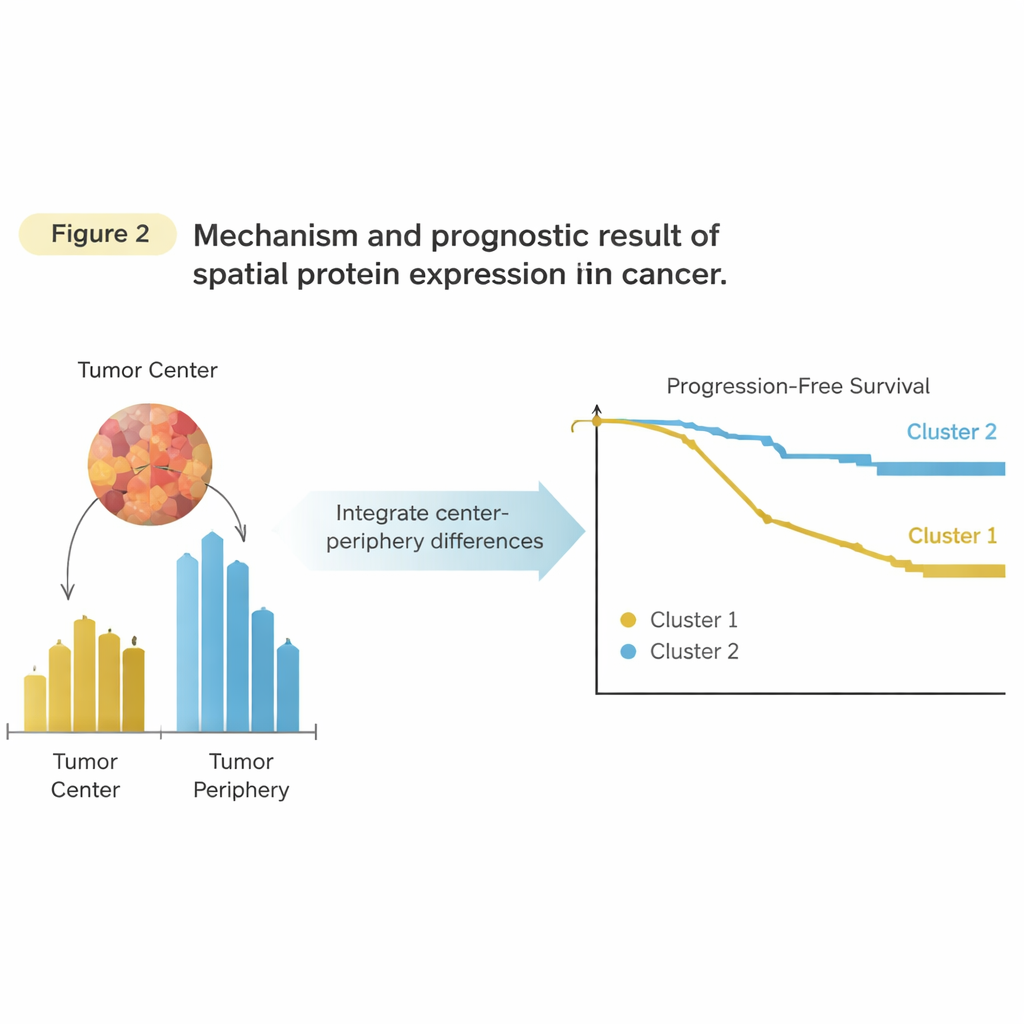
Combinare entrambi i quartieri rivela un segnale
Il passo chiave è stato combinare le informazioni di centro e perimetro invece di trattarle separatamente. Per ogni proteina e per ogni paziente, i ricercatori hanno calcolato quanto più (o meno) quella proteina fosse espressa nel perimetro rispetto al centro. Questo ha prodotto un unico “valore di bilancio” per proteina che catturava comunque dove la proteina fosse più elevata all’interno del tumore. Raggruppando i pazienti in base a questi bilanci spaziali, sono emersi due nuovi cluster. Questa volta i cluster erano rilevanti: un gruppo aveva un tempo di progressione della malattia molto più breve rispetto all’altro. È importante notare che la forza di questo approccio non derivava da una singola proteina predominante, ma dal pattern spaziale complessivo di molte proteine, in particolare quelle legate alle cellule immunitarie e al rimodellamento tissutale al margine del tumore.
Cosa potrebbe significare per i pazienti
Per le persone affette da cancro della prostata, questi risultati suggeriscono che la posizione in cui le proteine sono espresse all’interno del tumore — non solo la quantità totale — può fornire indizi preziosi sul comportamento futuro della malattia. Pur essendo uno studio di piccole dimensioni e basato su una tecnologia specialistica e costosa, fornisce una prova di principio che misure proteiche con consapevolezza spaziale possono rivelare informazioni prognostiche che i test standard non colgono. Con ulteriori validazioni e metodi di laboratorio più semplici, questo tipo di biomarker spaziale potrebbe un giorno aiutare i medici a distinguere meglio quali carcinomi prostatici ad alto rischio sono destinati a progredire rapidamente e quali potrebbero seguire un decorso più gestibile, portando a decisioni terapeutiche più mirate.
Citazione: Schneider, F., Böning, S.H., Antunes, B.C. et al. Prognostic impact of spatial niches in prostate cancer. Sci Rep 16, 2598 (2026). https://doi.org/10.1038/s41598-026-35720-1
Parole chiave: cancro alla prostata, profilazione spaziale, microambiente tumorale, biomarker prognostico, eterogeneità intratumorale