Clear Sky Science · it
La proteina Vpr dell’HIV induce la demetilazione del promotore antisenso di SNCA, portando a deficit neurocognitivi
Perché l’HIV può ancora colpire il cervello
Le persone che vivono con l’HIV oggi vivono più a lungo e in migliore salute grazie ai farmaci antiretrovirali moderni. Tuttavia molti continuano a sperimentare problemi di memoria, concentrazione e movimento, anche quando il virus nel sangue è ben controllato. Questo studio indaga il perché concentrandosi su una piccola proteina virale, chiamata Vpr, e su una proteina cerebrale, l’alfa‑sinucleina, anch’essa centrale nel morbo di Parkinson. Capire come interagiscono queste due molecole può spiegare perché l’HIV accelera l’invecchiamento cerebrale e suggerire nuovi modi per proteggere il cervello.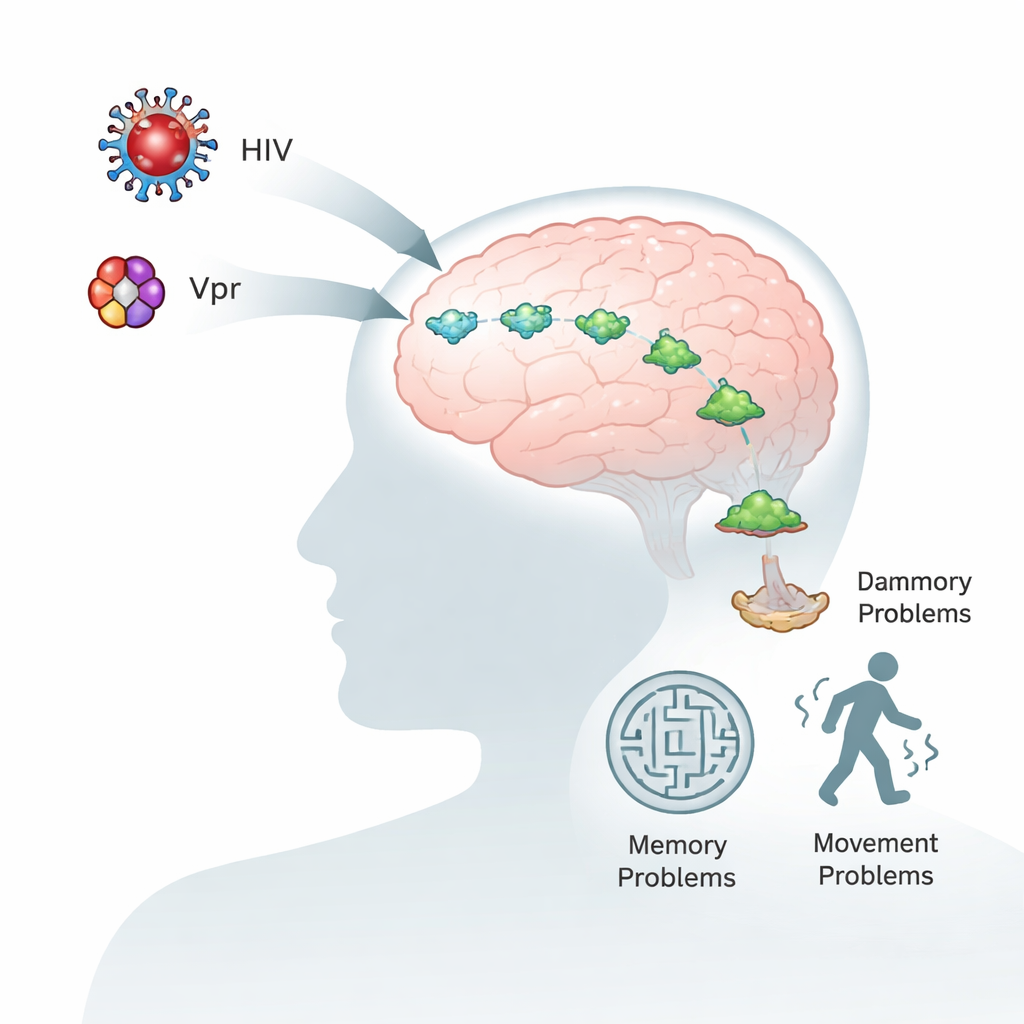
Una proteina cerebrale al crocevia tra HIV e Parkinson
L’alfa‑sinucleina è una proteina che aiuta i neuroni a comunicare, soprattutto in aree cerebrali che controllano il movimento e la memoria. Quando l’alfa‑sinucleina si accumula in eccesso, forma ammassi che danneggiano le sinapsi, sovraccaricano i mitocondri produttori di energia e alimentano l’infiammazione. Tali aggregati sono una caratteristica del morbo di Parkinson. Gli autori mostrano che l’alfa‑sinucleina si accumula anche con il normale invecchiamento nei topi, e che la proteina Vpr dell’HIV ne aumenta ulteriormente i livelli nelle cellule con caratteristiche neuronali. Questo pone l’alfa‑sinucleina al crocevia tra i problemi cognitivi associati all’HIV e i classici disturbi del movimento.
Come una proteina virale riscrive la “punteggiatura” cellulare
Ogni cellula usa etichette chimiche sul DNA—spesso descritte come segni di punteggiatura molecolare—per accendere o spegnere i geni. In questo lavoro il team si è concentrato su un interruttore di controllo poco noto all’interno del gene dell’alfa‑sinucleina chiamato promotore antisenso. Nelle cellule sane questo interruttore è fortemente marcato con gruppi metile, che lo mantengono relativamente silente. I ricercatori hanno trovato che Vpr rimuove queste marcature in siti specifici di questa regione, un processo noto come demetilazione. Una volta rimossi questi segni, il promotore antisenso diventa più attivo e stimola una produzione aggiuntiva di alfa‑sinucleina, creando le condizioni per un aggregazione dannosa.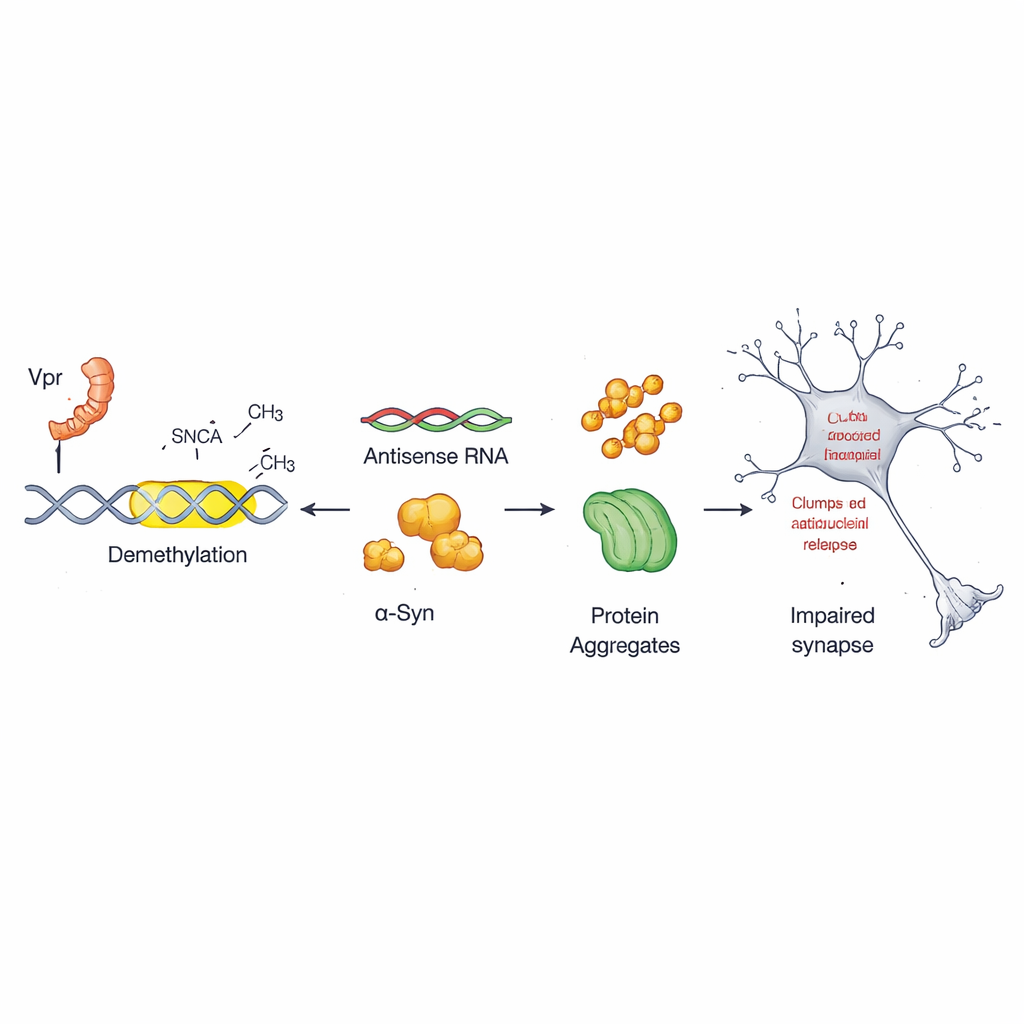
Evidenze da cellule, topi e cervelli umani
Usando cellule umane coltivate con caratteristiche neuronali e neuroni primari di topo, gli autori hanno mostrato che l’aggiunta di Vpr aumenta nel tempo i livelli di trascritto e di proteina dell’alfa‑sinucleina. Un farmaco che promuove in modo generale la demetilazione del DNA ha riprodotto alcuni di questi effetti, sottolineando il ruolo del controllo epigenetico. Al contrario, un composto chiamato DMOG, che inibisce gli enzimi demetilanti, ha impedito a Vpr di attivare pienamente il promotore antisenso. Il gruppo ha poi esaminato campioni di cervello umano provenienti da persone con e senza HIV. I cervelli dei donatori HIV‑positivi—sia prima sia dopo il trattamento antiretrovirale—mostravano meno marcature metiliche nella stessa regione del DNA e livelli più alti di alfa‑sinucleina e del suo trascritto antisenso, specialmente nei donatori con demenza correlata all’HIV. Questo suggerisce che il virus lascia una cicatrice epigenetica durevole nel cervello.
Dai cambiamenti molecolari ai problemi di memoria
Per collegare questi cambiamenti molecolari al comportamento, i ricercatori hanno esaminato come Vpr influenza i circuiti cerebrali nei topi. Quando hanno applicato Vpr a fette di ippocampo di topo, una regione vitale per la memoria, l’intensità del segnale di base tra i neuroni non è cambiata, ma la capacità di rafforzare le connessioni—un processo chiamato potenziamento a lungo termine—è risultata ridotta. Nei topi vivi, iniezioni mirate di Vpr nell’ippocampo hanno portato a prestazioni peggiori in un compito di memoria spaziale in cui gli animali devono ricordare la posizione degli oggetti. Nel loro insieme, questi esperimenti suggeriscono che i cambiamenti dell’alfa‑sinucleina indotti da Vpr non sono solo curiosità biochimiche; si traducono in sinapsi indebolite e deficit di memoria misurabili.
Cosa significa per le persone che vivono con l’HIV
Questo studio propone una catena di eventi chiara: l’HIV rilascia Vpr, Vpr riprogramma un interruttore chiave del DNA che controlla l’alfa‑sinucleina, la proteina si accumula e aggrega, e i neuroni perdono gradualmente la capacità di comunicare e sostenere la memoria. Poiché problemi simili con l’alfa‑sinucleina sono alla base del morbo di Parkinson, il lavoro lascia intendere che l’HIV e le malattie neurodegenerative classiche condividono meccanismi sovrapposti. Importante, i risultati evidenziano possibili nuove strategie—come farmaci che stabilizzano la metilazione del DNA al promotore antisenso o che limitano l’accumulo di alfa‑sinucleina—per rallentare o prevenire il declino cognitivo e i problemi di movimento legati all’HIV.
Citazione: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Parole chiave: Disturbi neurocognitivi associati all’HIV, alfa-sinucleina, epigenetica, metilazione del DNA, Sintomi simili al Parkinson