Clear Sky Science · it
Riprogettazione razionale di una DNAzima G-quadruplex ad alta attività tramite basi flangiate e anelli
Piccole macchine di DNA con grande potenziale
Immaginate di sostituire fragili enzimi proteici con sottili filamenti di DNA che sopravvivono a calore, agenti chimici e manipolazioni brusche, pur svolgendo reazioni chimiche utili. Questo studio esplora esattamente quell’idea. I ricercatori modificano strutture di DNA speciali in modo che si comportino come minuscoli enzimi detergenti, capaci di usare il perossido di idrogeno per generare un segnale intenso. Queste “macchine” di DNA, più robuste e più veloci, potrebbero rendere i test medici futuri, i sensori ambientali e i dispositivi diagnostici portatili più economici, affidabili e facili da usare al di fuori del laboratorio.
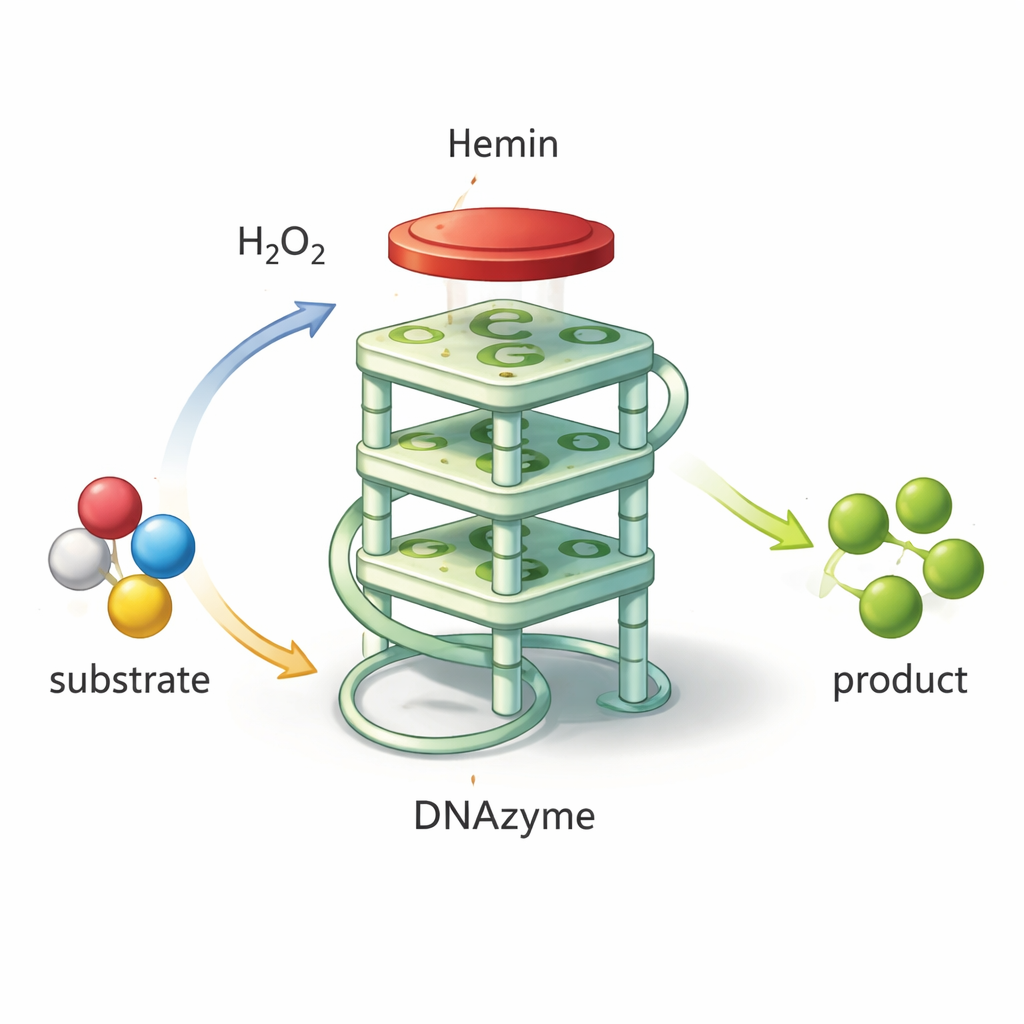
Trasformare il DNA in un piccolo strumento chimico
Non tutto il DNA è soltanto un supporto passivo dell’informazione genetica. Alcune sequenze corte possono ripiegarsi in forme insolite che catturano molecole specifiche o addirittura accelerano reazioni chimiche. Una di queste conformazioni è il G‑quadruplex, in cui il DNA ricco di guanine si organizza in un impilamento compatto a quattro livelli. Quando una piccola molecola contenente ferro chiamata emina si posiziona sopra questo impilamento, la coppia agisce come una “DNAzima”: un catalizzatore a base di DNA che imita le perossidasi naturali. Può usare il perossido di idrogeno per ossidare una sostanza che cambia colore, producendo un segnale verde intenso facilmente misurabile. Poiché queste DNAzime sono economiche da produrre, altamente stabili e semplici da riprogettare, rappresentano elementi promettenti per biosensori che rilevano patogeni, tossine o marcatori di malattia.
Perché gli attuali enzimi di DNA hanno bisogno di un aggiornamento
Nonostante le loro promesse, la maggior parte delle DNAzime è ancora più lenta e meno efficiente degli enzimi proteici presenti in natura. I biosensori esistenti spesso devono amplificare il bersaglio con tecniche come la PCR o aggiungere sostanze ausiliarie, aumentando costi e complessità. Tentativi precedenti di migliorare le DNAzime hanno incluso collegare due unità di DNA, fissare l’emina in modo permanente o circondare il sito reattivo con gruppi chimici aggiuntivi. Questi accorgimenti talvolta aiutano, ma possono anche introdurre ingombro che ostacola la funzione o richiedere chimica elaborata. Una domanda aperta fondamentale è come semplici modifiche alle basi di DNA vicine — in particolare quelle che non rompono la struttura centrale a G‑quadruplex — possano modulare l’attività in modo prevedibile e «progettabile».
Riprogettare un DNA enzima ad alte prestazioni
Il team si è concentrato su una DNAzima particolarmente attiva nota come B730, che già figura tra i migliori catalizzatori G‑quadruplex non modificati. Hanno alterato sistematicamente il DNA appena fuori dal nucleo aggiungendo o riposizionando basi comuni come adenina, timina e citosina nelle regioni ad anello e nella coda. Una versione riprogettata, chiamata B730‑1.2, combinava adenine aggiunte negli anelli con una breve coppia timina–citosina a un’estremità del filamento. In condizioni moderate di perossido di idrogeno, questa variante ha triplicato la velocità iniziale della reazione e circa quadruplicato la quantità totale di prodotto colorato rispetto all’originale B730. Ha inoltre superato chiaramente altri due noti DNAzimi, AS1411 e CatG4, quando testati in parallelo.
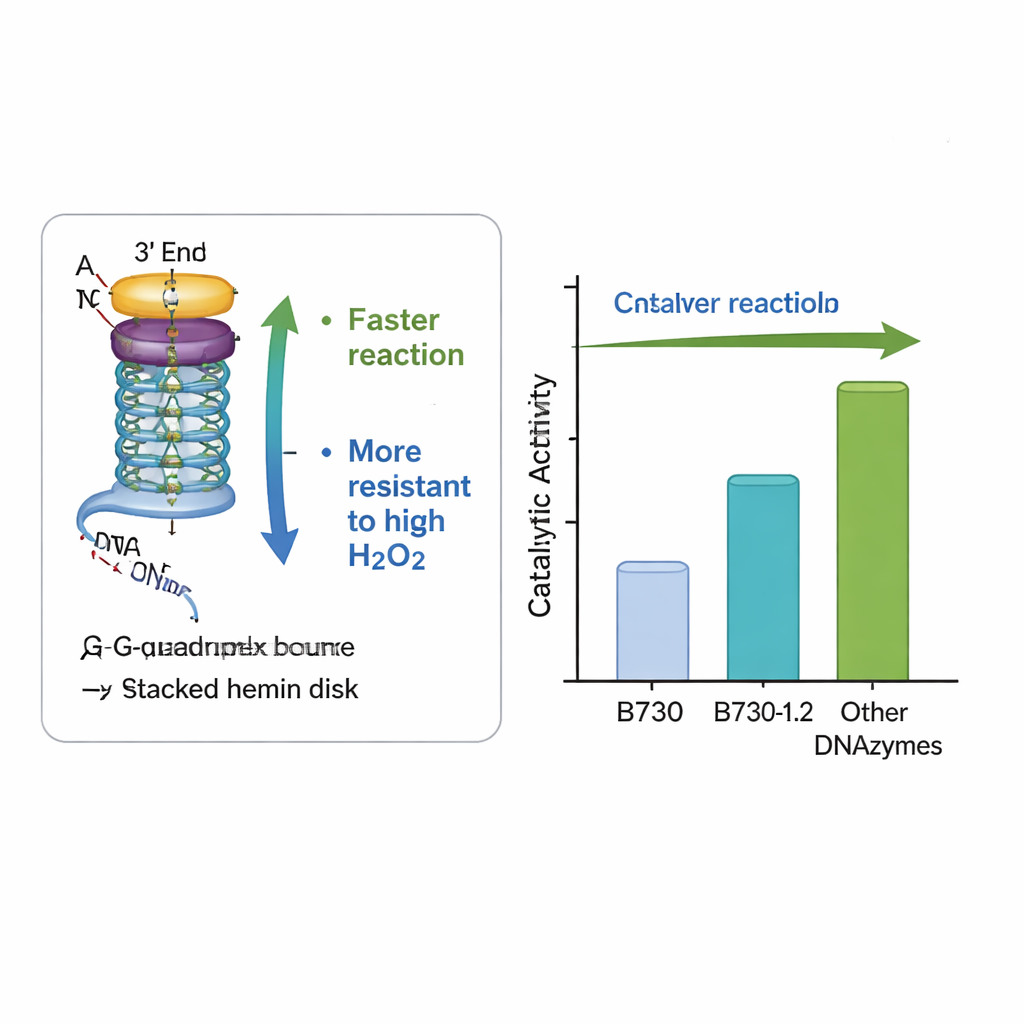
Progettata per resistere a condizioni severe
Un ostacolo pratico importante per perossidasi naturali e artificiali è che alti livelli di perossido di idrogeno, l’ingrediente che guida la reazione, possono distruggere l’enzima e bloccare il processo. La DNAzima riprogettata B730‑1.2 ha mostrato una resilienza notevole: ha mantenuto e persino aumentato la sua attività a livelli di perossido che normalmente inattivano sistemi simili. Misure di assorbimento della luce hanno confermato che il DNA modificato favorisce la formazione dell’intermedio reattivo chiave — il cosiddetto Compound I — più rapidamente, senza alterare la forma complessiva del G‑quadruplex. In altre parole, cambiamenti sottili nelle basi circostanti hanno creato un ambiente locale più favorevole per la chimica, accelerando i passaggi utili e contribuendo a proteggere il centro catalitico dall’autodistruzione.
Cosa significa tutto questo per i sensori futuri
Per un non specialista, il messaggio è semplice: regolando con cura solo poche “lettere” ai lati di una DNAzima già valida, gli autori hanno prodotto una versione che funziona più rapidamente e resiste a condizioni più dure. La loro strategia di modificare le basi flangiate e degli anelli offre una ricetta semplice e a basso costo per costruire catalizzatori a base di DNA più potenti senza ricorrere a complesse modifiche chimiche. Tali DNAzimi robusti ed efficienti potrebbero essere al centro di strisce reattive e dispositivi portatili di nuova generazione che trasformano rapidamente segnali biologici invisibili — come tracce di virus o inquinanti — in cambiamenti di colore facili da leggere.
Citazione: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Parole chiave: DNAzima G-quadruplex, mimetico della perossidasi, biosensori, ingegneria degli aptameri, catalisi del perossido di idrogeno