Clear Sky Science · it
Indagine sugli liquidi ionici a base di Acoramidis come potenziali stabilizzatori della transtiretina mediante calcoli DFT, docking molecolare e studi ADMET
Perché è così difficile realizzare una compressa per una rara malattia cardiaca
L’amiloidosi da transtiretina (ATTR) è una malattia grave in cui una proteina del sangue si accumula nel cuore e nei nervi, danneggiandoli progressivamente. Un nuovo farmaco, Acoramidis, può contribuire a fermare questo accumulo, ma esiste un problema pratico: il farmaco si dissolve poco in acqua, il che rende difficile l’assorbimento quando viene assunto per via orale. Questo studio esplora un modo ingegnoso per riprogettare l’Acoramidis in nuove forme simili a sali, chiamate liquidi ionici, che potrebbero rendere il medicinale più facile da somministrare e più efficace.
Trasformare un farmaco promettente in una forma bevibile
Perché una compressa sia efficace, deve prima sciogliersi nei liquidi acquosi dello stomaco e dell’intestino, quindi attraversare la parete intestinale per entrare nel flusso sanguigno. L’Acoramidis è efficace nel stabilizzare la proteina transtiretina (TTR), contribuendo a prevenire gli aggregati proteici dannosi legati all’ATTR, ma è scarsamente solubile e presenta una bassa biodisponibilità orale. I ricercatori hanno quindi cercato di affrontare il problema abbinando chimicamente l’Acoramidis a diversi partner caricati, creando tre nuove versioni in forma di liquidi ionici (IL1, IL2 e IL3). Queste varianti sono progettate per comportarsi più come sali fluidi che come cristalli rigidi, con il potenziale di aumentare la solubilità del farmaco e la sua diffusione nell’organismo. 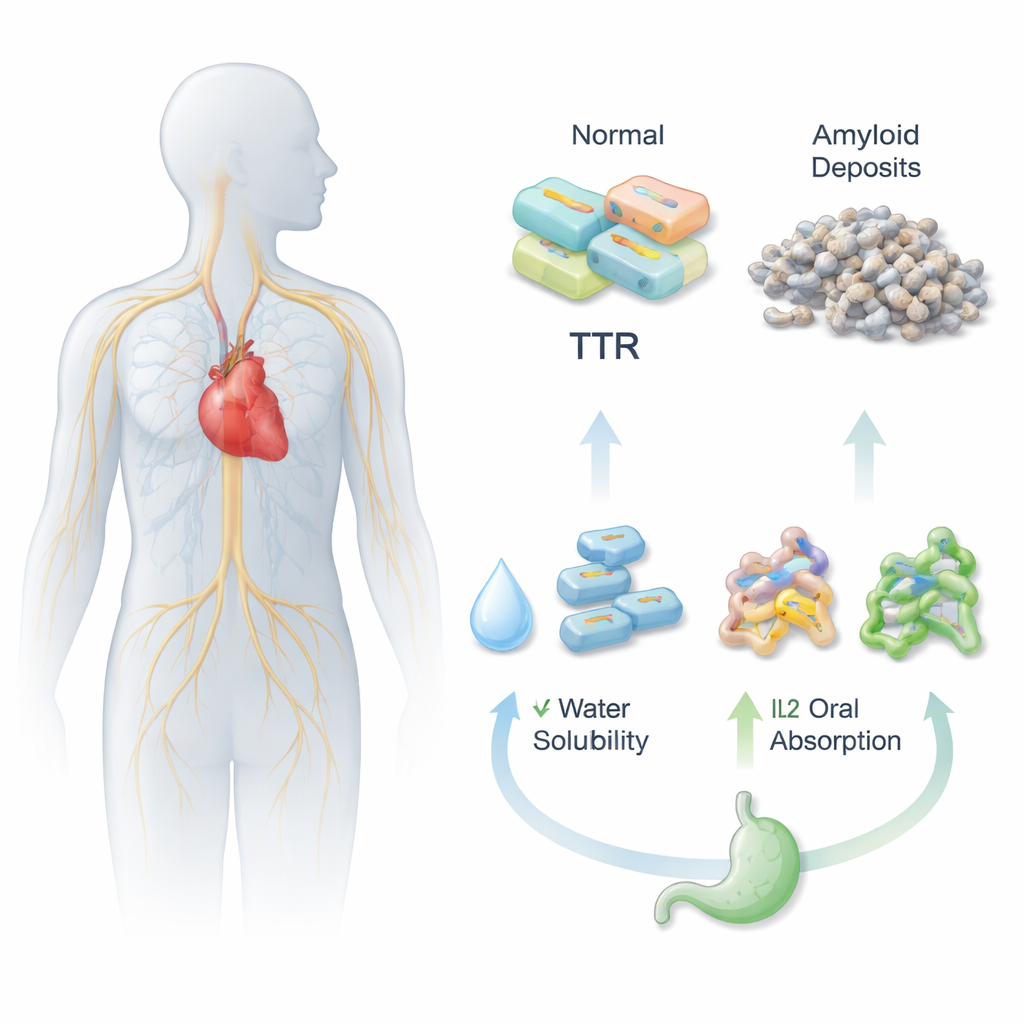
Esaminare le nuove molecole al computer
Invece di passare direttamente ai test su animali o esseri umani, il team ha usato avanzati metodi computazionali per prevedere il comportamento di queste nuove forme. I calcoli di chimica quantistica hanno stimato quanto siano polari le molecole—un indicatore chiave della solubilità in acqua—e quanto facilmente si ridistribuiscano gli elettroni, parametro rilevante per le interazioni con le proteine. IL1 si è distinta per il momento dipolare più elevato e la maggiore reattività elettronica, suggerendo una migliore solubilità in acqua e la capacità di formare contatti più forti e flessibili con i bersagli. I calcoli energetici hanno inoltre indicato che IL1 è termicamente più stabile rispetto al farmaco originale e alle altre due forme ioniche, il che significa che dovrebbe degradarsi meno facilmente prima di raggiungere la sua destinazione.
Quanto saldamente il farmaco può legarsi al suo bersaglio
Successivamente, i ricercatori hanno impiegato il docking molecolare, un test virtuale “chiave-serratura”, per verificare quanto bene l’Acoramidis e le sue tre forme ioniche si adattino al canale di legame della proteina TTR. Tutti e quattro i composti si sono posizionati nella regione corretta della TTR, ma IL1 ha formato l’interazione più salda, con l’energia di legame più favorevole e diversi contatti stabilizzanti—in particolare legami a idrogeno—con aminoacidi chiave della proteina. Questo legame più forte suggerisce che IL1 potrebbe essere ancora più efficace del farmaco padre nel mantenere la TTR nella sua struttura sicura a quattro subunità, contribuendo a prevenire la degradazione e il ripiegamento errato che porta ai depositi amiloidi.
Il corpo assorbirà e eliminerà queste nuove forme?
Infine, il team ha utilizzato strumenti farmacologici online per valutare come l’organismo potrebbe trattare questi composti—quanto si sciolgono, attraversano la parete intestinale, circolano nel sangue e vengono infine eliminati. Tutte e tre le forme ioniche sono state previste come più solubili in acqua rispetto all’Acoramidis, con IL3 che mostra la solubilità grezza più elevata. Le misure di permeabilità intestinale e assorbimento orale complessivo sono migliorate per tutte e tre le forme ioniche, con IL1 e IL2 che offrono il miglior equilibrio tra penetrazione intestinale e biodisponibilità prevista. Anche il legame proteico nel sangue, i tassi di clearance e le emivite sono variati in modi che suggeriscono che le forme in liquido ionico potrebbero garantire un’esposizione più affidabile dopo somministrazione orale, con IL1 che offre nuovamente un profilo particolarmente favorevole. 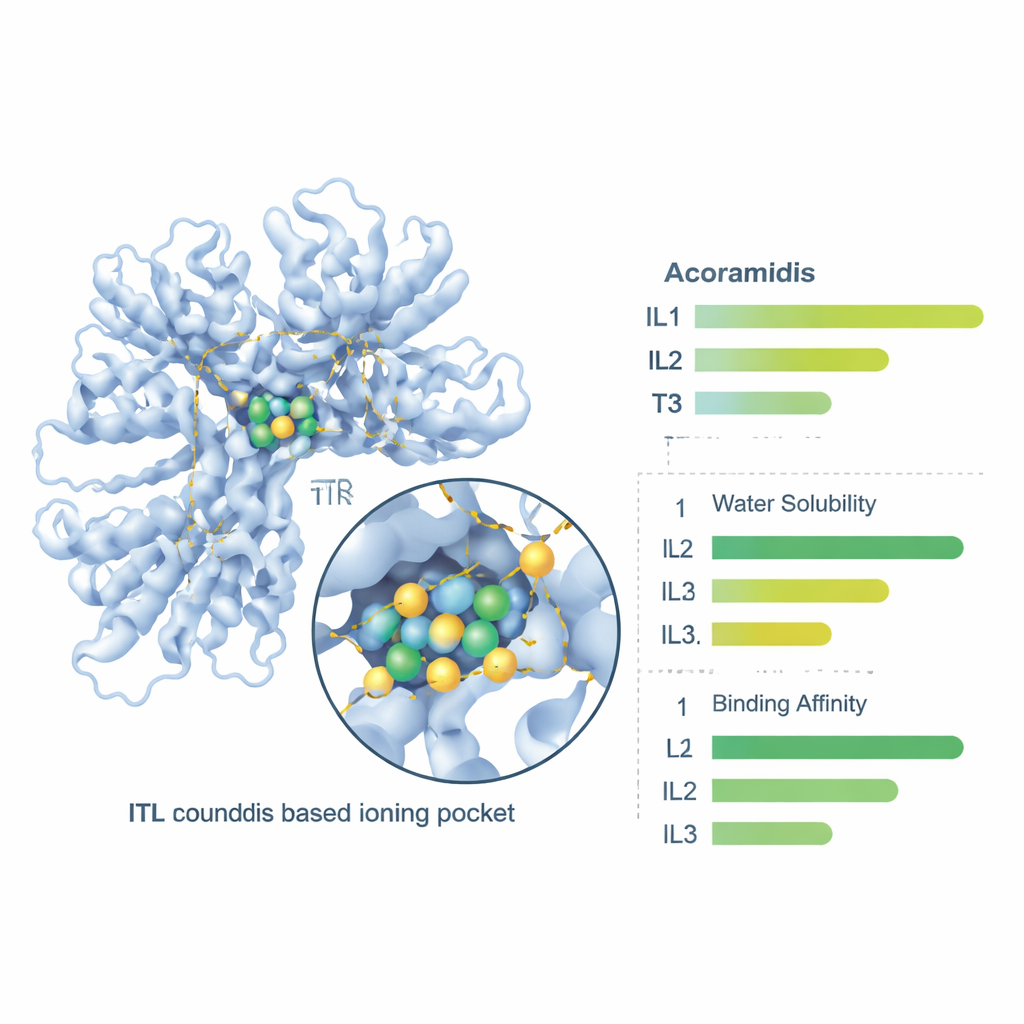
Cosa potrebbe significare per i futuri trattamenti dell’ATTR
Per un non specialista, il messaggio principale è che l’Acoramidis appare già promettente per una malattia cardiaca e nervosa rara ma grave, tuttavia la sua scarsa solubilità limita l’efficacia per somministrazione orale. Trasformando l’Acoramidis in liquidi ionici progettati, questo studio mostra—interamente attraverso test basati su calcoli computazionali—che potrebbe essere possibile ottenere versioni che si dissolvono meglio, si legano più saldamente al loro bersaglio proteico e vengono assorbite in modo più efficiente. Tra i tre candidati, IL1 sembra trovare il miglior equilibrio tra stabilità, forza di legame, solubilità e assorbimento orale previsto, rendendolo un promettente candidato per futuri sviluppi in laboratorio e clinici volti a fornire trattamenti per l’ATTR più efficaci e facili da assumere.
Citazione: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Parole chiave: amiloidosi da transtiretina, Acoramidis, liquidi ionici, ripiegamento proteico scorretto, somministrazione orale di farmaci