Clear Sky Science · it
Progettazione in silico di un vaccino multi-epitopo mirato a DENV-1 e DENV-3
Perché i vaccini contro la dengue sono ancora importanti
La febbre dengue non è più una malattia tropicale rara; oggi minaccia miliardi di persone in oltre 100 paesi e sovraccarica regolarmente gli ospedali in parti dell’Asia, dell’America Latina e oltre. Eppure, anche con due vaccini autorizzati sul mercato, la protezione è disomogenea, specialmente per chi non ha mai avuto la dengue e nelle regioni dove circolano contemporaneamente più sierotipi virali. Questo studio pone una domanda attuale: la progettazione guidata dal computer può aiutarci a costruire un vaccino più sicuro e preciso, pensato specificamente per le co‑infezioni pericolose dovute a due sierotipi della dengue che spesso colpiscono insieme?
Due sierotipi insidiosi e perché sono un problema
Il virus della dengue si presenta in quattro versioni, chiamate sierotipi DENV‑1 fino a DENV‑4. L’infezione da uno qualsiasi può provocare febbre alta, dolori intensi e in alcuni casi emorragie o shock potenzialmente letali. Preoccupante è il fatto che una seconda infezione con un sierotipo diverso può talvolta peggiorare la malattia anziché attenuarla, perché gli anticorpi preesistenti possono facilitare l’ingresso del nuovo virus nelle cellule, un processo chiamato potenziamento dipendente da anticorpi. In recenti focolai, i medici hanno riportato pazienti infettati contemporaneamente da DENV‑1 e DENV‑3, una combinazione associata a malattie più gravi e a risultati diagnostici confusi. I vaccini attuali non proteggono in modo affidabile tutte le fasce d’età e tutti i sierotipi, specialmente le persone senza esposizione precedente, lasciando una pericolosa lacuna nelle difese.
Progettare un vaccino a partire dalla molecola
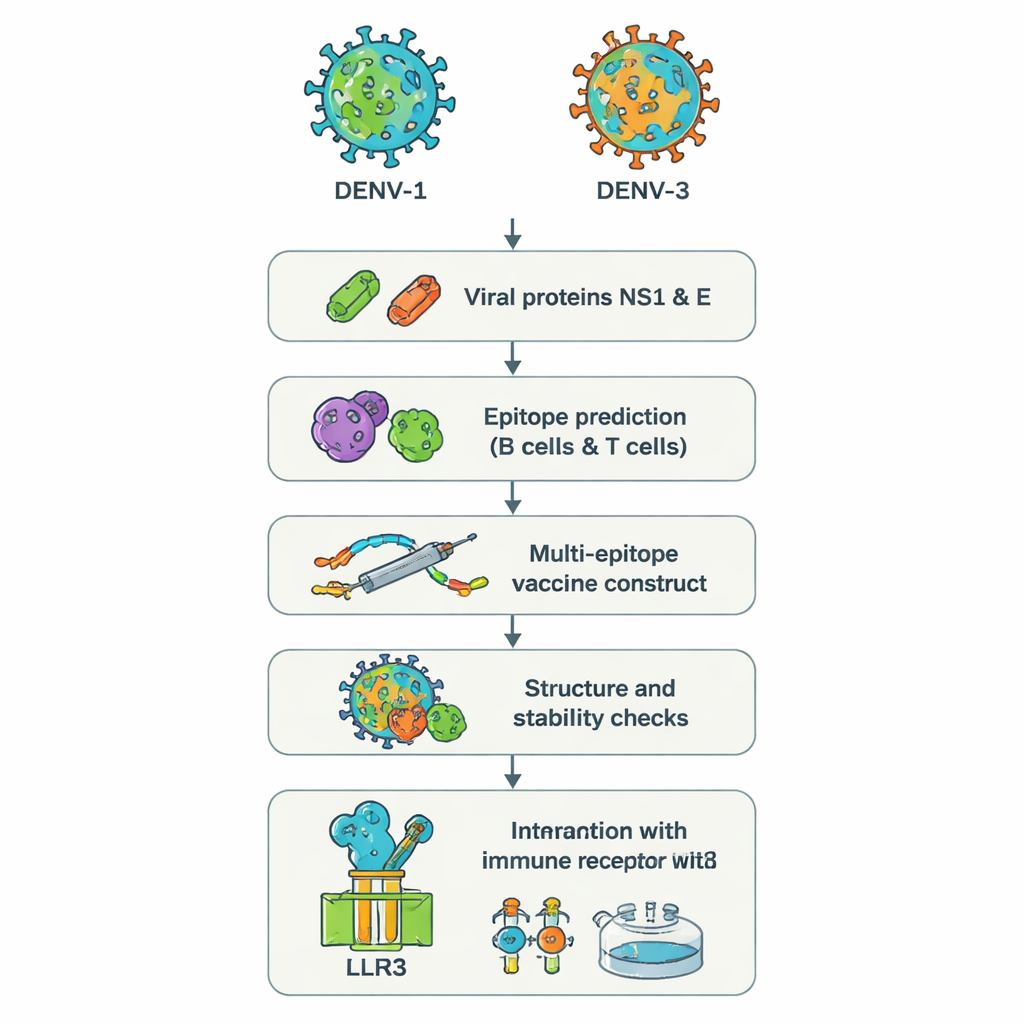
Invece di coltivare virus interi in laboratorio, i ricercatori hanno usato un approccio talvolta chiamato «reverse vaccinology». Sono partiti dalle sequenze genetiche di due proteine della dengue, NS1 ed E, provenienti da DENV‑1 e DENV‑3. Queste proteine sono fondamentali per il modo in cui il virus invade le cellule e per come il sistema immunitario le riconosce. Potenti strumenti web hanno analizzato le sequenze proteiche per individuare brevi segmenti—epitopi—più probabilmente riconosciuti dalle cellule B umane (che producono anticorpi) e dalle cellule T (che uccidono le cellule infette e coordinano le risposte). Da centinaia di candidati, il gruppo ha selezionato un piccolo insieme previsto come altamente visibile al sistema immunitario, condiviso tra i due sierotipi e capace di indurre segnali antivirali utili come l’interferone‑gamma.
Costruire una singola molecola vaccinale multiuso
Gli epitopi scelti sono stati quindi cuciti digitalmente insieme in un’unica lunga proteina artificiale, un vaccino «multi‑epitopo». Brevi linker di amminoacidi fungono da spaziatori flessibili in modo che ogni epitopo mantenga la propria struttura e resti accessibile alle cellule immunitarie. Un pezzo aggiuntivo, basato su un peptide antimicrobico umano naturale chiamato beta‑defensina, è stato inserito come adiuvante per potenziare la risposta complessiva. L’analisi al computer ha previsto che il costrutto finale, contenente 575 amminoacidi, sarebbe stabile, idrofilo (e quindi più facile da solubilizzare) e improbabile che agisca da allergene. Ulteriori strumenti di predizione strutturale hanno generato un modello tridimensionale e verificato che la maggior parte dei mattoni costitutivi si trovasse in posizioni realistiche, simili a quelle osservate in strutture proteiche note.
Testare il candidato dentro un corpo virtuale
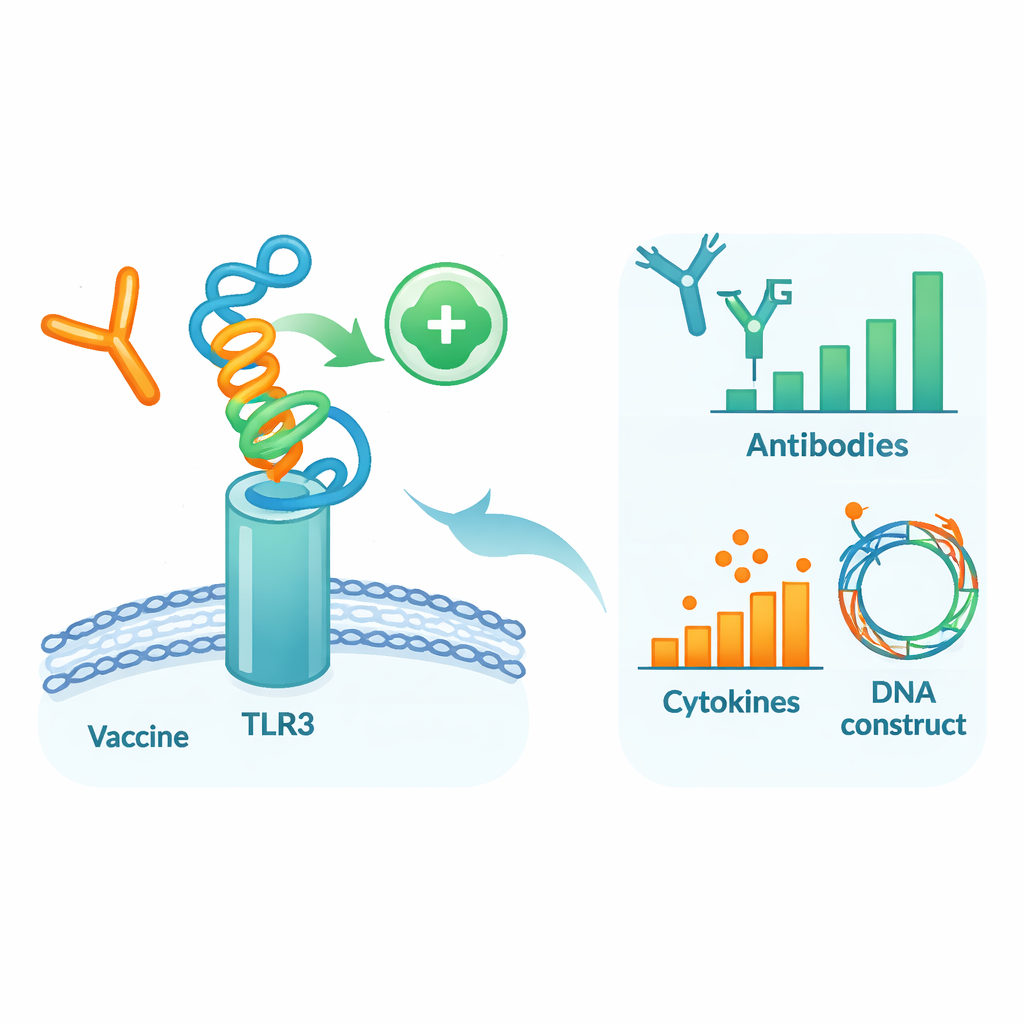
Per valutare come questa proteina progettata potesse comportarsi in un contesto simile a quello umano, gli autori hanno eseguito una serie di simulazioni informatiche dettagliate. Prima hanno dockato il modello del vaccino su TLR3, una proteina sensore sulle cellule immunitarie che rileva materiale virale e contribuisce a lanciare le difese precoci. Simulazioni di dinamica molecolare—filmati virtuali degli atomi in movimento—hanno suggerito che il vaccino e TLR3 formano un complesso stabile, supportato da energie di legame favorevoli e numerosi legami idrogeno. Analisi aggiuntive di movimento ed energia hanno indicato regioni specifiche di entrambe le molecole che agiscono come “punti caldi” di contatto. Successivamente, è stato utilizzato un simulatore del sistema immunitario per imitare tre dosi di vaccino distribuite su diversi mesi. Il sistema immunitario virtuale ha prodotto forti ondate di anticorpi IgG protettivi, memoria a lungo termine di cellule B e T, e molecole di segnalazione coerenti con una robusta risposta antivirale.
Dal modello al progetto pronto per il laboratorio
Infine, i ricercatori hanno adattato il codice genetico del vaccino per una produzione efficiente in comuni microrganismi da laboratorio e hanno inserito con successo questa sequenza di DNA ottimizzata in un plasmide di espressione standard, pronto per futuri test sperimentali. In termini semplici, il loro lavoro fornisce un progetto dettagliato per un nuovo vaccino contro la dengue che prende di mira pezzi selezionati di DENV‑1 e DENV‑3, è previsto essere stabile e sicuro, e dovrebbe coinvolgere fortemente entrambi i rami del sistema immunitario. Pur essendo questi risultati puramente computazionali e dovendo essere confermati in cellule, animali e infine nell’uomo, mostrano come la bioinformatica moderna possa generare rapidamente candidati vaccinali su misura per problemi complessi come la co‑infezione da dengue.
Citazione: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Parole chiave: vaccino per dengue, multi-epitopo, DENV-1, DENV-3, immunoinformatica