Clear Sky Science · it
Analisi integrativa di proteomica e metabolomica rivela un disordine del metabolismo degli aminoacidi nelle cellule di leucemia mieloide acuta resistenti all’adriamicina
Perché alcuni farmaci per la leucemia smettono di funzionare
La chemioterapia ha trasformato il trattamento della leucemia mieloide acuta (LMA), un tumore del sangue a rapida crescita. Eppure molti pazienti vedono la malattia ritornare perché le cellule tumorali imparano a sopravvivere ai farmaci pensati per ucciderle. Questo studio pone una domanda semplice ma cruciale: cosa cambia all’interno delle cellule leucemiche quando diventano resistenti all’adriamicina, uno dei farmaci chemioterapici di riferimento, e tali cambiamenti potrebbero indicare nuove vie per ripristinare l’efficacia del farmaco?
Uno sguardo dentro le cellule leucemiche
Per indagare, i ricercatori hanno confrontato una linea cellulare umana comune di LMA, chiamata HL60, con una linea sorella resa resistente all’adriamicina (HL60/R). Piuttosto che analizzare un singolo gene o una singola proteina alla volta, hanno impiegato due approcci ampi e complementari. La proteomica ha misurato migliaia di proteine diverse — le molecole che svolgono la maggior parte delle attività cellulari. La metabolomica ha misurato centinaia di piccole molecole che costituiscono il metabolismo cellulare, inclusi lipidi, zuccheri e aminoacidi. Combinando questi strati “omici”, il team ha costruito un quadro dettagliato di come le cellule resistenti differiscano dalle loro controparti ancora sensibili.
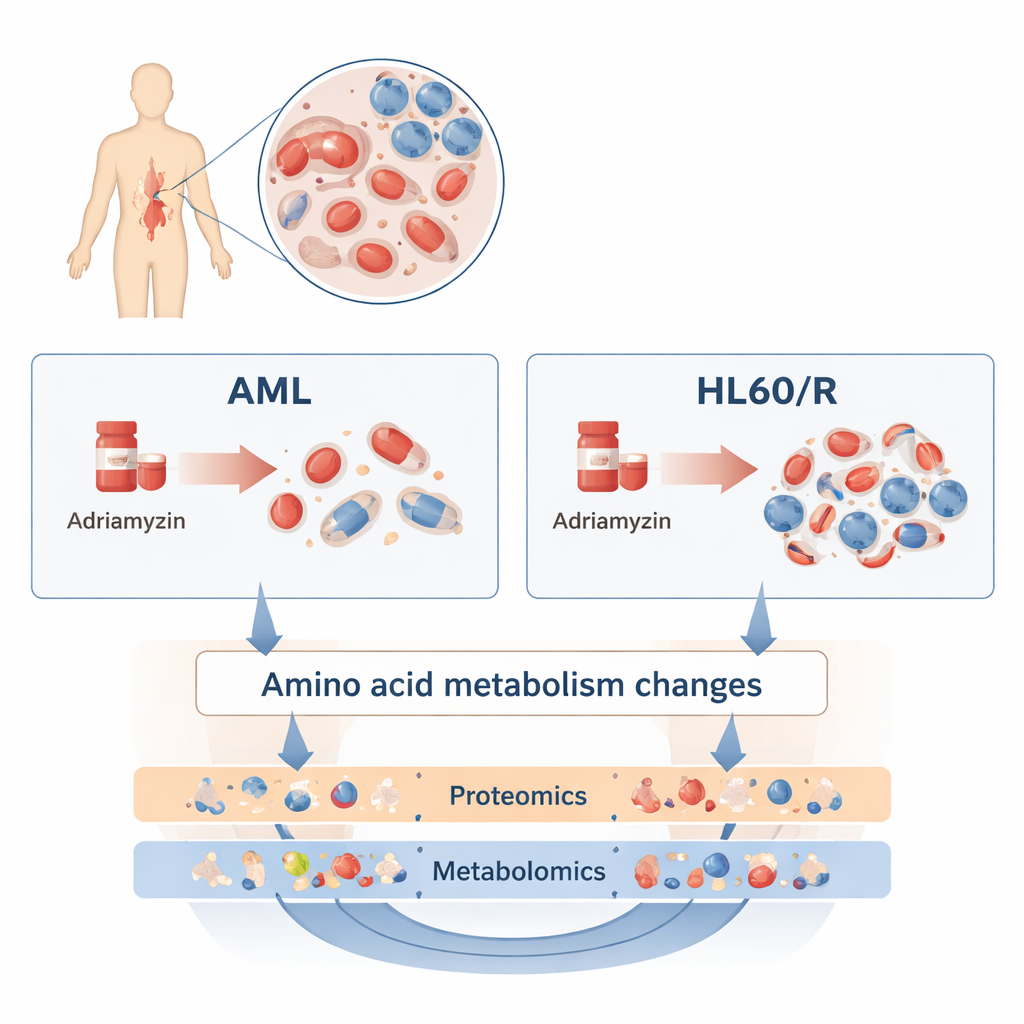
Rimodellamento massiccio dei meccanismi cellulari
Il sondaggio proteomico ha rivelato cambiamenti profondi: oltre 3.200 proteine erano presenti a livelli più alti o più bassi nelle cellule resistenti all’adriamicina rispetto alle cellule HL60 normali. Molte di queste proteine si raggruppavano in percorsi che controllano come le cellule utilizzano l’energia e rispondono allo stress. In particolare sono risultati alterati componenti della via di segnalazione del cAMP, della via HIF‑1 (che aiuta le cellule a far fronte alla bassa ossigenazione) e della fosforilazione ossidativa (un processo produttore di energia nei mitocondri). Questi spostamenti suggeriscono che le cellule leucemiche resistenti riprogrammano il loro modo di respirare, crescere e comunicare fra loro per resistere alla chemioterapia.
Il metabolismo si sposta verso gli aminoacidi
L’analisi metabolomica ha raccontato una storia complementare. Su circa 1.400 metaboliti rilevati, 260 sono cambiati in modo significativo nelle cellule resistenti. Modelli statistici hanno separato nettamente le cellule resistenti da quelle non resistenti, indicando una firma metabolica coerente di resistenza. Quando i metaboliti alterati sono stati mappati sui percorsi biochimici noti, sono emersi diversi percorsi rilevanti. Molti dei percorsi maggiormente coinvolti erano legati agli aminoacidi, i mattoni delle proteine — in particolare quelli che coinvolgono alanina, aspartato, glutammato, cisteina, metionina e glutatione. Altri network, come il metabolismo delle purine e delle pirimidine (importanti per DNA e RNA) e la gestione di alcuni lipidi, risultavano anch’essi perturbati, sottolineando che la resistenza è associata a un ampio rimodellamento metabolico.
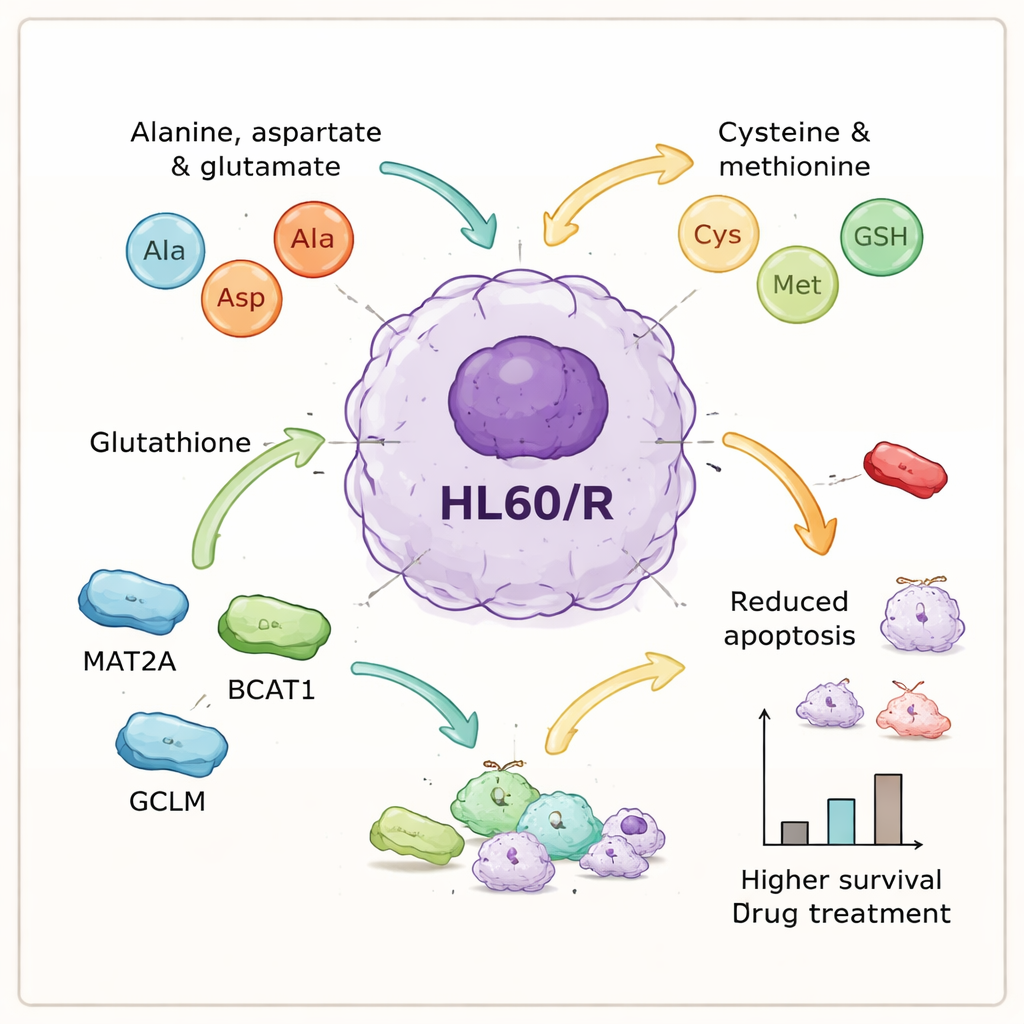
Attori molecolari chiave che aiutano le cellule tumorali a sopravvivere
Integrando i dati proteici e metabolici, gli autori si sono concentrati su un insieme di processi legati agli aminoacidi che sembravano centrali per la resistenza. Hanno selezionato sei proteine connesse a questi percorsi — GOT1, GPX1, AHCY, MAT2A, BCAT1 e GCLM — per un’analisi più approfondita. Test di laboratorio hanno confermato che cinque di queste erano più abbondanti nelle cellule resistenti, coerente con l’idea che l’elaborazione degli aminoacidi sia potenziata, mentre una enzima antiossidante, GPX1, risultava ridotta. Per indagare causalità, il team ha usato piccoli RNA interferenti per ridurre l’espressione di tre delle proteine sovraregolate — MAT2A, BCAT1 e GCLM — nelle cellule resistenti. Quando queste proteine sono state silenziate, le cellule hanno mostrato un aumento significativo dell’apoptosi dopo il trattamento, perdendo gran parte della loro protezione acquisita contro l’adriamicina.
Cosa significa per i trattamenti futuri
Nel complesso, questi risultati suggeriscono che le cellule di LMA resistenti all’adriamicina sopravvivono non solo per singole mutazioni, ma perché rimodellano la loro chimica interna, con il metabolismo degli aminoacidi come fulcro centrale. Dirottando risorse verso specifici percorsi degli aminoacidi e del glutatione, le cellule sembrano meglio in grado di gestire lo stress, riparare i danni ed evitare la morte quando esposte alla chemioterapia. Per i non specialisti, il messaggio chiave è che la resistenza non è casuale: segue schemi identificabili che possono essere misurati e, potenzialmente, bersagliati. A lungo termine, farmaci che interferiscono con proteine specifiche del metabolismo degli aminoacidi come MAT2A, BCAT1 o GCLM potrebbero essere associati all’adriamicina o a agenti simili, offrendo ai clinici nuovi strumenti per prevenire o superare la resistenza nei pazienti con leucemia mieloide acuta.
Citazione: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Parole chiave: leucemia mieloide acuta, resistenza ai farmaci, adriamicina, metabolismo degli aminoacidi, multi-omiche