Clear Sky Science · it
Un modello cellulare funzionale e robusto per lo screening ad alto rendimento dei modulatori di piezo1
Perché i piccoli sensori di pressione nelle nostre cellule sono importanti
Ogni volta che il sangue scorre nei nostri vasi oppure semplicemente quando camminiamo in una stanza, le nostre cellule avvertono piccole forze meccaniche. Una proteina chiave, un vero e proprio "sensore di pressione" chiamato Piezo1, aiuta le cellule a tradurre queste forze in segnali elettrici e chimici che mantengono i tessuti sani. Poiché Piezo1 è coinvolto nella crescita dei vasi sanguigni, nella robustezza delle ossa, nell’immunità e in alcune malattie genetiche rare, gli sviluppatori di farmaci sono interessati a trovare molecole in grado di modulare la sua attività. L’articolo qui descritto presenta un nuovo modo, più rapido, per cercare tali molecole usando cellule ingegnerizzate e letture basate sulla luce invece di tecniche lente e laboriose.
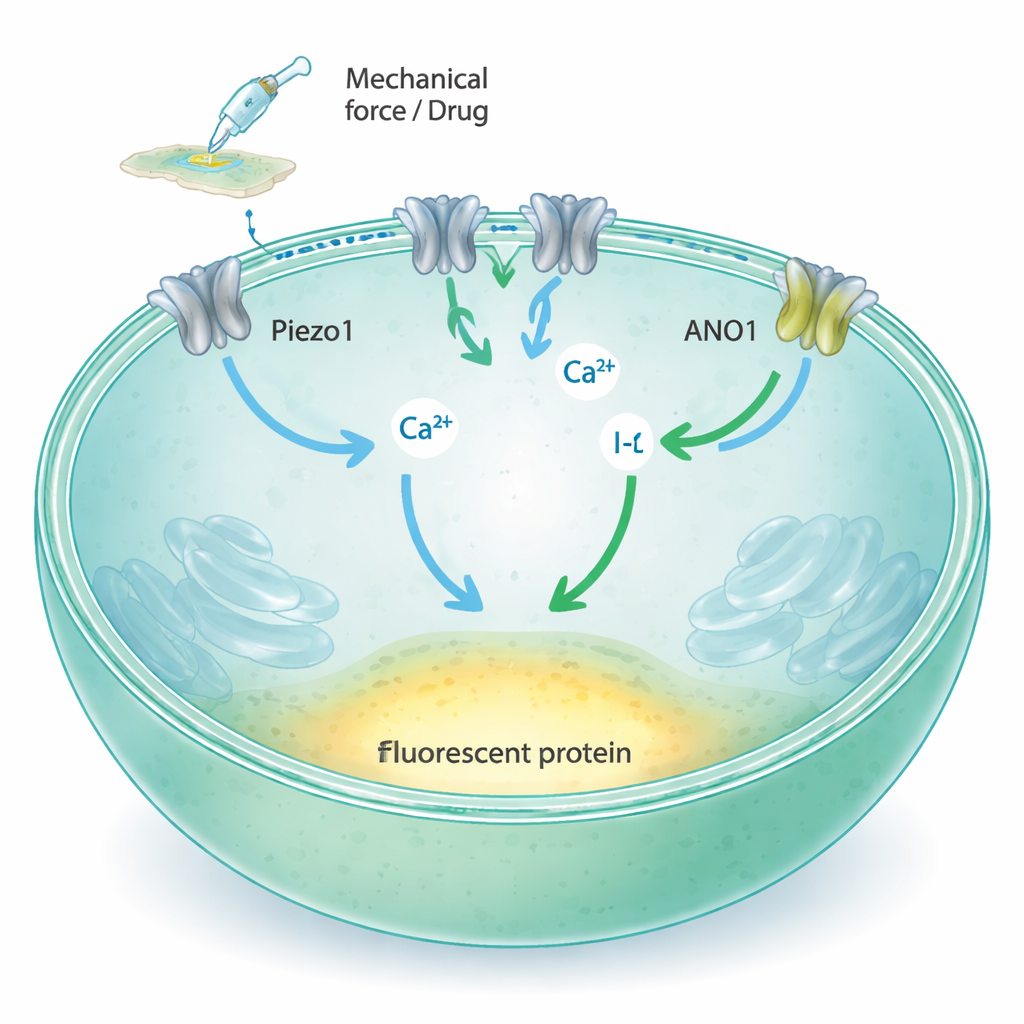
Convertire il tatto in un segnale luminoso
Piezo1 è un canale nella membrana cellulare che si apre quando la membrana viene allungata o spinta, permettendo al calcio e ad altri ioni carichi di entrare nella cellula. I metodi tradizionali per studiare questi canali si basano su sottili elettrodi di vetro o su sonde fluorescenti specializzate, strumenti potenti ma difficili da estendere alle decine di migliaia di test necessari per la moderna scoperta di farmaci. Gli autori hanno voluto convertire l’attività di Piezo1 in un semplice cambiamento di luce che un lettore di piastre può misurare rapidamente su molteplici campioni contemporaneamente. L’idea è stata collegare Piezo1 a due componenti aggiuntivi: ANO1, un altro canale ionico che risponde al calcio, e una proteina fluorescente gialla modificata che perde brillantezza quando esposta a ioni ioduro.
Costruire una cellula test reattiva
I ricercatori hanno iniziato con cellule Fischer Rat Thyroid (FRT), che producono naturalmente Piezo1 e aderiscono bene alle piastre di plastica standard. Hanno confermato che queste cellule esprimono Piezo1 ma non il suo stretto parente Piezo2, e hanno mostrato che Piezo1 in queste cellule risponde al flusso di fluido e alla stimolazione meccanica facendo entrare calcio. Successivamente hanno introdotto il canale ANO1 e la proteina fluorescente sensibile all’ioduro (YFP‑H148Q/I152L) nelle cellule. Quando il calcio aumenta all’interno della cellula, ANO1 si apre e permette l’ingresso di ioduro; la proteina fluorescente quindi si affievolisce man mano che lo ioduro si accumula attorno a essa. Microscopia, citometria a flusso e registrazioni elettriche hanno mostrato che sia ANO1 sia il sensore fluorescente erano presenti ad alti livelli e funzionavano come previsto.
Dall’azione del farmaco a un bagliore misurabile
Con questo sistema a tre componenti, il gruppo ha creato una semplice catena di causa‑effetto: se una molecola in prova attiva Piezo1, il calcio entra, ANO1 si apre, lo ioduro irrompe e il segnale di fluorescenza diminuisce; se una molecola blocca Piezo1, il segnale resta brillante. Hanno validato questa logica usando attivatori noti di Piezo1 (Yoda1, Jedi1, Jedi2) e inibitori (Ruthenium Red, GsMTx4). Gli attivatori hanno prodotto diminuzioni di fluorescenza dipendenti dalla dose, con valori di sensibilità in linea con i dati precedentemente riportati. Gli inibitori hanno mostrato l’andamento opposto, riducendo la risposta all’aumentare della concentrazione. Il saggio ha funzionato solo quando sia il calcio sia lo ioduro erano presenti, sottolineando che il segnale dipendeva realmente dall’ingresso di calcio guidato da Piezo1 e dal successivo afflusso di ioduro mediato da ANO1. Misure statistiche come il fattore Z e il rapporto segnale‑rumore indicano che il metodo è sufficientemente stabile e affidabile per lo screening su scala industriale.
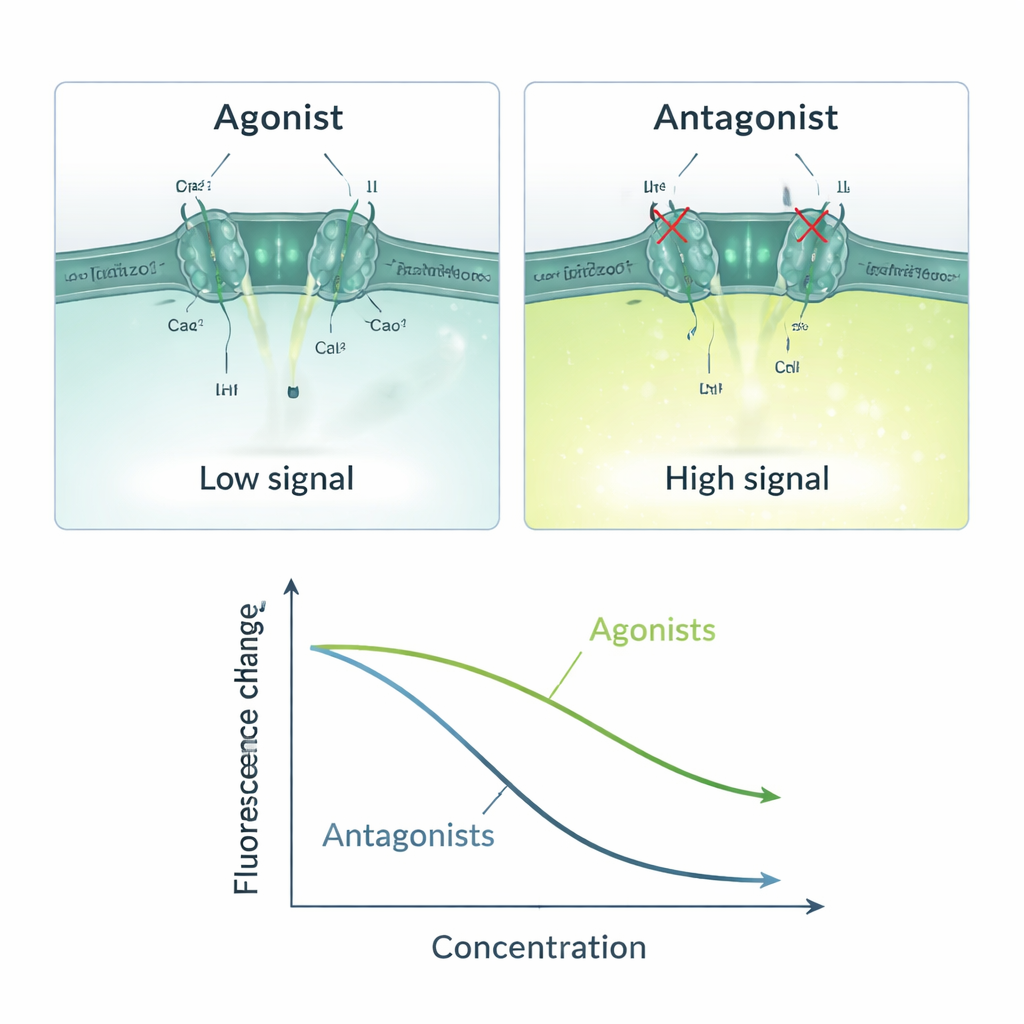
Test rapidi e scalabili con alcune avvertenze
Il nuovo modello cellulare può eseguire la misura di un singolo pozzetto in circa 14 secondi e scansionare una piastra a 96 pozzetti in circa 22 minuti, e può essere adattato a strumenti che leggono centinaia di pozzetti simultaneamente. Le cellule ingegnerizzate rimangono stabili per molte generazioni sotto selezione antibiotica, permettendo esperimenti ripetuti nel tempo. Poiché la lettura è ottica e usa apparecchiature per micropiastre standard, l’approccio è relativamente a basso costo e accessibile. Tuttavia, gli autori osservano che il test è indiretto: qualsiasi composto che agisca su passaggi anteriori o successivi a Piezo1 nella catena di segnalazione — come ANO1 stesso o altre proteine che gestiscono il calcio — può produrre un falso positivo. Per questo motivo, i composti selezionati in questo screening necessitano comunque di conferma con metodi più diretti come l’elettrofisiologia.
Cosa significa per i trattamenti futuri
In termini pratici, i ricercatori hanno costruito un vero e proprio "rilevatore di fumo" di laboratorio che si attenua ogni volta che una sostanza fa aprire Piezo1 e resta luminoso quando Piezo1 è bloccato. Questo allarme è sensibile, veloce e facile da eseguire in grandi quantità, rendendolo adatto al primo passaggio nella ricerca di farmaci che modulano i sensori meccanici del corpo. Sebbene non sostituirà i test di follow‑up più dettagliati, questo modello cellulare fornisce un punto di partenza potente per la scoperta di molecole che potrebbero un giorno aiutare a trattare disturbi vascolari, malattie ossee, problemi immunitari e altre condizioni legate al modo in cui le nostre cellule avvertono e rispondono alle forze fisiche.
Citazione: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Parole chiave: Canale Piezo1, canali ionici meccanosensibili, screening ad alto rendimento, saggio su cellule, scoperta di farmaci