Clear Sky Science · it
Effetti radiosensibilizzanti delle nanoparticelle d'argento mirate all'angiogenesi e alla segnalazione delle metalloproteinasi della matrice in linee cellulari di carcinoma mammario triplo negativo
Rendere più vulnerabili i tumori mammari più difficili
Il carcinoma mammario triplo negativo è una delle forme più difficili da trattare. Tende a crescere rapidamente, a diffondersi precocemente e manca dei soliti “manici” molecolari a cui si legano molti farmaci moderni. La radioterapia è spesso parte del trattamento, ma questi tumori possono essere ostinatamente resistenti. Questo studio pone una domanda semplice e stimolante: particelle d'argento microscopiche possono rendere la radioterapia più efficace, rallentando al contempo la capacità del tumore di formare nuovi vasi sanguigni e di diffondersi?
Piccoli aiutanti d'argento per la radioterapia
I ricercatori si sono concentrati sulle nanoparticelle d'argento — sfere ultra-piccole d'argento misurate in miliardesimi di metro. Poiché l'argento è denso e interagisce fortemente con i raggi X, queste particelle possono concentrare gli effetti della radiazione proprio dove si accumulano. Il gruppo ha lavorato con due modelli di laboratorio ampiamente usati per il carcinoma mammario triplo negativo, confrontandoli con una linea cellulare mammaria non cancerosa. Hanno prima testato quanto le nanoparticelle d'argento fossero tossiche da sole e hanno scoperto che le cellule tumorali venivano uccise a dosi molto più basse rispetto alle cellule normali, suggerendo una finestra terapeutica utile. Utilizzando metodi matematici per analizzare l'interazione tra particelle e radiazione, hanno dimostrato che la combinazione dei due produceva un effetto di uccisione delle cellule decisamente più forte rispetto a ciascun trattamento singolarmente.
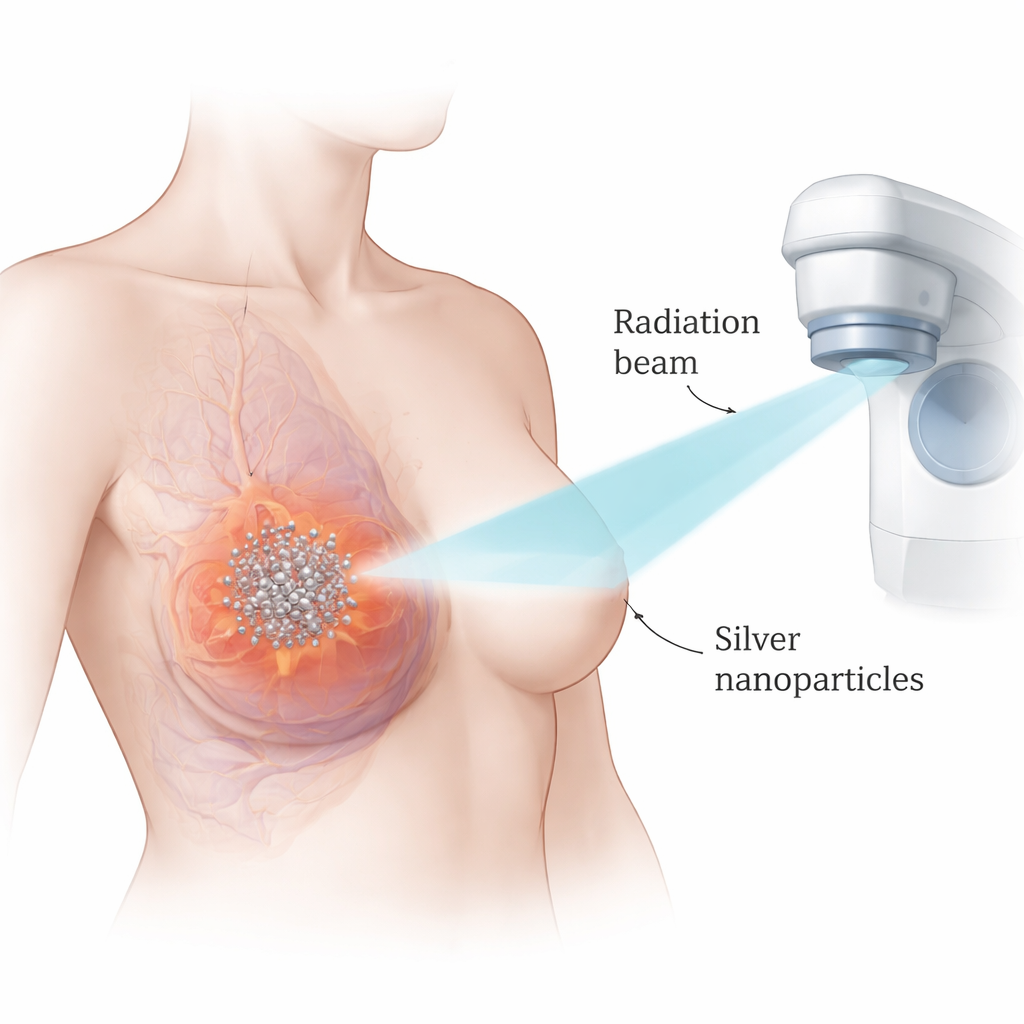
Spingere le cellule tumorali all'autodistruzione
Successivamente, gli scienziati hanno esaminato come il trattamento combinato uccidesse le cellule. Hanno misurato l'apoptosi, una forma di suicidio cellulare programmato, e monitorato l'accumulo di molecole altamente reattive note come specie reattive dell'ossigeno, o ROS. È già noto che la radiazione agisce in parte generando ROS che danneggiano il DNA. In entrambe le linee cellulari di carcinoma triplo negativo, le nanoparticelle d'argento da sole aumentavano apoptosi e livelli di ROS, e lo stesso faceva la radiazione — ma l'uso combinato spingeva entrambe le misure in modo drammatico. Ciò significa che un maggior numero di cellule tumorali veniva indirizzato verso una modalità ordinata di autodistruzione, anziché rimanere in uno stato danneggiato che a volte può favorire recidive o resistenza.
Interrompere l'apporto di sangue e rallentare la diffusione
I tumori dipendono dai vasi sanguigni per ricevere ossigeno e nutrienti, e i tumori aggressivi possono perfino imitare i vasi sanguigni stessi. Il team ha esaminato due interruttori molecolari chiave coinvolti nella costruzione e stabilizzazione dei vasi tumorali, chiamati VEGFR2 e Tie2. In entrambe le linee cellulari, le nanoparticelle d'argento riducevano l'attività di questi geni, e la combinazione con la radiazione li sopprimeva ancora di più. Hanno anche esaminato due enzimi, MMP-2 e MMP-9, che aiutano le cellule tumorali a degradare il tessuto circostante e a migrare. In uno dei modelli cellulari, sia la radiazione sia le nanoparticelle d'argento abbassavano questi enzimi, mentre il trattamento combinato aveva l'effetto più marcato. Quando gli scienziati hanno osservato lo spostamento delle cellule tumorali in un “graffio” artificiale in una piastra e quando hanno testato la formazione di strutture simili a vasi sanguigni in un sistema di co-coltura, il trattamento combinato rallentava più chiaramente migrazione e formazione di tubi.
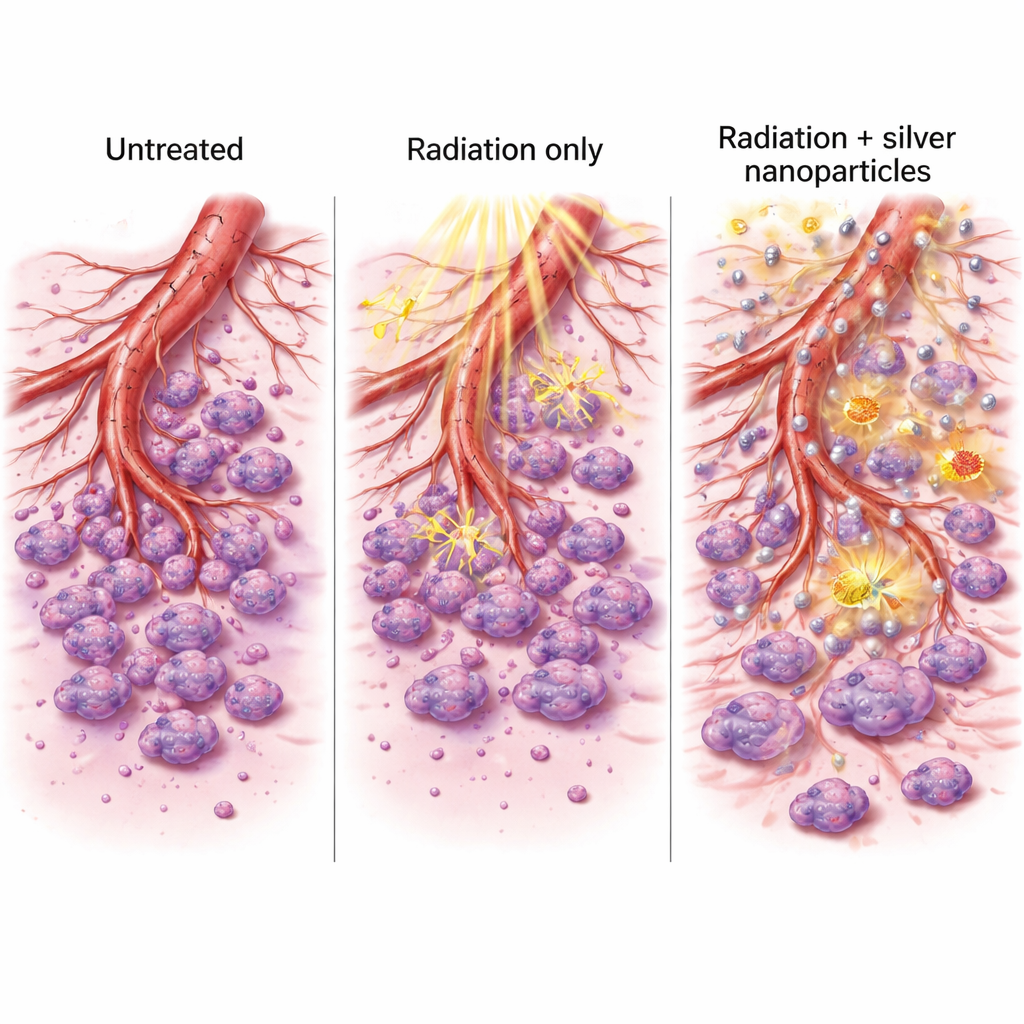
Perché questi cambiamenti sono importanti
Riducendo l'espressione di geni che promuovono la crescita di nuovi vasi e di enzimi che facilitano l'invasione, la combinazione argento-più-radiazione ha fatto più che uccidere le cellule tumorali. Ha inoltre disturbato i sistemi di supporto che i tumori utilizzano per espandersi e diffondersi. Le cellule trattate erano meno capaci di richiudere ferite in piastre di laboratorio e meno in grado di organizzarsi in reti ramificate che ricordano i vasi sanguigni precoci. Insieme al marcato aumento della morte cellulare e della produzione di ROS, questi effetti suggeriscono un duplice vantaggio: un attacco diretto più potente sul tumore e strumenti indeboliti per la crescita futura e le metastasi.
Cosa potrebbe significare per i pazienti
Per ora, questi risultati provengono da cellule tumorali coltivate in laboratorio, non da pazienti. Tuttavia, dipingono un quadro promettente. Le nanoparticelle d'argento hanno agito da radiosensibilizzatori, rendendo la radioterapia standard più potente contro le cellule di carcinoma mammario triplo negativo. Allo stesso tempo, sembravano soffocare la capacità del tumore di costruire linee di approvvigionamento sanguigno e di invadere i tessuti circostanti. Se studi futuri su animali e trial clinici confermeranno che queste particelle possono essere somministrate in modo sicuro e selettivo ai tumori, potrebbero aiutare i medici a usare dosi di radiazione più basse ottenendo risultati migliori, offrendo un nuovo modo per affrontare una delle forme più impegnative di cancro al seno.
Citazione: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Parole chiave: carcinoma mammario triplo negativo, nanoparticelle d'argento, radioterapia, angiogenesi, metastasi