Clear Sky Science · it
Risposta chemosensoriale ai chemioterapici a base di Pt tramite i recettori del gusto amaro in vitro rivela un nuovo meccanismo per i disturbi del gusto amaro
Perché i farmaci oncologici possono improvvisamente far risultare tutto disgustoso
I pazienti oncologici riferiscono spesso che il cibo inizia ad avere un sapore stranamente amaro o metallico poco dopo l’inizio della chemioterapia. Questo non si limita a rovinare i pasti: può ridurre l’appetito, favorire la perdita di peso e intaccare la qualità della vita proprio quando i pazienti hanno più bisogno di forza. Questo studio pone una domanda apparentemente semplice ma dalle grandi conseguenze pratiche: come interferiscono esattamente i comuni farmaci chemioterapici a base di platino con il nostro senso del gusto, e si può attenuare in modo sicuro questo effetto senza indebolire il trattamento?
Il ruolo nascosto dei “sensori dell’amaro” in bocca e nell’intestino
La lingua e il tratto digestivo sono punteggiati di recettori per il gusto amaro, progettati per avvertirci di sostanze potenzialmente dannose. Questi sensori, noti come TAS2R, non si limitano alle papille gustative; si trovano anche nelle cellule dello stomaco. I ricercatori hanno usato una linea cellulare gastrica umana (HGT-1) che funziona come un rilevatore di amarezza in vitro: quando i recettori amari vengono attivati, le cellule espellono più protoni (acido), misurabili come variazione di un parametro chiamato indice protonico intracellulare. Esponendo queste cellule a due farmaci antitumorali a base di platino ampiamente usati — carboplatino e cisplatino — il team ha potuto sondare in sicurezza quanto questi farmaci appaiano “amari” alle cellule umane senza mai chiedere a una persona di assaggiare un composto tossico. 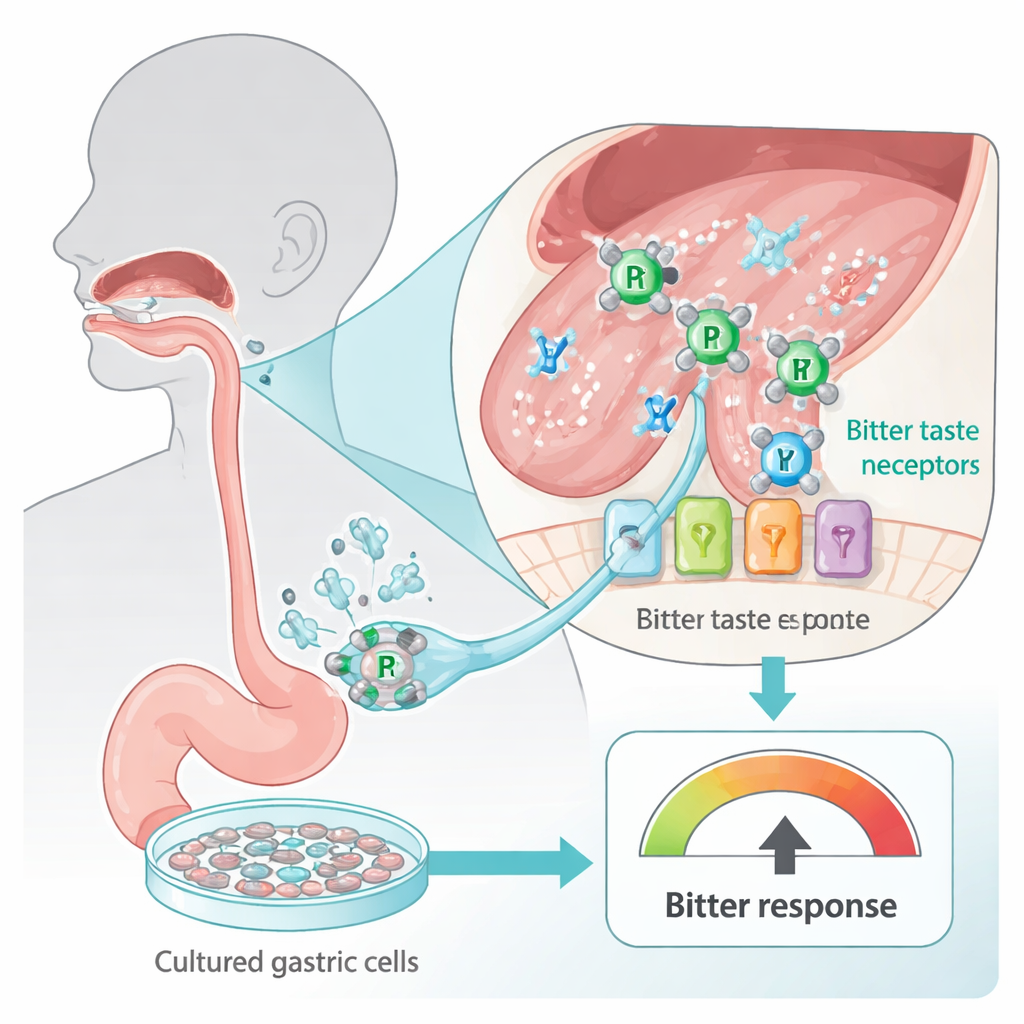
Farmaci chemioterapici che risultano amari per le cellule
Quando le cellule gastriche sono state trattate con concentrazioni clinicamente rilevanti di carboplatino e cisplatino, entrambi i farmaci hanno innescato una chiara risposta di tipo amaro dipendente dalla dose: più alta è la dose, più forte è la reazione cellulare. Il cisplatino, tuttavia, ha prodotto una risposta più intensa rispetto al carboplatino se si considera il loro rapporto di dose terapeutica abituale (circa 1:4), suggerendo che potrebbe contribuire in misura maggiore ai problemi di sapore amaro nei pazienti. A livello genetico, l’esposizione a questi farmaci ha modificato l’attività di diversi geni dei recettori dell’amaro nelle cellule, indicando che i composti a base di platino non agiscono su un unico “interruttore dell’amaro” ma rimodellano ampiamente il sistema di rilevazione dell’amaro. Tra questi recettori, TAS2R4 e TAS2R5 si sono distinti per essere sia altamente attivi sia fortemente influenzati dal trattamento.
Spegnere i segnali dell’amaro e testare un bloccante amaro naturale
Per identificare quali recettori sono più importanti, il team ha disattivato selettivamente recettori amari specifici. L’abbattimento di TAS2R4 o la riduzione di TAS2R5 hanno ciascuno ridotto la risposta di tipo amaro a carboplatino e cisplatino, confermando che questi recettori contribuiscono a percepire i farmaci. Gli scienziati hanno poi testato una contromisura promettente: il sale sodico dell’homoeriodictyol (Na‑HED), una flavanone isolata originariamente dalla pianta nordamericana Herba Santa e già nota per mascherare l’amaro di altri composti. Quando Na‑HED è stato aggiunto insieme ai farmaci a base di platino, ha attenuato nettamente la risposta cellulare amara — di circa tre quarti sia per il carboplatino sia per il cisplatino — senza danneggiare le cellule da solo. Questo mostra che Na‑HED può agire direttamente sui recettori dell’amaro per smorzare il segnale scatenato dai farmaci chemioterapici.
Quando la percezione dell’amaro e l’assorbimento del farmaco si intersecano
Oltre a spiegare perché la chemioterapia a base di platino può risultare amara, lo studio rivela una svolta inaspettata: gli stessi recettori dell’amaro sembrano influenzare anche quanto di questi farmaci entra nelle cellule. Utilizzando spettrometria di massa ad alta sensibilità, i ricercatori hanno misurato il contenuto di platino all’interno delle cellule dopo il trattamento. Le cellule prive di certi recettori, come TAS2R4 o TAS2R43, hanno accumulato più platino rispetto alle cellule normali, suggerendo che recettori integri contribuiscono a limitare l’assorbimento o la ritenzione cellulare di questi agenti tossici. Na‑HED non ha modificato l’assorbimento di carboplatino, ma ha ridotto la quantità di cisplatino che entrava nelle cellule e ha mostrato un’interazione molecolare diretta con il cisplatino in soluzione. Ciò suggerisce che un composto mascherante l’amaro potrebbe, in alcuni casi, modulare anche quanto intensamente un farmaco agisce sui tessuti locali, come le cellule del gusto o le ghiandole salivari. 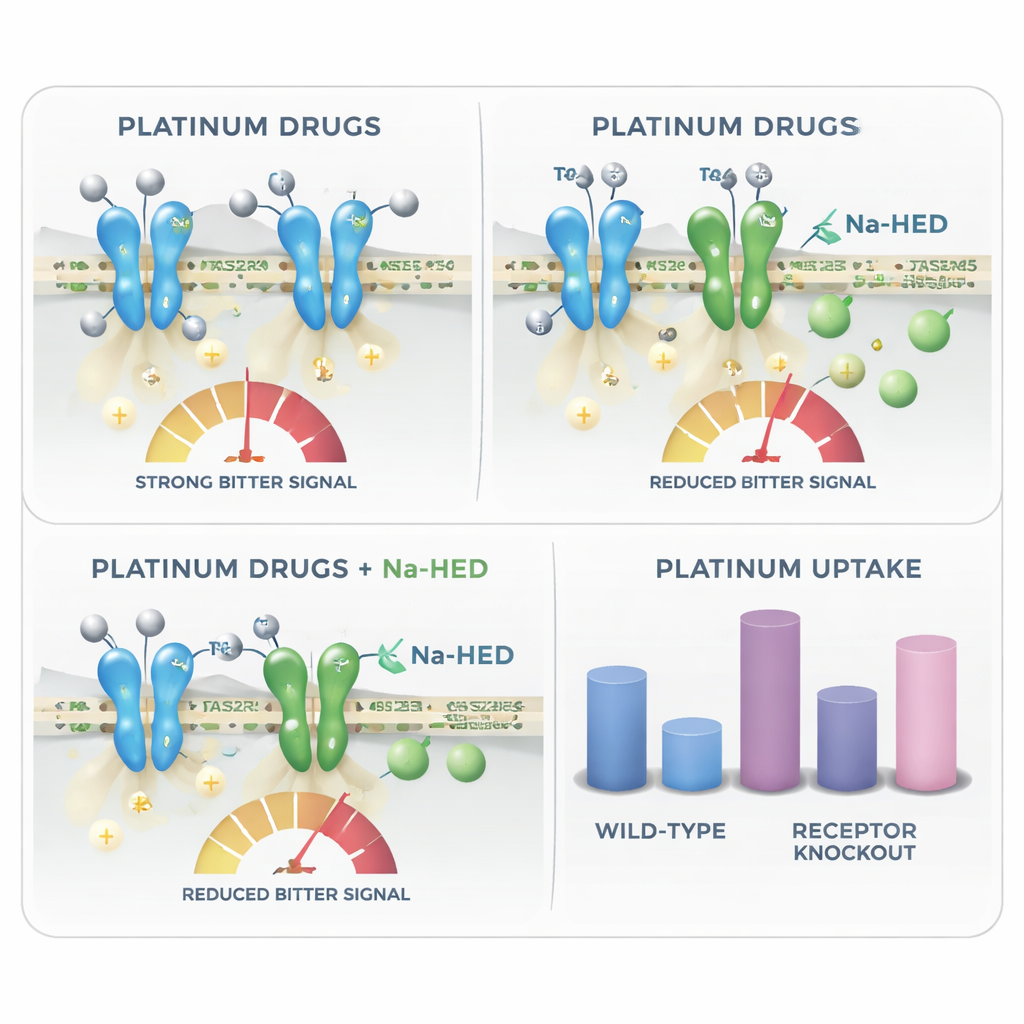
Verso esperienze gustative più miti durante la chemioterapia
Per i pazienti, la principale conclusione è incoraggiante: la chemioterapia a base di platino sembra provocare problemi di sapore amaro attivando direttamente recettori dell’amaro che esistono non solo sulla lingua ma anche in cellule di tipo gastrico. Il cisplatino appare particolarmente potente a questo riguardo. Lo studio dimostra che Na‑HED può attenuare sostanzialmente questo segnale amaro in un sistema cellulare controllato e potrebbe anche limitare l’assorbimento locale di cisplatino. Pur richiedendo conferme negli esseri umani, questi risultati indicano la possibilità di futuri trattamenti «sciacqua e sputa» contenenti Na‑HED che potrebbero attenuare sensazioni amare e metalliche intense senza interferire con l’azione antitumorale dei farmaci nell’organismo.
Citazione: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Parole chiave: cambiamenti del gusto da chemioterapia, recettori del gusto amaro, cisplatino e carboplatino, composti mascheranti l'amaro, nutrizione dei pazienti oncologici