Clear Sky Science · it
Indagine sperimentale e correlazione termodinamica della solubilità del clordiazepossido in CO₂ supercritica
Perché sciogliere un farmaco noto in modo nuovo conta
Molti farmaci moderni sono efficaci ma difficili da formulare in modo efficiente: possono non dissolversi facilmente, degradarsi durante la produzione o richiedere grandi quantità di solventi organici. Questo studio esamina il clordiazepossido, un medicinale usato da tempo per l’ansia, e pone una domanda pratica di ampio impatto: quanto si dissolve in anidride carbonica supercritica, un solvente più pulito e modulabile che potrebbe aiutare a ottenere particelle farmaceutiche più sicure ed efficaci?
Un fluido «verde» che si comporta sia da gas sia da liquido
L’anidride carbonica supercritica è CO₂ portata oltre una certa pressione e temperatura fino a non essere né un gas convenzionale né un liquido normale. In questo stato scorre come un gas ma ha una densità simile a un liquido, capace di dissolvere molte sostanze. L’industria la usa già per decaffeinare il caffè ed estrarre aromi e oli. Per il settore farmaceutico, la CO₂ supercritica è interessante perché è non‑tossica, accettata dai regolatori, economica e facilmente riciclabile. Può aiutare a creare particelle di farmaco piccole e uniformi e ridurre la necessità di solventi organici aggressivi—se, e solo se, il farmaco si dissolve in essa in misura utile.
Misurare come si comporta un farmaco per l’ansia sotto pressione
Gli autori si sono proposti di misurare, per la prima volta, quanto clordiazepossido si dissolve in CO₂ supercritica pura all’interno di una finestra di processo pratica. Hanno posto polvere solida del farmaco in una cella ad alta pressione e fatto fluire CO₂ attraverso la stessa a pressioni comprese tra 12 e 30 megapascals e temperature tra 308 e 338 kelvin (circa 35–65 °C). Dopo aver lasciato il sistema raggiungere l’equilibrio, hanno campionato la fase di CO₂, l’hanno espansa rapidamente in un solvente e hanno usato l’assorbimento nell’ultravioletto‑visibile per determinare quanto farmaco era stato dissolto. La solubilità complessiva variava da circa 20 a 576 parti per milione, corrispondenti a frazioni molari tra 0,0198×10⁻³ e 0,576×10⁻³, valori in linea con molti altri farmaci moderatamente solubili in CO₂ supercritica.
Come pressione e temperatura influenzano la solubilità
Le misure hanno rivelato schemi chiari e intuitivi. A temperatura fissa, aumentare la pressione aumentava sempre la solubilità. Una pressione maggiore comprime le molecole di CO₂ rendendo la fase supercritica più densa e più efficace nel circondare e trasportare le molecole del farmaco. La temperatura ha un effetto più sottile. A pressioni più basse, riscaldare il sistema tendeva a ridurre la solubilità perché assottigliava la CO₂ e ne diminuiva il potere solvente. Oltre una pressione di crossover di circa 19 megapascals, la tendenza si inverteva: temperature più alte aumentavano la solubilità perché favorivano la tendenza del farmaco a passare dallo stato solido al fluido. Questo equilibrio tra densità del fluido e volatilità intrinseca del farmaco è caratteristico dei sistemi supercritici ed è importante per scegliere condizioni operative pratiche.
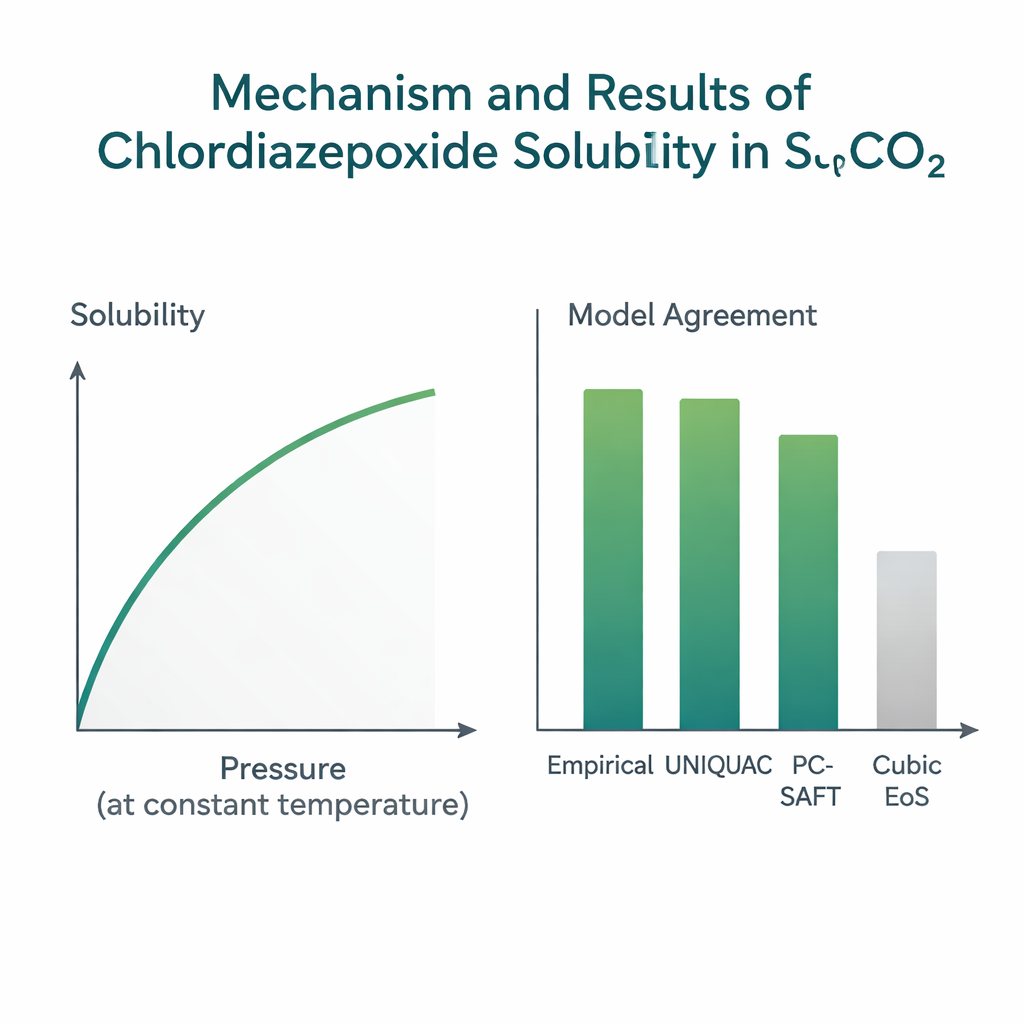
Insegnare ai modelli a prevedere ciò che vede il laboratorio
Poiché condurre esperimenti ad alta pressione è lento e costoso, gli ingegneri si affidano a modelli matematici per prevedere la solubilità in nuove condizioni o per farmaci affini. Il gruppo ha testato diverse famiglie di modelli usando il nuovo set di dati. Semplici formule empiriche «basate sulla densità», che collegano la solubilità direttamente alla densità della CO₂ e alla temperatura con pochi parametri di adattamento, hanno dato le migliori prestazioni. In particolare, la consolidata correlazione di Chrastil ha riprodotto i dati con uno scarto medio di circa il 5%, e altre formule simili hanno ottenuto risultati analoghi. Un approccio più fisico e dettagliato, denominato UNIQUAC e basato su un liquido espanso che tiene conto di dimensioni, forma molecolare ed energie di interazione, ha raggiunto un’accuratezza comparabile, intorno al 6% di scarto. Al contrario, le equazioni di stato cubiche comunemente usate—formule generali per il comportamento dei fluidi—hanno mostrato scarti intorno al 20%, mancando dettagli più fini sull’interazione specifica di questo farmaco con la CO₂.
Cosa significa per la produzione farmaceutica futura
In termini semplici, lo studio dimostra che il clordiazepossido si dissolve nella CO₂ supercritica in condizioni rilevanti per la tecnologia, e che il suo comportamento può essere descritto molto bene con modelli relativamente semplici e ben scelti. Ciò fornisce una guida affidabile per progettare processi più verdi per ottenere nuove forme solide o nanoparticelle del farmaco, migliorando stabilità o assorbimento nell’organismo. Più in generale, il lavoro fornisce un raro set di dati misurati con cura per un farmaco di largo uso e dimostra quali strumenti di modellazione sono più attendibili nella pianificazione di processi con CO₂ supercritica—informazioni utili per guidare una produzione più pulita ed efficiente di molti altri farmaci.
Citazione: Saadati Ardestani, N., Noubigh, A., Esfandiari, N. et al. Experimental investigation and thermodynamic correlation of chlordiazepoxide solubility in supercritical CO₂. Sci Rep 16, 6552 (2026). https://doi.org/10.1038/s41598-026-35623-1
Parole chiave: anidride carbonica supercritica, solubilità dei farmaci, clordiazepossido, processi farmaceutici ecologici, modellazione termodinamica