Clear Sky Science · it
Un approccio di proteomica e redox-proteomica per comprendere l’eterogeneità della SDRA
Perché è importante per le persone in terapia intensiva
La sindrome da distress respiratorio acuto (SDRA) è una forma pericolosa per la vita di insufficienza polmonare che può colpire persone con infezioni gravi, traumi o altre patologie critiche. Molti pazienti con SDRA appaiono simili al letto del paziente, eppure alcuni guariscono mentre altri no, e nessun farmaco ha dimostrato di invertire specificamente la sindrome. Questo studio pone una domanda semplice ma cruciale: se esaminiamo da vicino le proteine e le reazioni chimiche nei polmoni e nel sangue dei pazienti con SDRA, possiamo scoprire tipi biologici nascosti della malattia che spieghino perché i pazienti evolvono in modo così diverso?
Esaminare i polmoni, non solo il sangue
Per indagare ciò, i ricercatori hanno seguito 16 adulti in terapia intensiva con SDRA assistiti da ventilatori. Entro i primi tre giorni dalla diagnosi hanno raccolto sangue e un campione speciale chiamato liquido di lavaggio broncoalveolare (BAL), una delicata lavanda degli spazi aerei nei polmoni. Hanno ripetuto queste raccolte nei giorni successivi quando possibile. Utilizzando spettrometria di massa avanzata, hanno misurato centinaia di proteine in ciascun campione (proteomica) e, cosa cruciale, hanno anche esaminato quanto fossero ossidate alcune di queste proteine (redox-proteomica), indicatore del loro danno o della loro regolazione da parte delle specie reattive dell’ossigeno, i prodotti chimici aggressivi dell’infiammazione.
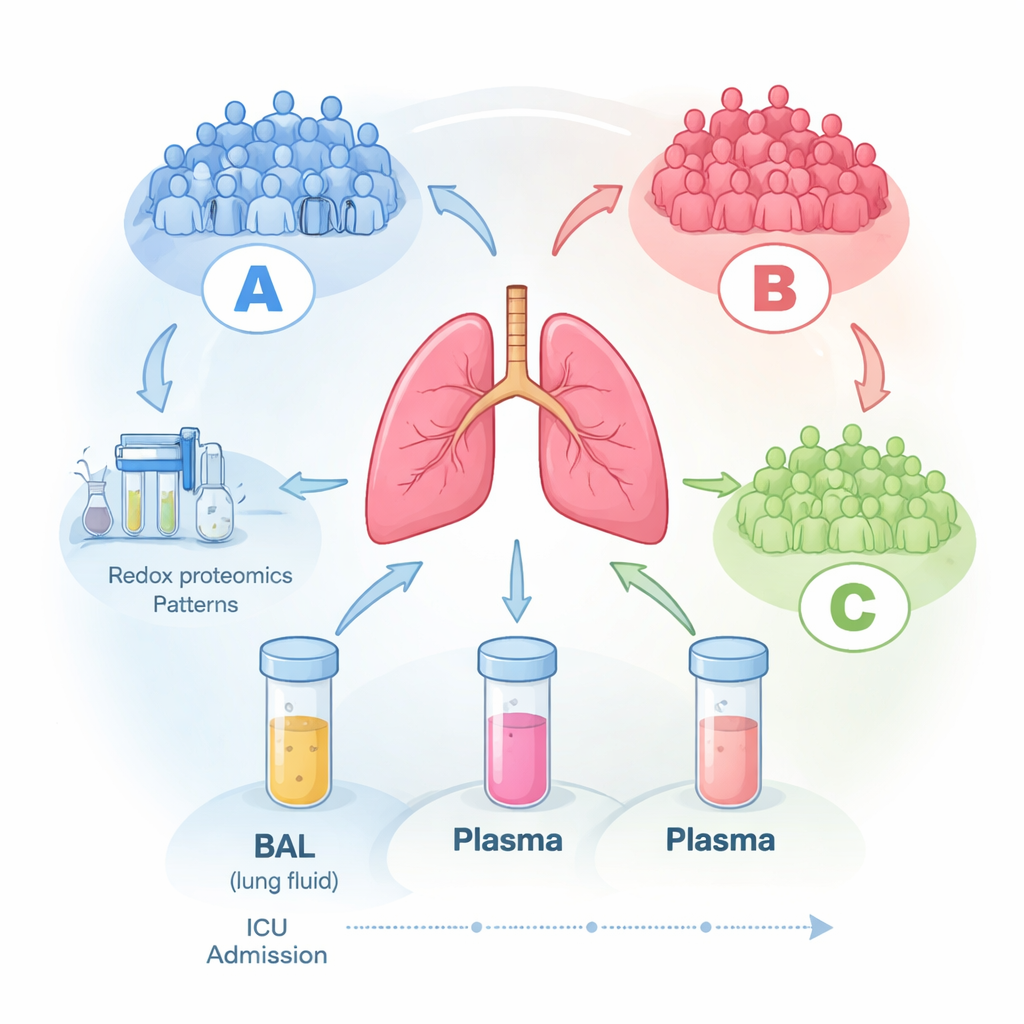
Emergono tre gruppi nascosti di pazienti
Quando il team ha lasciato che i dati si raggruppassero da soli senza fornire al computer informazioni sui pazienti, è emerso un pattern chiaro nei campioni di liquido polmonare: tre gruppi molecolari distinti, denominati A, B e C. I pazienti del gruppo A tendevano a essere più gravemente malati al momento dell’arruolamento, mentre i gruppi B e C presentavano malattia meno grave. In modo significativo, queste firme molecolari sono rimaste in gran parte stabili per fino a sei giorni in terapia intensiva, suggerendo che ogni paziente rientra in un modello biologico relativamente coerente anziché fluttuare casualmente giorno per giorno. Le misure cliniche standard—come i livelli di ossigeno, la durata della degenza o i punteggi generali di gravità—non si sono correlate bene con questi raggruppamenti molecolari, indicando che gli strumenti clinici abituali perdono aspetti chiave della biologia che avviene nei polmoni.
Stress ossidativo e le difese dell’organismo
Un tema ricorrente nei dati è stato l’equilibrio tra le specie reattive dell’ossigeno dannose e le difese antiossidanti dell’organismo. Nel gruppo A, il più grave, molte proteine polmonari coinvolte nella produzione di energia e nel mantenimento cellulare erano presenti a livelli più bassi. Ancora più indicativo, importanti enzimi antiossidanti come le perossiredossine, proteine correlate al glutatione, tioredossina e catalasi risultavano significativamente ridotti. Al contrario, i gruppi B e soprattutto C mostravano livelli più elevati di queste proteine protettive, suggerendo che i loro polmoni fossero più attrezzati per disattivare ossidanti nocivi e limitare i danni collaterali dell’infiammazione. I pattern nello stato di ossidazione delle proteine hanno aggiunto un ulteriore livello di informazione, mostrando sottogruppi diversi di proteine ossidate arricchite nei gruppi più e meno gravi.
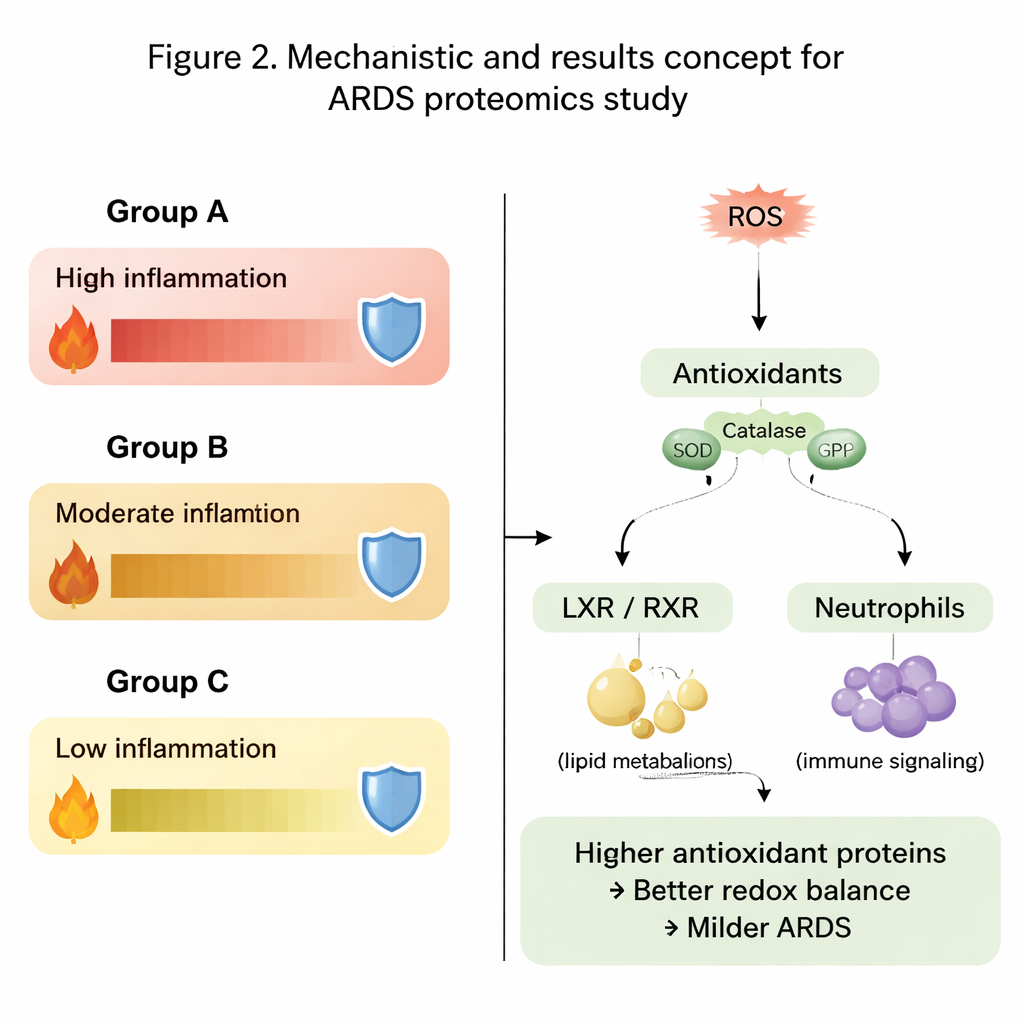
Vie di segnalazione che plasmano l’infiammazione
Oltre alle singole proteine, gli autori hanno esaminato interi percorsi biologici. Hanno trovato che vie legate all’infiammazione, al metabolismo del colesterolo e dei lipidi e all’attività delle cellule immunitarie si comportavano in modo diverso nei tre gruppi. Segnali connessi alla via del recettore X del fegato–recettore X dei retinoidi (LXR/RXR) e a un enzima chiamato DHCR24, che insieme regolano sia il metabolismo lipidico sia le risposte immune, sono risultati particolarmente rilevanti. Nel gruppo più grave queste vie erano previste come più attive, associate a una segnalazione ridotta dell’interleuchina-12, messaggero immune. Allo stesso tempo, le vie che coinvolgono le specie reattive dell’ossigeno, la loro detossificazione e l’attività dei neutrofili (globuli bianchi) mostravano pattern contrastanti tra liquido polmonare e sangue, sottolineando che ciò che accade localmente nel polmone può differire da quanto osservato nella circolazione.
Cosa potrebbe significare per le cure future
Questo piccolo studio esplorativo non cambia il trattamento odierno e i suoi risultati devono essere confermati in gruppi di pazienti molto più ampi. Tuttavia mostra che profilando da vicino le proteine e il loro stato redox direttamente nel liquido polmonare—piuttosto che basarsi solo su analisi del sangue o punteggi clinici—è possibile distinguere sottotipi biologicamente significativi di SDRA. Questi sottotipi differiscono per stress ossidativo, capacità antiossidante, metabolismo e segnalazione immune, e rimangono relativamente stabili nei primi giorni critici della malattia. In futuro, queste impronte molecolari potrebbero aiutare i medici a classificare i pazienti con SDRA in gruppi più precisi, scegliere terapie mirate in base al modello biologico e progettare trial clinici più intelligenti con maggiori probabilità di trovare trattamenti efficaci.
Citazione: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Parole chiave: sindrome da distress respiratorio acuto, proteomica, stress ossidativo, lavaggio broncoalveolare, terapia intensiva