Clear Sky Science · it
Sequenza genomica completa e caratterizzazione funzionale di Bacillus amyloliquefaciens NJF-55: un candidato probiotico derivato da pecora
Perché i batteri intestinali di una pecora ci riguardano
Dietro le quinte di ogni animale sano c’è una vivace comunità di microrganismi intestinali che aiutano a digerire il cibo, addestrano il sistema immunitario e tengono sotto controllo i germi nocivi. Questo studio si concentra su uno di questi microrganismi, un ceppo di Bacillus amyloliquefaciens chiamato NJF-55, scoperto nel colon di una pecora sana. Leggendo l’intero suo libro delle istruzioni genetiche, gli autori pongono una questione pratica con grandi implicazioni per l’allevamento e la produzione alimentare: questo batterio naturale potrebbe essere sviluppato in un probiotico sicuro ed efficace che aiuti il bestiame a rimanere sano senza dipendere così pesantemente dagli antibiotici?
Un aiuto robusto dall’intestino di una pecora
I ricercatori hanno iniziato isolando NJF-55 dal colon distale di un ariete sano e confermandone l’identità con metodi basati sul DNA. Hanno quindi sequenziato il suo genoma completo, assemblando un singolo cromosoma circolare e un piccolo plasmide — un anello aggiuntivo di DNA — entrambi con caratteristiche tipiche per questo gruppo di Bacillus. I controlli di qualità hanno mostrato che la sequenza era quasi completa e priva di errori rilevanti. Quando hanno confrontato NJF-55 con parenti ben noti, si è raggruppato strettamente con altri ceppi di B. amyloliquefaciens già considerati come probiotici e microrganismi benefici per le piante.
Progettato per vivere in un ambiente intestinale ostile
Un’analisi dettagliata dei geni ha rivelato che NJF-55 è un tuttofare metabolico. Possiede tutta la macchina centrale necessaria per trasformare zuccheri, amminoacidi e altri nutrienti in energia, e codifica numerosi sistemi di trasporto per introdurre queste sostanze nella cellula. Al pari importante per un probiotico, dispone di un ricco arsenale per sopravvivere allo stress: geni per la formazione di spore resistenti, la riparazione del DNA, la gestione dello stress ossidativo e l’adattamento a variazioni di temperatura e salinità. Il genoma contiene inoltre molti geni legati al movimento, all’adesione e alla formazione di biofilm, suggerendo che NJF-55 può spostarsi verso nicchie favorevoli, aderire alle superfici intestinali e costruire comunità protettive una volta arrivato. 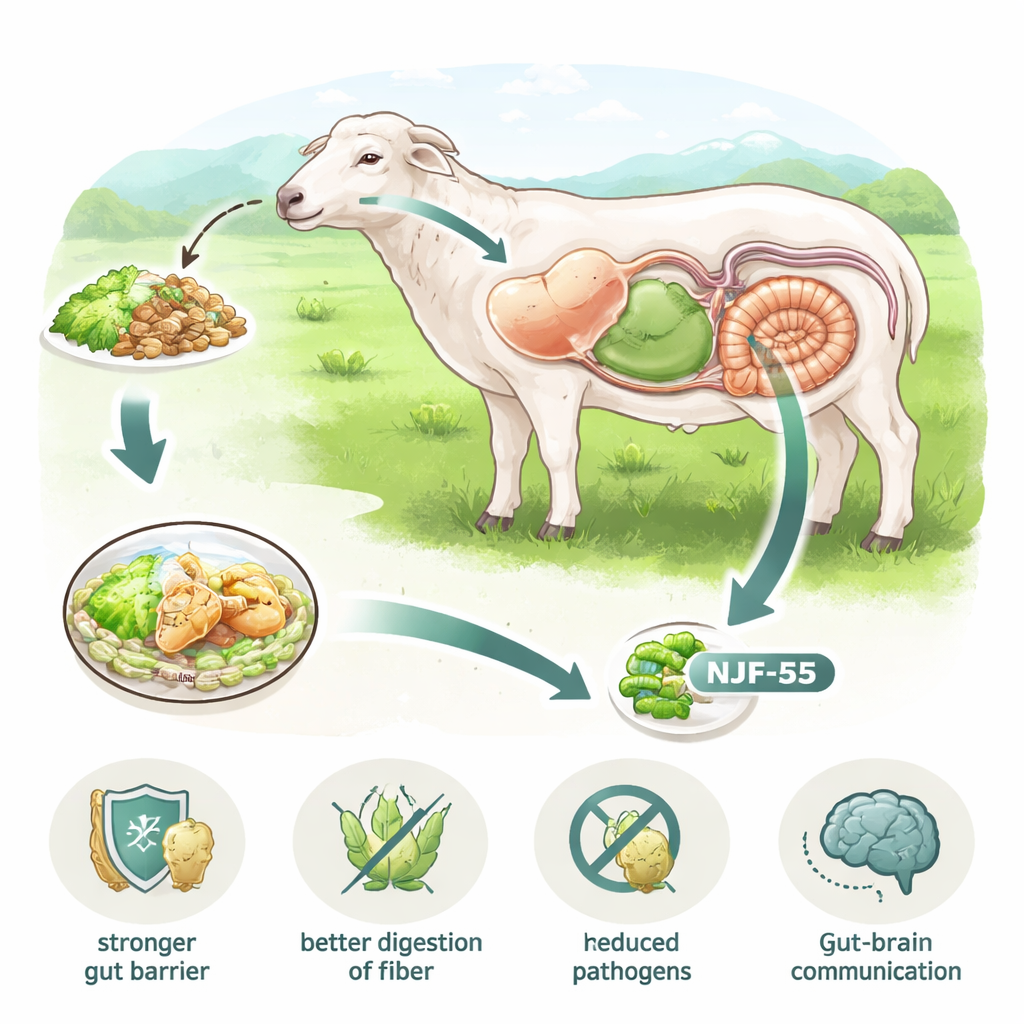
Nutre l’ospite e combatte i germi
Il genoma del ceppo suggerisce che fa più che badare a se stesso. NJF-55 porta geni per la produzione di enzimi digestivi che possono aiutare a degradare fibre vegetali complesse, un compito chiave nel rumine e negli intestini degli erbivori. Possiede anche vie metaboliche complete per la sintesi di diverse vitamine del gruppo B, inclusi riboflavina, folati, biotina e forme di vitamina B12. Queste vitamine sono importanti per il metabolismo energetico e la funzione del sistema nervoso, collegando NJF-55 all’idea emergente che i microbi intestinali possano influenzare l’asse intestino–cervello. Sul fronte difensivo, il batterio ospita cluster genici per noti lipopeptidi e polichetidi dei Bacillus — surfattina, fengycina, bacillaene e macrolactin — composti noti per disturbare i microbi concorrenti e modulare le risposte immunitarie. Contiene inoltre diverse regioni previste per la produzione di batteriocine, piccole proteine antibiotiche in grado di inibire selettivamente batteri rivali.
Sicurezza prima di tutto: ciò che il genoma non contiene
Poiché i probiotici vengono somministrati a numerosi animali, la sicurezza è cruciale. Gli autori hanno utilizzato più database e strumenti di screening per cercare nel genoma di NJF-55 i classici geni di tossine e gli elementi acquisiti di resistenza agli antibiotici. Non hanno trovato i fattori di virulenza tipici associati a ceppi di Bacillus patogeni, né geni di resistenza collegati a farmaci di importanza medica come i beta-lattamici o i fluorochinoloni. I quattro residui virali (profagi) incorporati nel cromosoma erano privi di evidenti geni di tossina o resistenza, e il piccolo plasmide sembrava essere un elemento di mantenimento semplice senza tratti rischiosi. Il confronto con altri quattro genomi di Bacillus ha mostrato che la maggior parte delle caratteristiche legate ai probiotici — come la tolleranza alla bile, le risposte allo stress e i sistemi di acquisizione del ferro — appartengono a un nucleo condiviso, mentre NJF-55 si distingue principalmente per il possesso di copie extra di alcune famiglie geniche benefiche, incluse enzimi per la produzione di composti antimicrobici e fattori che rafforzano la resilienza allo stress. 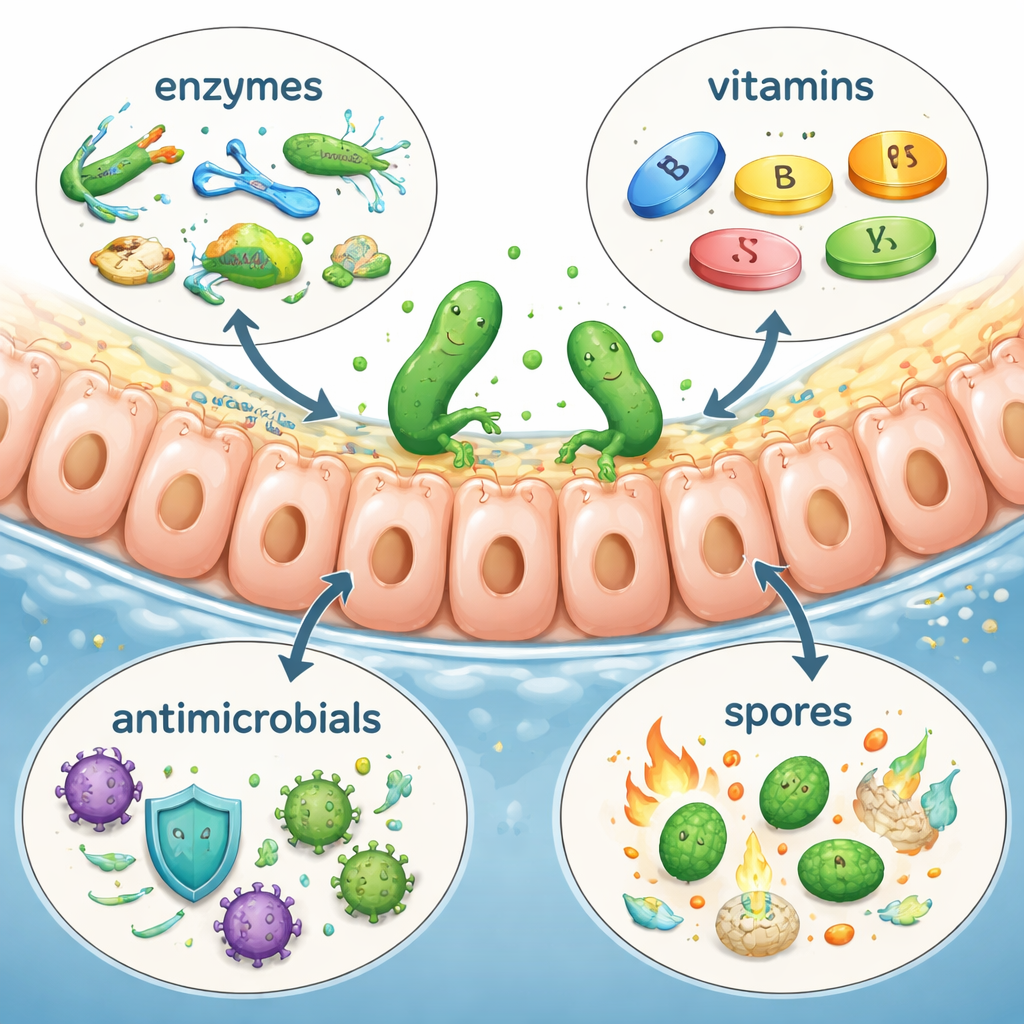
Dalla mappa del genoma all’uso in stalla
Complessivamente, il profilo genetico di Bacillus amyloliquefaciens NJF-55 dipinge il ritratto di un microbo robusto e adattabile, ben adatto alla vita nel tratto gastrointestinale dei ruminanti. Sembra in grado di aiutare l’ospite a digerire alimenti fibrosi, fornire vitamine, competere con microbi dannosi e resistere al percorso ostile attraverso stomaco e intestini — tutto ciò senza evidenti segnali di virulenza o resistenza antibiotica problematica. Gli autori sottolineano che queste conclusioni si basano su predizioni dai dati del DNA e test di laboratorio; sono ancora necessari trial alimentari sul campo e analisi chimiche dettagliate. Ma se quegli studi confermeranno le promesse viste nel genoma, NJF-55 potrebbe entrare a far parte delle formulazioni probiotiche di nuova generazione che supportano la salute e la produttività animale riducendo la dipendenza dagli antibiotici.
Citazione: Al-Hasan, B.A., Janabi, A.H.D. & Helmer, C. Complete genome sequence and functional characterization of Bacillus amyloliquefaciens NJF-55: a sheep-derived probiotic candidate. Sci Rep 16, 6408 (2026). https://doi.org/10.1038/s41598-026-35600-8
Parole chiave: batteri probiotici, salute intestinale dei ruminanti, Bacillus amyloliquefaciens, microbioma del bestiame, alternative agli antibiotici