Clear Sky Science · it
L’autoencoder quantistico per la riduzione del rumore migliora la qualità delle immagini del fondo oculare per lo screening precoce della retinopatia diabetica
Scansioni oculari più nitide per proteggere la vista
Per milioni di persone con diabete, una semplice fotografia della parte posteriore dell’occhio può rivelare i primi segnali di avvertimento della perdita della vista. Tuttavia queste immagini retiniche sono spesso granulose o sfocate dal rumore della fotocamera, rendendo difficili da distinguere quei dettagli minuscoli che possono salvare la vista. Questo articolo esplora un alleato insolito nella lotta contro la cecità: un nuovo metodo di pulizia delle immagini che combina il deep learning attuale con i computer quantistici del futuro per produrre scansioni oculari più nitide per lo screening precoce della retinopatia diabetica.
Perché i piccoli dettagli nelle foto dell’occhio sono importanti
La retinopatia diabetica è una malattia in cui l’iperglicemia danneggia progressivamente i sottili vasi sanguigni della retina. I medici cercano piccole dilatazioni dei vasi (microaneurismi), sottili capillari ramificati e lievi cambiamenti di texture per individuare la malattia prima che la vista venga compromessa. Questi segni sono spesso lunghi solo pochi pixel in una fotografia standard del fondo oculare. Sfortunatamente, le immagini rilevate nei centri di screening reali sono soggette a molti tipi di rumore: imperfezioni del sensore, illuminazione scarsa e sfocatura da movimento. Gli strumenti tradizionali di pulizia, come la smoothing gaussiana o i filtri mediani, possono rimuovere parte di questo rumore, ma tendono a cancellare proprio le strutture delicate che i medici considerano più importanti.
Limiti dei filtri intelligenti odierni
Negli ultimi anni, i metodi di deep learning sono diventati i cavalli di battaglia del denoising nelle immagini mediche. Autoencoder convoluzionali, reti residuali (ResNet) e CNN di denoising specializzate possono imparare come dovrebbe apparire un’immagine «pulita» e quindi sottrarre il rumore dalle nuove scansioni. Questi modelli funzionano bene, ma presentano delle criticità. Per catturare pattern complessi delle immagini richiedono molteplici strati e milioni di parametri, con grandi esigenze computazionali e numerosi dati di addestramento. Nell’imaging medico, dove i dataset etichettati sono relativamente piccoli, modelli così grandi possono sovra‑adattarsi—memorizzando le immagini di addestramento invece di generalizzare—e possono comunque sfocare vasi sottili o piccole lesioni.
Portare le idee quantistiche nel quadro
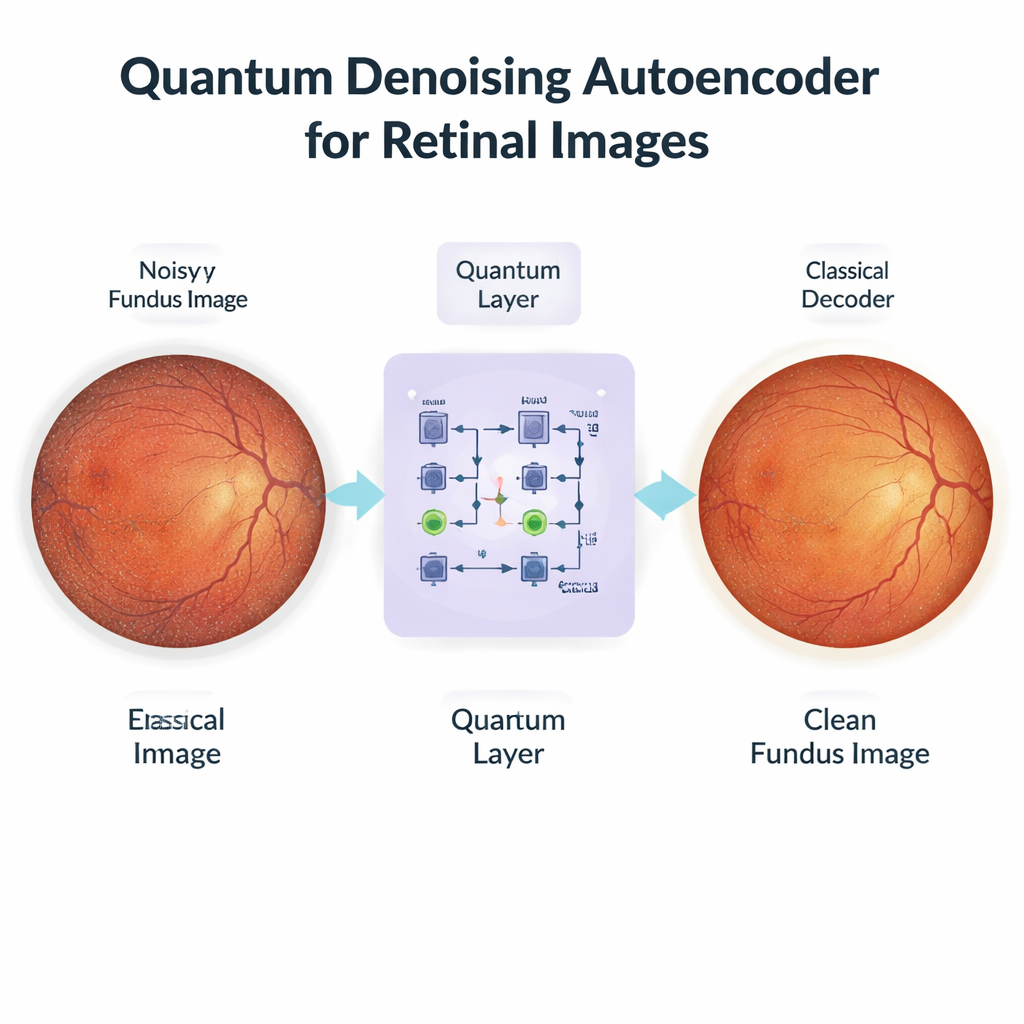
Gli autori propongono un approccio ibrido chiamato Quantum Denoising Autoencoder (QDAE). A prima vista somiglia a una normale pipeline di deep learning: un encoder classico comprime ogni foto oculare rumorosa in un set compatto di caratteristiche, e un decoder classico ricostruisce poi un’immagine ripulita. La svolta chiave avviene nel mezzo. Invece di passare le feature direttamente attraverso un semplice collo di bottiglia matematico, QDAE le converte in stati in stile quantistico e le elabora con un piccolo circuito quantistico parametrizzato prima di riconvertirle. Su macchine quantistiche fisiche, la sovrapposizione permetterebbe di considerare molte combinazioni di feature contemporaneamente e l’entanglement collegherebbe porzioni distanti dell’immagine. Anche se questo lavoro utilizza circuiti simulati su una GPU tradizionale, la stessa struttura permette al modello di rappresentare relazioni non lineari ricche tra i pixel usando un numero relativamente ridotto di parametri allenabili.
Immagini più nitide, vasi sottili preservati
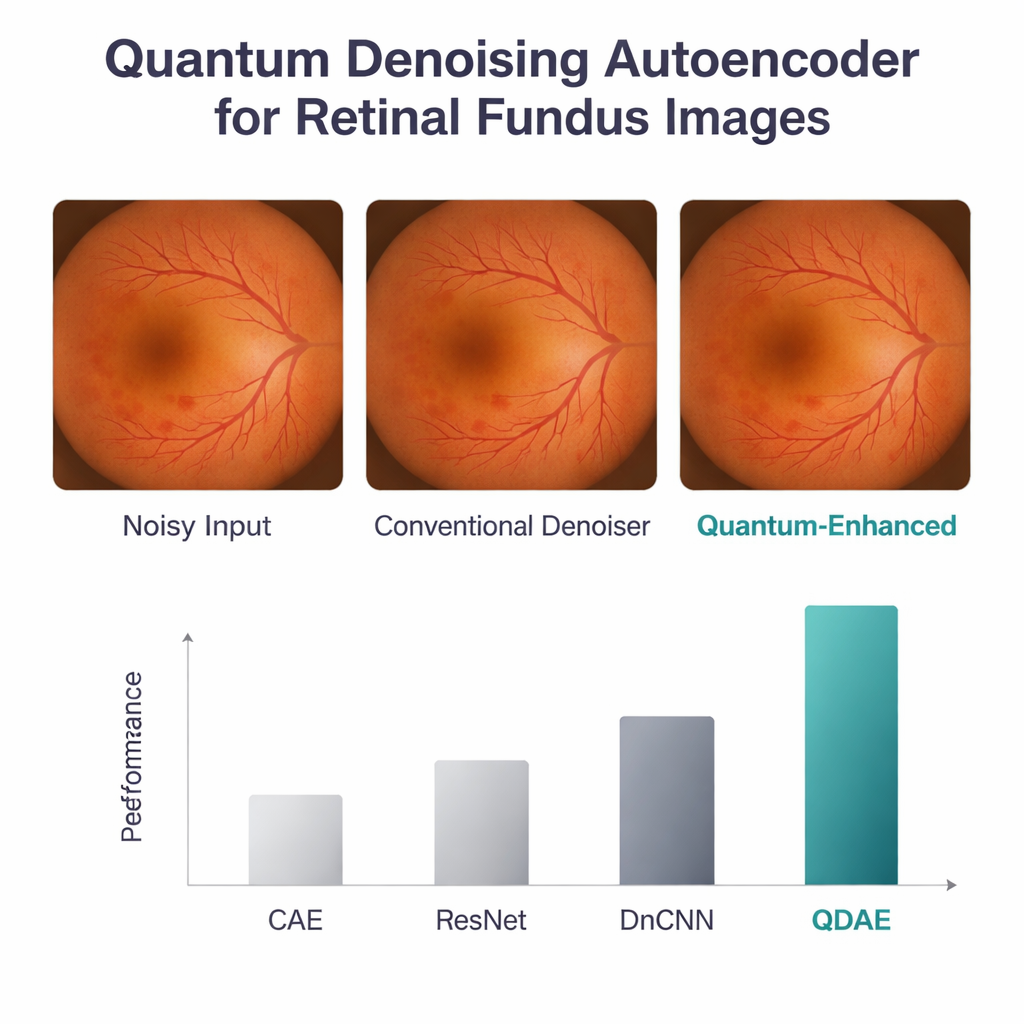
Per testare il QDAE, i ricercatori hanno usato un dataset pubblico di immagini retiniche, ridimensionate a 224×224 pixel e corrotte artificialmente con rumore gaussiano e speckle realistici. Hanno confrontato il loro metodo con tre solide baseline: un autoencoder convoluzionale, un modello basato su ResNet e una nota CNN per il denoising. Tutti i modelli sono stati addestrati e valutati sugli stessi dati usando metriche standard di qualità dell’immagine. Il modello arricchito con la componente quantistica ha prevalso su tutte le misure principali: ha raggiunto un rapporto segnale‑rumore di picco (PSNR) di 38,8 dB e un indice di similarità strutturale (SSIM) di 0,96, valori ben superiori alle reti classiche. Ha inoltre preservato meglio l’intensità e i pattern di texture originali delle immagini, inclusa la luminosità e il contrasto del disco ottico, della macula e della sottile rete vascolare. Sebbene il passaggio quantistico abbia aggiunto un piccolo ritardo—circa mezzo secondo per immagine—il costo computazionale complessivo è rimasto simile a quello delle profonde CNN grazie all’uso di circuiti poco profondi con solo quattro qubit e tre strati.
Cosa potrebbe significare per pazienti e cliniche
Per una persona con diabete, i dettagli tecnici si traducono in un semplice vantaggio: foto oculari più nitide che facilitano a software e specialisti l’individuazione precoce della malattia, quando il trattamento può ancora prevenire la perdita della vista. Il QDAE agisce come una fase intelligente di pre‑pulizia che può integrarsi nei sistemi di screening esistenti, aiutando gli strumenti a valle che segmentano le lesioni o valutano la gravità della malattia. Poiché la componente quantistica è attualmente simulata, gli ospedali non avrebbero bisogno di hardware quantistico speciale per provarlo, ma il progetto è pronto per i futuri dispositivi quantistici man mano che matureranno. Lo studio richiede ancora test clinici più ampi su immagini provenienti da molte cliniche e fotocamere, ma offre uno scorcio interessante di come il calcolo ispirato al quantistico potrebbe migliorare silenziosamente gli esami oculari di routine e, in ultima analisi, contribuire a preservare la vista.
Citazione: Chilukuri, R., P, P., Gatla, R.K. et al. Quantum denoising autoencoder improves retinal fundus image quality for early diabetic retinopathy screening. Sci Rep 16, 5970 (2026). https://doi.org/10.1038/s41598-026-35540-3
Parole chiave: retinopatia diabetica, imaging retinico, denoising delle immagini, apprendimento automatico quantistico, IA medica