Clear Sky Science · it
Nanospine di Co3O4 cresciute su ossido di grafene come efficiente elettrocatalizzatore per elettrolisi ibrida dell’acqua tramite reazioni anodiche alternative
Trasformare gli scarti di frutta nel carburante del futuro
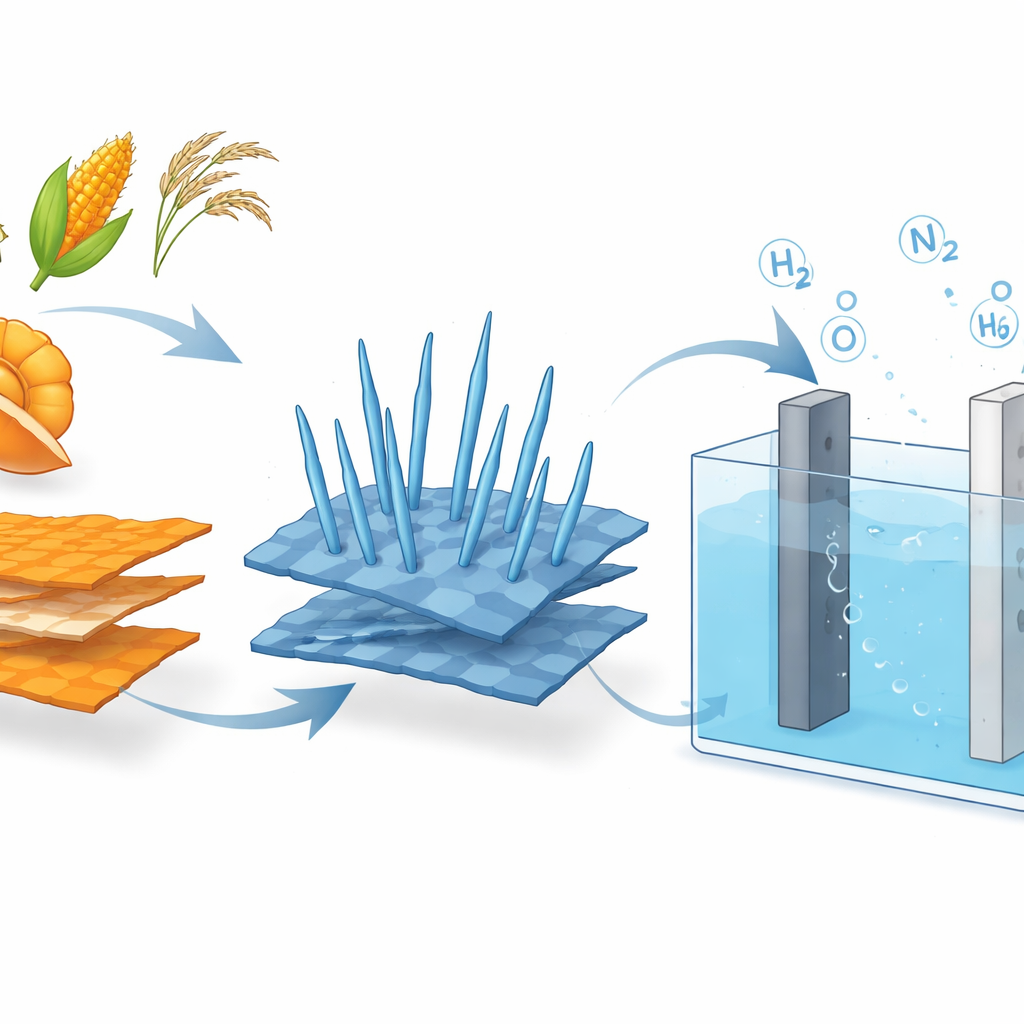
L’idrogeno è spesso decantato come un combustibile pulito del futuro, ma produrlo richiede tipicamente molta elettricità. Questo studio mostra come qualcosa di semplice come gli scarti di buccia d’arancia possa contribuire a cambiare le cose. Trasformando questi rifiuti in un materiale carbonioso speciale e combinandolo con un composto a base di cobalto, i ricercatori hanno creato un catalizzatore a basso costo in grado di produrre idrogeno consumando molta meno energia rispetto ai metodi convenzionali di scissione dell’acqua. Inoltre, sostituiscono uno stadio inefficiente dell’elettrolisi con reazioni più miti che convertono sostanze problematiche in gas innocui.
Perché la scissione tradizionale dell’acqua spreca energia
Per separare l’acqua in idrogeno e ossigeno, un elettrolizzatore fa passare corrente elettrica attraverso acqua contenente un sale o una base disciolti. Da un lato si forma facilmente gas idrogeno. Dall’altro si produce ossigeno in una reazione lenta e impegnativa, perché richiede il trasferimento di quattro elettroni in passaggi strettamente coordinati. Questo stadio di produzione dell’ossigeno, chiamato reazione anodica, è ciò che costringe gli ingegneri ad aumentare la tensione, innalzando i costi energetici. Peggio ancora, l’ossigeno viene spesso semplicemente ventilato e non utilizzato, il che significa che una larga parte dell’energia elettrica immessa nel sistema genera poco valore pratico.
Sostituire un consumatore di energia con reazioni più dolci
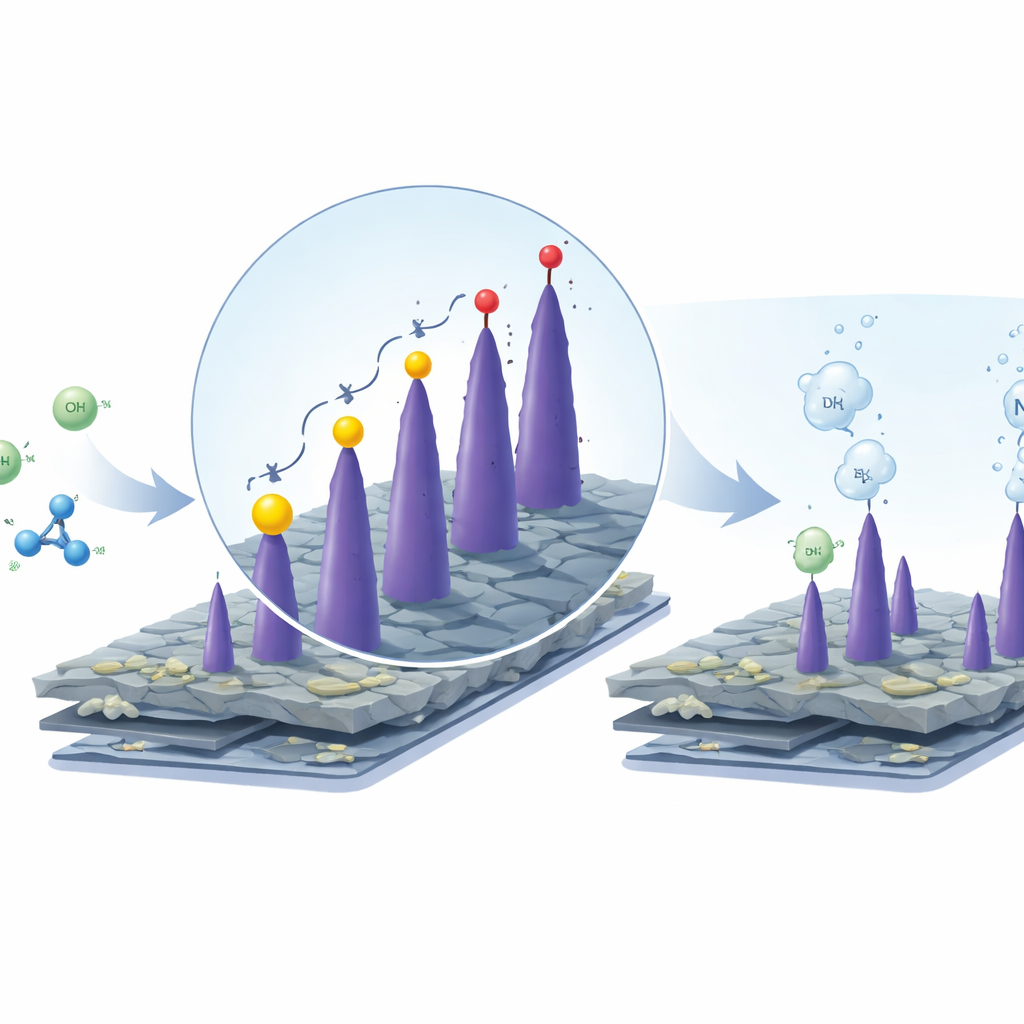
Il gruppo ha affrontato questo collo di bottiglia ripensando ciò che avviene al polo energivoro della cella. Invece di produrre ossigeno dall’acqua, si sono chiesti: cosa succederebbe se il sistema ossidasse altre sostanze chimiche più facili da gestire pur continuando a generare idrogeno dall’altro lato? Hanno scelto due composti ricchi di azoto, l’urea e l’idrazina, comuni nelle acque reflue e in processi industriali. Quando queste molecole vengono ossidate in soluzione alcalina, si decompongono in azoto gassoso, acqua e, nel caso dell’urea, anidride carbonica. Crucialmente, queste reazioni iniziano a tensioni molto più basse rispetto alla produzione di ossigeno, il che significa che la stessa quantità di idrogeno può essere generata con un apporto elettrico molto inferiore.
Dalle bucce d’arancia agli elettrodi intelligenti
Per rendere praticabile questo approccio, i ricercatori avevano bisogno di un catalizzatore economico, robusto e attivo per tre compiti distinti: produzione convenzionale di ossigeno, ossidazione dell’urea e ossidazione dell’idrazina. Hanno iniziato convertendo bucce d’arancia essiccate in ossido di grafene, un materiale carbonioso sottile e conduttivo, usando un semplice processo termico invece di trattamenti chimici aggressivi. Su questi fogli hanno fatto crescere piccolissime “nanospine” di ossido di cobalto in una camera a pressione. L’ibrido risultante — nanospine di ossido di cobalto su ossido di grafene — forma una superficie ruvida e spugnosa con numerosi siti reattivi esposti e un percorso agevole per il flusso di elettroni. Le misure hanno mostrato che il supporto in grafene impedisce l’aggregazione delle particelle di cobalto e aumenta notevolmente l’area superficiale effettiva e la conducibilità elettrica.
Come il nuovo catalizzatore riduce il costo energetico
Testato in soluzione alcalina, il nuovo elettrodo ha raggiunto una corrente di riferimento standard a tensioni significativamente inferiori rispetto al solo ossido di cobalto. Per la produzione convenzionale di ossigeno, ha reso in modo comparabile ad alcuni catalizzatori commerciali a metalli nobili. Con l’aggiunta di urea, la tensione richiesta è diminuita ulteriormente, e con l’idrazina il miglioramento è stato notevole: l’elettrodo ha richiesto solo un piccolo sovra-potenziale rispetto al valore di riferimento per sostenere la stessa corrente. In una cella a due elettrodi completa accoppiata con un elettrodo standard a base di platino per la produzione di idrogeno, l’elettrolisi assistita da idrazina ha prodotto idrogeno a soli 0,33 volt — circa 1,3 volt in meno rispetto alla scissione tradizionale dell’acqua nelle stesse condizioni. Il sistema è rimasto stabile per molte ore, con struttura e composizione del catalizzatore sostanzialmente invariate.
Cosa significa questo per l’idrogeno pulito
Per un non specialista, il messaggio è semplice: ripensando sia il materiale dell’elettrodo sia la reazione che vi avviene, i ricercatori hanno dimostrato che l’idrogeno può essere prodotto con molta meno elettricità e con ingredienti poco costosi. Gli scarti di frutta diventano uno scheletro carbonioso ad alte prestazioni; le nanospine di ossido di cobalto forniscono siti attivi; e sostituire la formazione di ossigeno con l’ossidazione di urea o idrazina riduce drasticamente la tensione necessaria. Nel caso dell’idrazina, i prodotti secondari sono principalmente azoto e acqua, evitando emissioni di carbonio aggiuntive. Pur richiedendo ulteriori studi per gestire approvvigionamento chimico e sicurezza su scala, questa strategia di elettrolisi ibrida indica una via verso una produzione di idrogeno più pulita ed economica che valorizza anche flussi di rifiuti e biomassa rinnovabile.
Citazione: Rahamathulla, N., Murthy, A.P. Co3O4 nanoneedles grown on graphene oxide as an efficient electrocatalyst for hybrid water electrolysis through alternative anodic oxidation reactions. Sci Rep 16, 8452 (2026). https://doi.org/10.1038/s41598-026-35522-5
Parole chiave: produzione di idrogeno, elettrolisi dell’acqua, ossido di grafene, ossidazione della idrazina, catalizzatori derivati dalla biomassa