Clear Sky Science · it
Genomica comparativa di Pseudomonas aeruginosa multiresistente non suscettibile alla colistina rivela lignaggi emergenti in Thailandia
Perché questo germe ospedaliero riguarda tutti
Pseudomonas aeruginosa è un germe ospedaliero che attacca le persone quando sono più vulnerabili—dopo interventi chirurgici, su ventilatori polmonari o in presenza di gravi ustioni o malattie polmonari. Per anni i medici hanno fatto affidamento su un potente antibiotico “di ultima risorsa” chiamato colistina quando gli altri farmaci falliscono. Questo studio analizza ceppi di Pseudomonas provenienti da ospedali in tutta la Thailandia che non rispondono più alla colistina né a molti altri antibiotici. Leggendo il DNA completo di questi batteri, i ricercatori mostrano come nuovi lignaggi altamente resistenti stiano emergendo e diffondendosi, e perché questo dovrebbe preoccupare pazienti, clinici e sistemi sanitari a livello mondiale.
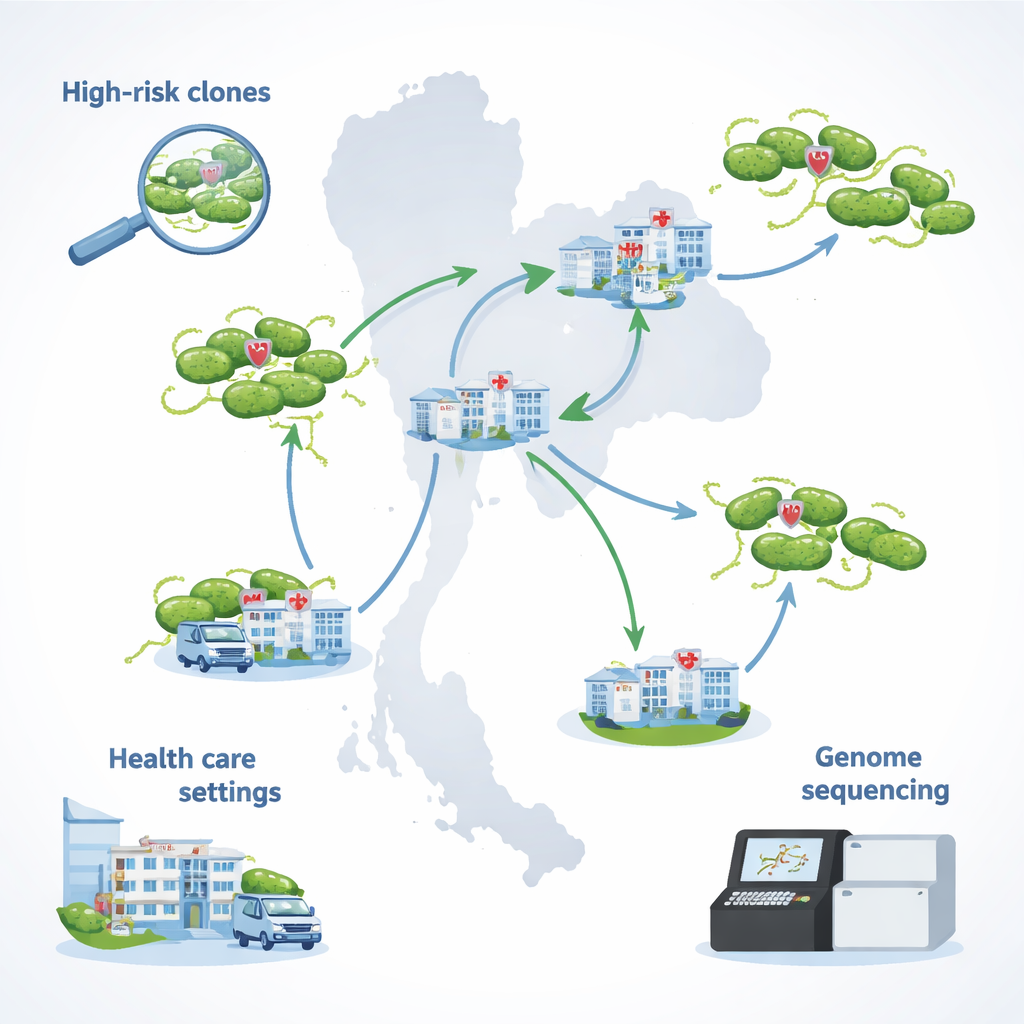
Tracciare un’infezione difficile da curare in tutta la Thailandia
Il gruppo si è concentrato su 29 ceppi di Pseudomonas aeruginosa raccolti nel 2021–2022 in ospedali che partecipano al programma nazionale thailandese di sorveglianza della resistenza agli antibiotici. Tutti questi ceppi erano multiresistenti: potevano sopportare diverse classi principali di antibiotici, comprese molecole solitamente impiegate per infezioni gravi. Crucialmente, non erano pienamente suscettibili alla colistina, il farmaco spesso riservato per casi potenzialmente letali. La maggior parte dei campioni proveniva da urine, ma altri erano prelevati da sangue, espettorato, pus e liquidi di drenaggio chirurgico—riflettendo i molti tipi di infezioni che questo germe può causare nei pazienti ospedalizzati.
Leggere le “impronte genetiche” dei batteri
Utilizzando una combinazione di sequenziamento del DNA a letture corte e lunghe, i ricercatori hanno assemblato genomi di alta qualità per ciascun ceppo. Hanno quindi confrontato questi genomi per classificare i batteri in famiglie genetiche, note come tipi di sequenza. Sono stati identificati nove tipi di sequenza distinti, rivelando una notevole diversità. Uno, etichettato ST5340, non era mai stato descritto prima. È risultato strettamente correlato a un noto clone internazionale ad alto rischio chiamato ST357, differendo in una sola delle sette classiche geni housekeeping. Nonostante questa stretta parentela, lo ST5340 si distingueva perché ogni suo isolato resisteva a tutti gli antibiotici testati, segnalandolo come un lignaggio particolarmente preoccupante.
Lignaggi ad alto rischio emergenti e la loro diffusione
Allineando piccole differenze del DNA chiamate polimorfismi a singolo nucleotide su 108 genomi thailandesi di Pseudomonas (i 29 nuovi più 79 provenienti da banche dati pubbliche), il gruppo ha ricostruito un albero genealogico dei ceppi circolanti nel paese. Questa analisi ha evidenziato diversi cluster predominanti centrati su ST5340, ST357, ST654 e ST235—lignaggi già noti, o ora emergenti, come “ad alto rischio” perché frequentemente resistono a più farmaci e causano focolai ospedalieri. In particolare lo ST5340 è apparso in più province e regioni, suggerendo una diffusione ampia anziché essere confinato a un singolo ospedale. Anche altri cloni globali ad alto rischio, come ST654 e ST235, erano presenti, mentre alcuni lignaggi di rilevanza globale come ST244 erano assenti, probabilmente perché lo studio includeva solo ceppi non suscettibili alla colistina.
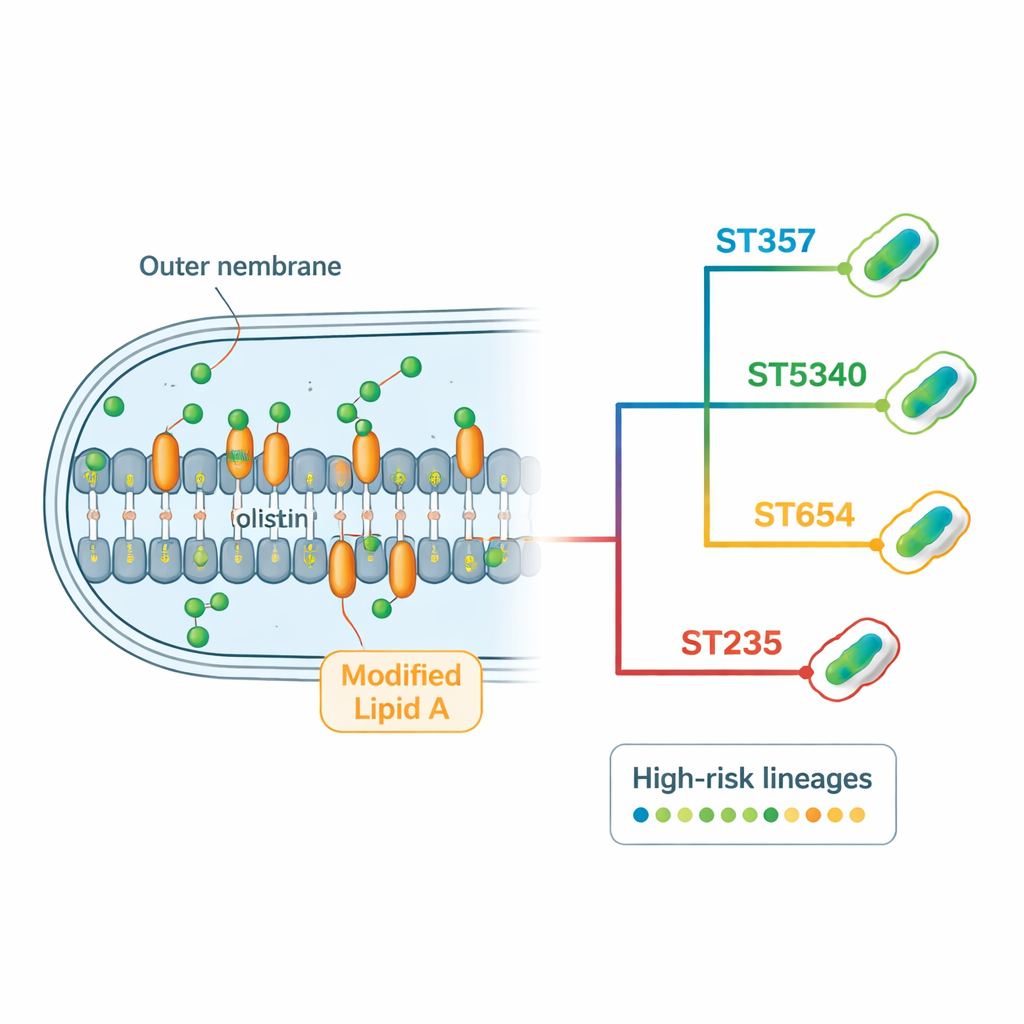
Come questi batteri eludono gli antibiotici
L’analisi genomica ha rivelato un “resistoma” ricco—l’insieme completo di geni e mutazioni di resistenza presenti in ciascun ceppo. Molti isolati codificavano diversi tipi di beta‑lattamasi, enzimi che degradano antibiotici comuni come penicilline, cefalosporine e carbapenemi. Il gene della carbapenemasi blaNDM‑1, associato alla resistenza ad alcuni dei farmaci ospedalieri più potenti, è comparso in quasi tutti i ceppi, talvolta in copie multiple. I batteri portavano anche geni che modificano chimicamente gli aminoglicosidi, oltre a potenti pompe di efflusso che funzionano come pompaggi molecolari per espellere i farmaci dalla cellula. Per la colistina, il team non ha trovato geni mobili di resistenza ma ha identificato cambiamenti ricorrenti in geni cromosomici coinvolti nella membrana esterna e nella sua regolazione. Alcune mutazioni in proteine regolatorie e in enzimi che costruiscono il lipid A sono risultate fortemente correlate alla resistenza alla colistina, specialmente nei lignaggi dominanti ST357 e ST5340.
Cosa significa per pazienti e ospedali
Combinando la sorveglianza nazionale con il sequenziamento genomico moderno, questo studio dimostra che gli ospedali thailandesi affrontano una minaccia crescente da un clone ad alto rischio di recente identificazione, ST5340, insieme a ceppi problematici globali già noti. Questi batteri non sono solo resistenti alla colistina ma anche a molti altri farmaci chiave, riducendo drasticamente le opzioni terapeutiche quando i pazienti sviluppano infezioni gravi. Per il lettore non specialista, il messaggio è chiaro: la resistenza agli antibiotici non è un rischio astratto per il futuro ma una realtà attuale che può influire direttamente sugli esiti di interventi chirurgici, cure intensive e terapie oncologiche. Gli autori sostengono che è urgente proseguire la sorveglianza genomica, rafforzare il controllo delle infezioni e usare con cautela gli antibiotici per evitare che questi lignaggi altamente resistenti diventino ancora più diffusi e difficili da contenere.
Citazione: Wankaew, N., Arigul, T., Kruasuwan, W. et al. Comparative genomics of colistin-nonsusceptible multidrug-resistant Pseudomonas aeruginosa reveals emerging lineages in Thailand. Sci Rep 16, 5968 (2026). https://doi.org/10.1038/s41598-026-35520-7
Parole chiave: Pseudomonas aeruginosa, resistenza agli antibiotici, colistina, sorveglianza genomica, infezioni ospedaliere