Clear Sky Science · it
hsa-miR-339-5p esosomiale nel plasma è associato a NOD-like receptor family CARD domain-containing 5 nell'insufficienza cardiaca con frazione di eiezione ridotta
Perché piccole molecole nel sangue possono rivelare un cuore in difficoltà
L'insufficienza cardiaca con frazione di eiezione ridotta (HFrEF) è una condizione comune in cui il cuore non riesce più a pompare sangue a sufficienza per le esigenze dell'organismo. I medici la diagnosticano spesso solo dopo che il danno è già rilevante. Questo studio esplora se messaggi microscopici in circolo nel sangue — piccole molecole di RNA confezionate in minuscole bolle chiamate esosomi — possano segnalare problemi in anticipo e chiarire come il cuore si irrigidisce e si cicatrizza nel tempo.
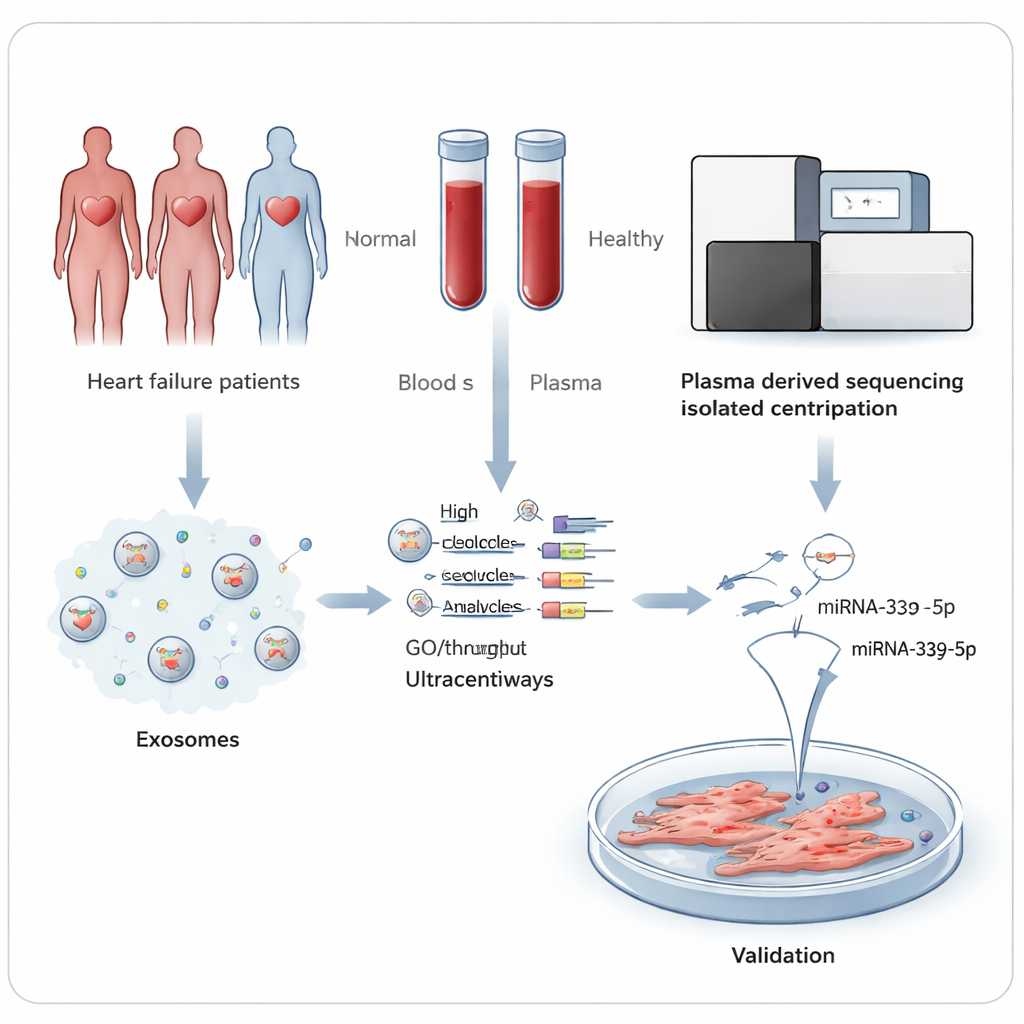
Messaggi nascosti che viaggiano nel flusso sanguigno
Il nostro sangue trasporta innumerevoli esosomi, sacche di dimensioni nanometriche rilasciate dalle cellule che trasportano proteine e materiale genetico da una cellula all'altra. Tra il loro carico ci sono i microRNA, brevi filamenti che modulano finemente quali geni vengono attivati o spenti. Poiché gli esosomi proteggono questi microRNA dalla degradazione, possono essere misurati in modo affidabile con un semplice prelievo di sangue. I ricercatori hanno ipotizzato che se il cuore in difficoltà o i tessuti correlati rilasciano una miscela di microRNA diversa rispetto a un cuore sano, quei modelli potrebbero funzionare da segnali di allarme e rivelare processi che guidano la malattia.
Confrontare pazienti con cuore indebolito e volontari sani
Il team ha raccolto il sangue di 45 persone con HFrEF e di 45 volontari sani e comparabili in un ospedale di Hefei, in Cina. Dal plasma sanguigno hanno isolato con cura gli esosomi e ne hanno confermato dimensione e forma usando la microscopia elettronica e strumenti di tracciamento delle particelle. In una prima fase hanno sequenziato i piccoli RNA presenti negli esosomi di un sottogruppo di cinque pazienti e cinque controlli. Questo approccio ad alta produttività ha rilevato centinaia di microRNA noti e ha evidenziato 27 molecole presenti a livelli nettamente diversi tra i due gruppi — 10 più elevate e 17 più basse nelle persone con insufficienza cardiaca.
Concentrare l'attenzione su un segnale evidente
Per verificare quali di questi cambiamenti fossero più affidabili, gli scienziati hanno poi utilizzato un metodo PCR altamente sensibile per misurare sei microRNA promettenti in tutti i restanti 40 pazienti e 40 controlli. Diversi segnali si sono confermati, ma uno in particolare — chiamato hsa-miR-339-5p — è emerso con chiarezza. Era costantemente più elevato nei pazienti con HFrEF e, analizzato come marcatore diagnostico, discriminava meglio questi pazienti dagli individui sani. Analisi dei percorsi basate su computer hanno suggerito che questo microRNA potrebbe agire su un gene chiamato NLRC5, che a sua volta influenza una via centrale di crescita e sopravvivenza cellulare nota come pathway PI3K/Akt, precedentemente collegata all'ispessimento del muscolo cardiaco e alla fibrosi.
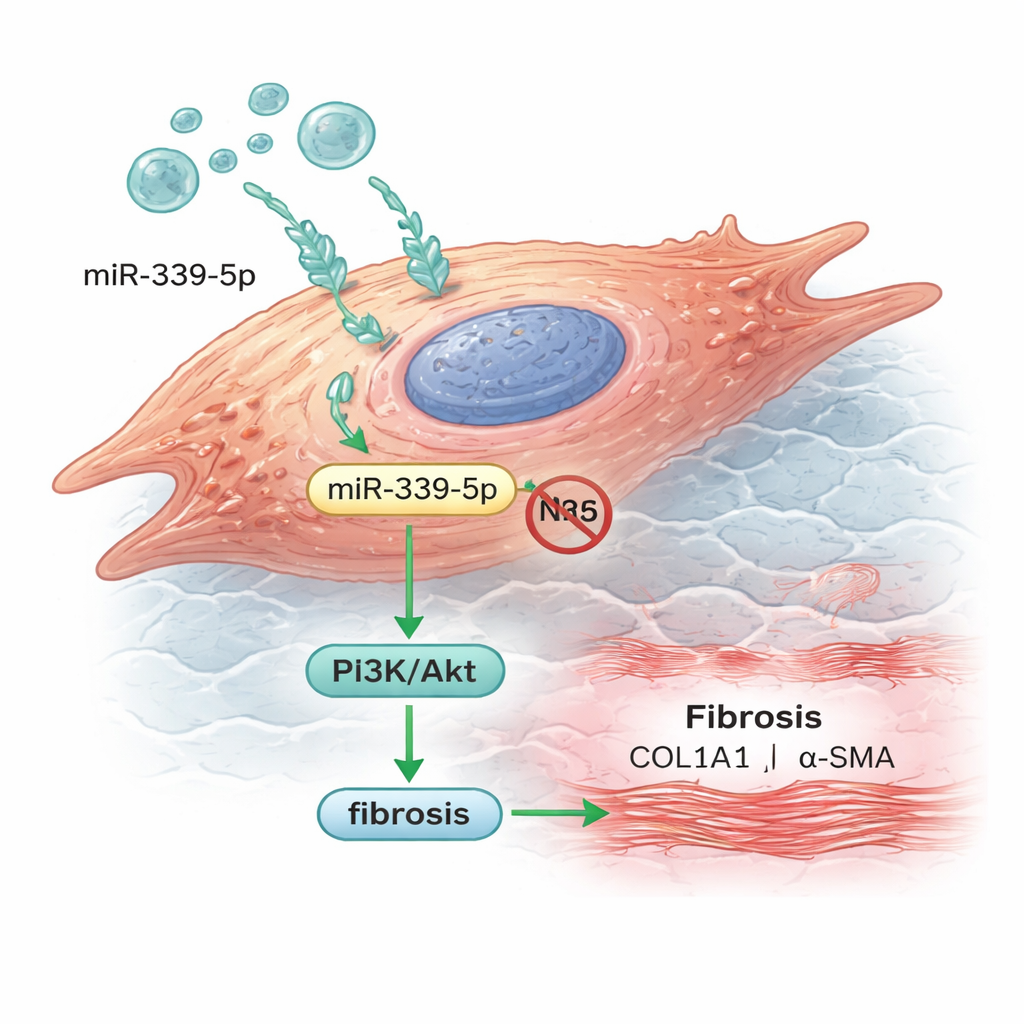
Da marcatore nel sangue a promotore di fibrosi
I ricercatori sono quindi passati a cellule di tipo cardiaco coltivate in laboratorio per osservare come si comporta questo microRNA nei tessuti. Hanno dimostrato che gli esosomi provenienti dai pazienti venivano prontamente assorbiti dai cardiomiociti umani, consegnando miR-339-5p nelle cellule. Quando hanno aumentato artificialmente miR-339-5p, i livelli di NLRC5 sono diminuiti e il pathway PI3K/Akt è diventato più attivo. Contemporaneamente le cellule hanno prodotto più collagene e una proteina chiamata actina alfa a livello muscolare liscio — entrambe caratteristiche tipiche del tessuto fibrotico e rigido anziché del muscolo sano e flessibile. Quando miR-339-5p è stato bloccato, questi cambiamenti sono stati invertiti, suggerendo che questo singolo microRNA contribuisce a spingere le cellule cardiache verso uno stato che favorisce la formazione di cicatrici.
Cosa significa per i pazienti e per le cure future
Mappando questa catena di eventi — dall'aumento di miR-339-5p negli esosomi plasmatici alla riduzione di NLRC5, dall'attivazione della segnalazione PI3K/Akt all'aumento delle proteine della fibrosi — lo studio collega un marcatore misurabile nel sangue a un meccanismo plausibile di danno all'interno del cuore. Per i pazienti, questo apre la possibilità che in futuro un esame del sangue di routine possa aiutare a rilevare il rimodellamento dannoso prima rispetto alle scansioni e ai marcatori di laboratorio attuali. Indica inoltre che farmaci progettati per ridurre miR-339-5p o ripristinare l'attività di NLRC5 potrebbero rallentare l'irrigidimento e la fibrosi che peggiorano progressivamente l'insufficienza cardiaca. Pur richiedendo studi più ampi e di lungo periodo, questi piccolissimi messaggeri di RNA potrebbero offrire sia una spia luminosa sul cruscotto sia un nuovo bersaglio sotto il cofano.
Citazione: Cheng, D., Hu, J., Zhao, M. et al. Plasma exosomal hsa-miR-339-5p is associated with NOD-like receptor family CARD domain-containing 5 in heart failure with reduced ejection fraction. Sci Rep 16, 5690 (2026). https://doi.org/10.1038/s41598-026-35519-0
Parole chiave: insufficienza cardiaca, esosomi, microRNA, fibrosi, biomarcatori