Clear Sky Science · it
Sviluppo supportato da dati strutturali e computazionali di analoghi 2,5-disostituiti-1,3,4-ossadiazolo come inibitori attivi di LOX, ureasi e α-glucosidasi
Nuovi strumenti chimici per affrontare malattie comuni
Molti problemi di salute quotidiani — dalle ulcere e calcoli renali al diabete e all’infiammazione cronica — sono guidati da enzimi iperattivi nel nostro organismo. Questo studio esplora una famiglia di piccole molecole recentemente progettate che agiscono come freni per tre di questi enzimi. Regolando le loro strutture e testandole in laboratorio e con strumenti computazionali, i ricercatori mirano a gettare le basi per farmaci più efficaci e sicuri in futuro. 
Perché questi enzimi sono importanti
Il gruppo si è concentrato su tre bersagli enzimatici che svolgono ruoli molto diversi ma ugualmente rilevanti per la salute. L’ureasi aiuta a degradare l’urea; quando è iperattiva in alcuni batteri o tessuti può contribuire a ulcere gastriche e delle vie urinarie, alla formazione di calcoli renali e persino a ipertensione. L’alfa-glucosidasi si trova sulla superficie delle cellule intestinali e scompone i carboidrati complessi in glucosio; bloccarla è una strategia consolidata per controllare la glicemia nel diabete di tipo 2. La lipossigenasi (LOX) converte i lipidi in molecole segnale che guidano l’infiammazione, l’asma e alcuni processi legati al cancro. Di conseguenza, sono molto ricercati farmaci che modulino questi enzimi senza danneggiare altri sistemi.
Costruire una libreria di molecole candidate
Per cercare tali farmaci, i ricercatori hanno sintetizzato una serie di 15 composti correlati basati su un sistema ad anello chiamato 1,3,4-ossadiazolo connesso a un’unità piperidinica. Questo impalcatura chimica compare già in diversi farmaci moderni ed è nota per interagire favorevolmente con bersagli biologici. Il gruppo ha variato le “decorazioni” attaccate a questo nucleo — piccoli gruppi come metile, etile, metossile, benzile e cicloesile — in posizioni diverse, creando una piccola libreria di candidati etichettati da 7a a 7o. Hanno confermato ciascuna struttura usando strumenti analitici standard come spettroscopia infrarossa e risonanza magnetica nucleare, assicurandosi che ciò che avevano ottenuto corrispondesse ai progetti.
Valutare quanto bene le molecole bloccano gli enzimi
Ciascun composto è stato poi testato contro LOX, ureasi e alfa-glucosidasi purificati per valutare quanto potesse rallentare l’attività enzimatica. Diverse molecole sono emerse come particolarmente promettenti. Contro l’alfa-glucosidasi, i composti 7a e 7n si sono rivelati molto efficaci, superando il farmaco standard per il diabete acarbosio nei test in vitro raggiungendo alte percentuali di inibizione a basse concentrazioni micromolari. Per la LOX, i composti 7a, 7h e 7n hanno mostrato attività molto forte, in alcuni casi migliore rispetto all’inibitore di riferimento naturale quercetina. Nei saggi sull’ureasi, i composti 7a e in particolare 7l hanno eguagliato o leggermente superato l’inibitore standard tiourea, suggerendo che potrebbero un giorno fungere da capostipiti per terapie anti-ulcera o anti-calcoli. 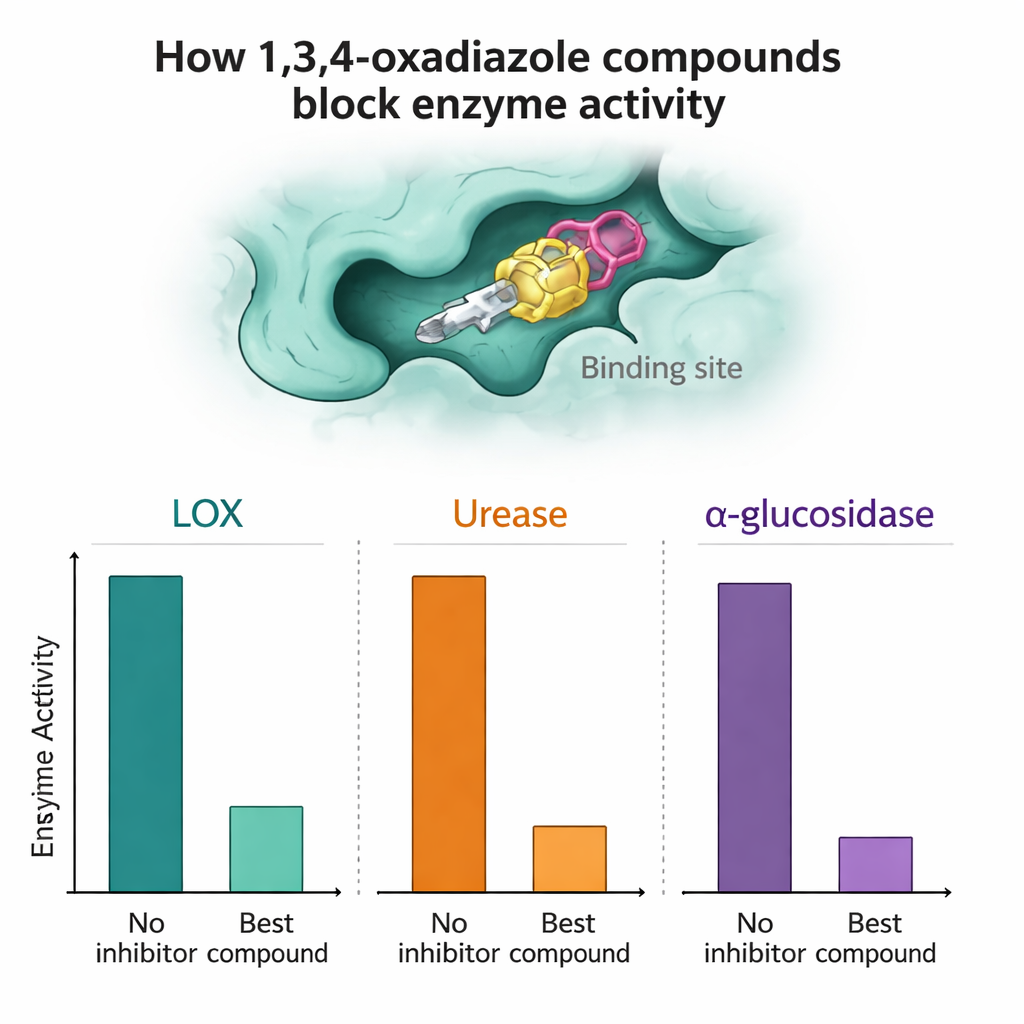
Collegare la struttura alla performance
Poiché le uniche differenze tra i composti 7a–7o sono piccole modifiche attorno al sistema ad anello centrale, i ricercatori hanno potuto cominciare a delineare semplici relazioni struttura–attività. Per esempio, l’aggiunta di piccoli gruppi ricchi di carbonio in certe posizioni “orto” su un anello attaccato spesso aumentava la capacità di bloccare l’alfa-glucosidasi o la LOX. Altre sostituzioni, come specifici gruppi metossile o estere posizionati in modo meno favorevole, tendevano a indebolire l’attività. Per capire il perché, il team ha impiegato simulazioni al computer. Calcoli quantomeccanici hanno mostrato che tutte le molecole erano termodinamicamente stabili e sufficientemente flessibili da adattarsi alle tasche enzimatiche. Studi di docking — l’adattamento virtuale di ciascuna molecola nei modelli tridimensionali degli enzimi — hanno rivelato che i composti più attivi stabilivano contatti più stretti tramite una combinazione di legami a idrogeno e interazioni idrofobiche nei punti chiave dei siti attivi, mentre i candidati meno efficaci si inserivano meno saldamente o mancavano punti di contatto critici.
Cosa significa per i futuri farmaci
In termini pratici, lo studio identifica una manciata di “chiavi” promettenti che si adattano bene a tre “serrature” legate a malattie e comincia a spiegare, a livello atomico, perché alcune chiavi funzionano meglio di altre. Nessuna di queste molecole è ancora pronta per diventare un farmaco — necessitano di test di sicurezza, ottimizzazione del comportamento nell’organismo e studi su animali e successivamente sull’uomo. Tuttavia, il lavoro dimostra che lo schema 1,3,4-ossadiazolo–piperidina è un punto di partenza fertile per futuri trattamenti mirati al diabete, a condizioni infiammatorie e ai disturbi correlati all’ureasi. La combinazione di misure di laboratorio accurate con modellizzazione computazionale dettagliata fornisce una tabella di marcia per affinare questi candidati in farmaci più precisi ed efficaci.
Citazione: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Parole chiave: inibitori enzimatici, scoperta di farmaci, composti ossadiazolici, diabete e infiammazione, ureasi e lipossigenasi