Clear Sky Science · it
SHP2 promuove l’osteosarcoma regolando la via STAT3/TET3/HOXB2
Perché questo studio sul cancro osseo è importante
L’osteosarcoma è il tumore osseo primario più comune nei bambini e negli adolescenti e, nonostante la chemioterapia moderna e la chirurgia, la sopravvivenza nei pazienti con malattia avanzata o recidivante è migliorata pochissimo nel corso dei decenni. Questo studio esplora l’architettura interna delle cellule di osteosarcoma per identificare quali molecole agiscono come “interruttori principali” che favoriscono la crescita, la diffusione e la resistenza al trattamento del tumore. Scoprendo una via di controllo chiave incentrata su una proteina chiamata SHP2, il lavoro indica nuovi bersagli farmacologici che potrebbero un giorno rendere le terapie per l’osteosarcoma più efficaci e più precise.
Seguire gli indizi nell’attività genica del tumore
I ricercatori hanno iniziato trattando l’osteosarcoma come un problema di dati. Hanno analizzato set di espressione genica pubblici confrontando campioni tumorali con tessuto osseo normale, quindi hanno usato strumenti statistici per individuare geni costantemente sovra- o sottoespressi nel cancro. Centinaia di geni risultavano diversi, e molti di questi si raggruppavano in note vie oncogeniche che guidano crescita cellulare, sopravvivenza e migrazione. Tra questi, una proteina, SHP2, è emersa come snodo fortemente collegato ad altri fattori: il fattore di segnalazione STAT3, l’enzima che modifica il DNA TET3 e il regolatore dello sviluppo HOXB2. Ciò suggeriva che queste molecole potessero formare una catena connessa che aiuta le cellule di osteosarcoma a comportarsi in modo aggressivo. 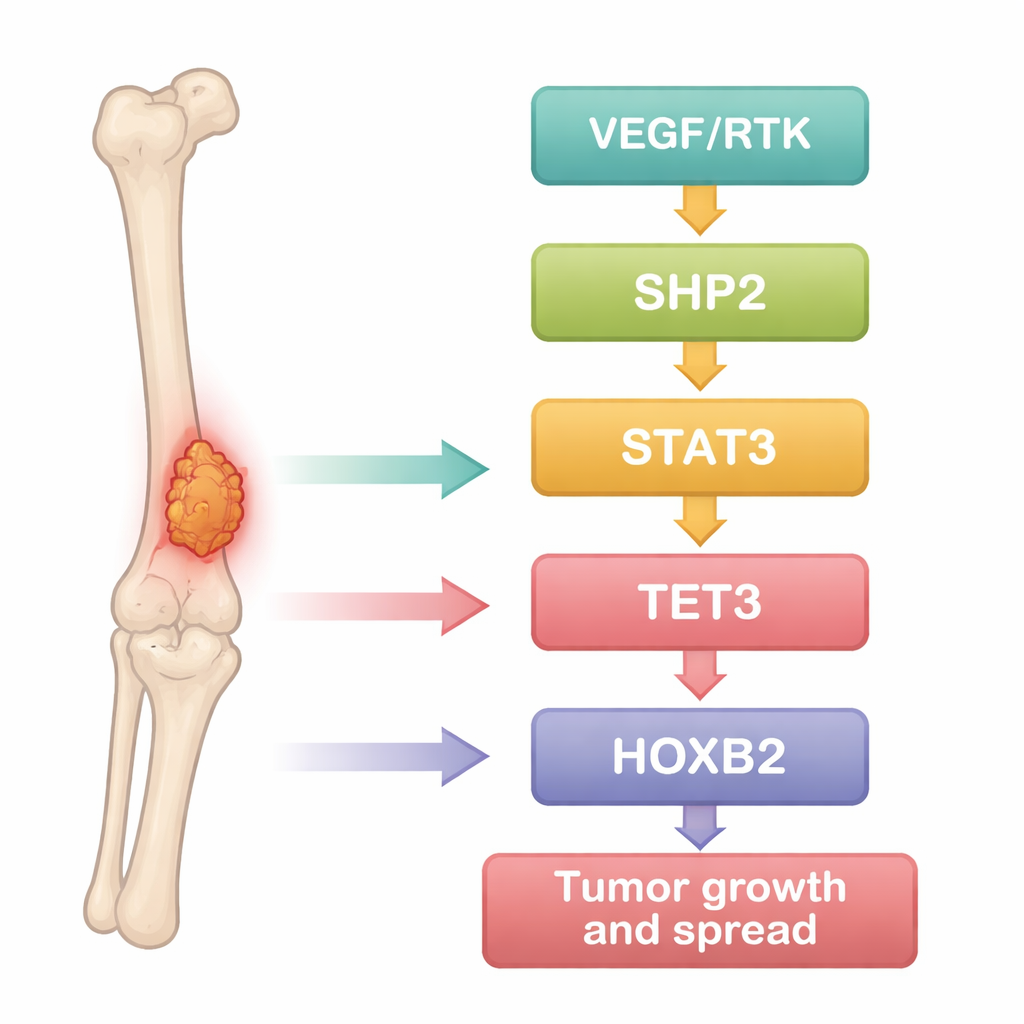
Mettere alla prova il ruolo di SHP2 nelle cellule tumorali
Per andare oltre le correlazioni, il team ha ingegnerizzato linee cellulari umane di osteosarcoma (143B e MG63) per ridurre o aumentare SHP2. Quando SHP2 è stato silenziato, la capacità delle cellule di proliferare, migrare su una superficie e invadere attraverso una membrana è diminuita in modo significativo. Anche i livelli delle proteine STAT3, TET3 e HOXB2, così come marcatori associati al cancro come c-Myc, NANOG e NUSAP1, sono calati. Quando STAT3 è stato riattivato o HOXB2 sovraespresso, molti di questi effetti sono stati invertiti, indicando che SHP2 si pone a monte di una catena che infine influisce sui geni che controllano la divisione cellulare, i tratti simili alle cellule staminali e il macchinario della mitosi.
Costruire un percorso oncogenico passo dopo passo
Assemblando gli esperimenti, gli autori descrivono un modello graduale. Nell’ambiente tumorale, alti livelli di fattore di crescita endoteliale vascolare (VEGF) stimolano le tirosin chinasi recettoriali (RTK) sulla superficie cellulare. Queste, a loro volta, attivano SHP2 all’interno della cellula. SHP2 attivo accende STAT3, un fattore di trascrizione che si sposta nel nucleo e aumenta la produzione di TET3. TET3 modifica poi i marcatori chimici sul DNA, rimuovendo specificamente gruppi metile nella regione del gene HOXB2. Questa demetilazione agisce come la rimozione di un freno, permettendo una maggiore espressione di HOXB2. HOXB2, un gene che normalmente guida lo sviluppo, potenzia ora l’attività di c-Myc, NANOG e NUSAP1, che insieme alimentano la crescita inarrestabile delle cellule tumorali, aumentano il comportamento invasivo e supportano tratti associati alle metastasi.
Dal piatto di coltura agli animali vivi
Per verificare se questa via avesse rilevanza nei tumori interi, gli scienziati hanno impiantato sotto la pelle dei topi cellule di osteosarcoma modificate. I tumori derivati da cellule che sovraproducevano SHP2 sono cresciuti più grandi e più pesanti rispetto ai controlli. Quando TET3 è stato silenziato in queste cellule ricche di SHP2, la crescita tumorale è rallentata e i livelli di HOXB2 sono diminuiti, anche se SHP2 e STAT3 restavano attivi. La reintroduzione di HOXB2 ha ripristinato la vigoria del tumore. In tutto lo studio, le misurazioni dei livelli proteici nei tessuti tumorali rispecchiavano i risultati ottenuti in coltura cellulare, rafforzando l’idea che SHP2, STAT3, TET3 e HOXB2 agiscano come un asse collegato che spinge l’osteosarcoma verso comportamenti più maligni. 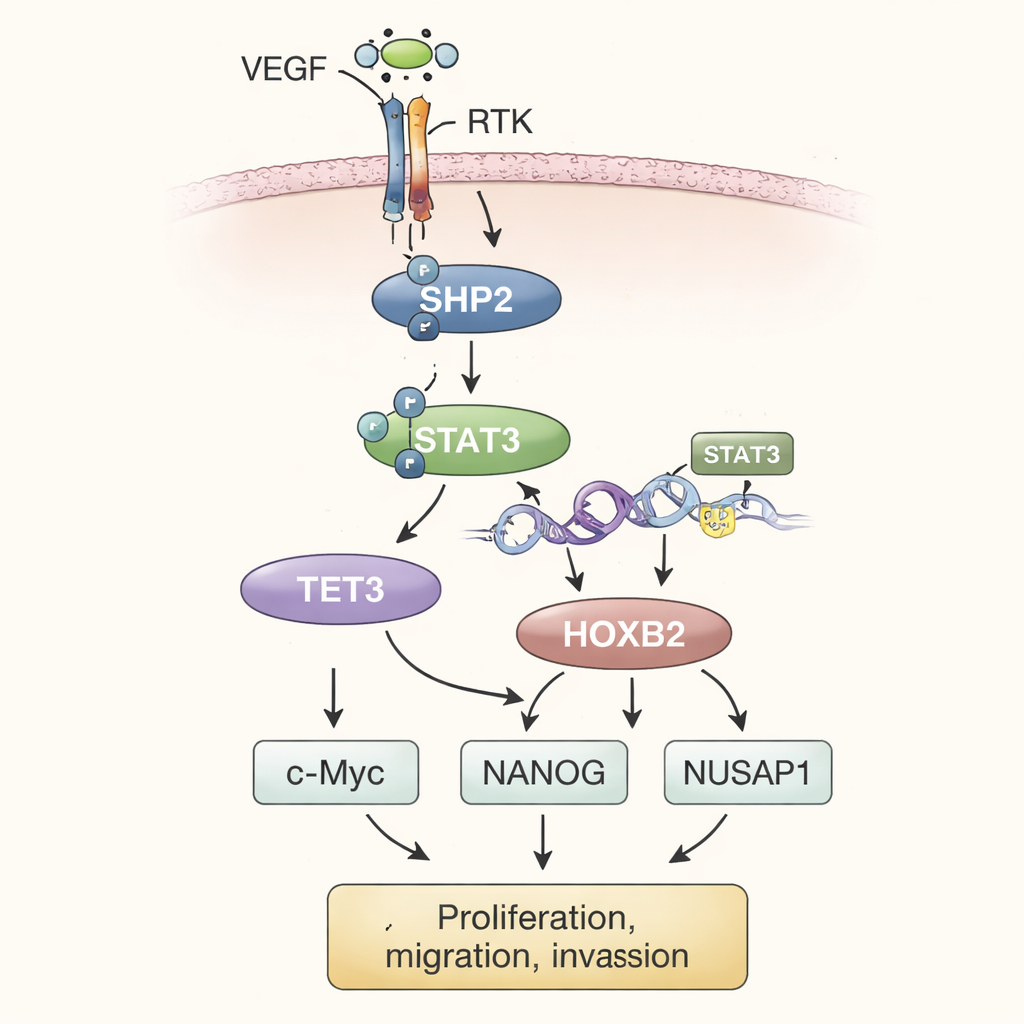
Cosa significa per i trattamenti futuri
Per il lettore non specialista, il messaggio principale è che i ricercatori hanno tracciato una catena di segnale chiara — dal VEGF e i suoi recettori di superficie, attraverso SHP2 e STAT3, fino a TET3, HOXB2 e vari geni di crescita potenti — che aiuta a spiegare perché l’osteosarcoma può crescere rapidamente e diffondersi precocemente. Poiché SHP2 e STAT3 sono enzimi che, in linea di principio, possono essere bloccati da piccoli farmaci molecolari, e TET3 e HOXB2 rappresentano fasi successive nella stessa via, questo percorso offre più punti dove le terapie future potrebbero intervenire. Pur essendo uno studio condotto in linee cellulari e in modelli murini, fornisce una mappa dettagliata che gli sviluppatori di farmaci possono utilizzare per progettare trattamenti combinati mirati a spegnere gli interruttori di controllo centrali del tumore anziché limitarsi ad attaccarne gli esiti finali.
Citazione: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Parole chiave: osteosarcoma, SHP2, via STAT3, segnalazione tumorale, terapia mirata