Clear Sky Science · it
Progettazione e valutazione immunoinformatiche di un vaccino multi-epitopo contro Vibrio fluvialis
Perché un nuovo vaccino è importante per gli amanti dei frutti di mare
Vibrio fluvialis è un parente meno noto dei batteri che causano il colera: vive nelle acque costiere calde e può contaminare frutti di mare e acqua potabile. Provoca diarrea grave e infezioni intestinali e sta diventando più comune con il riscaldamento degli oceani e la perdita di efficacia degli antibiotici. Tuttavia attualmente non esiste alcun vaccino per le persone. Questo studio usa metodi computazionali avanzati per progettare un nuovo tipo di vaccino sperimentale, costruito a partire da frammenti selezionati del batterio, con l’obiettivo a lungo termine di proteggere chi è esposto tramite cibo, acqua o inondazioni dovute al cambiamento climatico.

Da una minaccia nascosta a un bersaglio chiaro
Vibrio fluvialis è spesso stato scambiato per altre specie di Vibrio, il che significa che il suo ruolo nelle malattie trasmesse dagli alimenti è probabilmente sottostimato. Focolai sono stati collegati a frutti di mare contaminati e acque inquinate, e tempeste e inondazioni recenti hanno portato questi batteri verso l’interno, facendo ammalare persone lontane dalla costa. Molti pazienti richiedono cure ospedaliere e un numero preoccupante di ceppi resiste ormai a più antibiotici. Poiché la superficie del microrganismo assomiglia a quella di batteri correlati, i medici possono diagnosticare erroneamente le infezioni, ritardando il trattamento appropriato. Tutto ciò crea una forte necessità di prevenzione, anziché fare affidamento solo sui farmaci.
Progettare un vaccino all’interno di un computer
Invece di coltivare l’intero batterio in laboratorio, i ricercatori si sono rivolti all’“immunoinformatica” — l’uso di software per prevedere quali piccoli pezzi di Vibrio fluvialis siano più probabilmente riconosciuti e attaccati dal sistema immunitario umano. Si sono concentrati su due proteine di membrana che si trovano sulla superficie del batterio e sono importanti per la sua sopravvivenza e per la capacità di causare malattia. Da queste proteine il team ha estratto dieci brevi segmenti, chiamati epitopi, che possono essere riconosciuti sia dalle cellule T sia dalle cellule B, i principali elementi della difesa immunitaria. Hanno poi cucito insieme questi pezzi in una singola catena di 246 amminoacidi, aggiungendo brevi segmenti spaziatori affinché il sistema immunitario possa processare ogni pezzo correttamente, e un frammento adiuvante per potenziare la risposta complessiva.
Verificare forza, sicurezza e portata globale
Una volta costruito il vaccino virtuale, il team ha eseguito una serie di test interamente in silico, cioè al computer piuttosto che su animali o persone. I programmi hanno previsto che il costrutto combinato sarebbe fortemente “visibile” al sistema immunitario ma improbabile che scatenasse allergie o tossicità. Gli epitopi scelti corrispondevano a varianti comuni dei geni immunitari a livello mondiale, suggerendo che circa il 99,97 percento della popolazione globale dovrebbe essere in grado di rispondere, incluse persone in regioni fortemente colpite come il Sud e l’Est asiatico. La proteina vaccinale è risultata anche stabile, sufficientemente idrofila da dissolversi bene, e adatta alla produzione efficiente in batteri da laboratorio standard, rendendo più praticabile una futura fabbricazione.
Come il vaccino potrebbe innescare la protezione
I ricercatori si sono poi chiesti se la proteina progettata potesse plausibilmente interagire con un sensore immunitario reale. Utilizzando strumenti moderni di predizione strutturale, hanno costruito un modello tridimensionale del vaccino e poi simulato come questo potesse legarsi al recettore Toll‑like 2 (TLR2), una molecola presente sulle cellule immunitarie che riconosce componenti batterici. Il docking computazionale ha suggerito un accoppiamento stretto tra vaccino e TLR2, sostenuto da molti contatti molecolari stabilizzanti. Lunghe simulazioni dinamiche dettagliate per 100 nanosecondi hanno indicato che la coppia vaccino‑recettore rimaneva stabile e compatta nel tempo. Ulteriori simulazioni del sistema immunitario hanno predetto forti ondate di anticorpi e attività delle cellule T, insieme alla formazione di cellule della memoria che, in linea di principio, potrebbero fornire una protezione duratura contro Vibrio fluvialis.
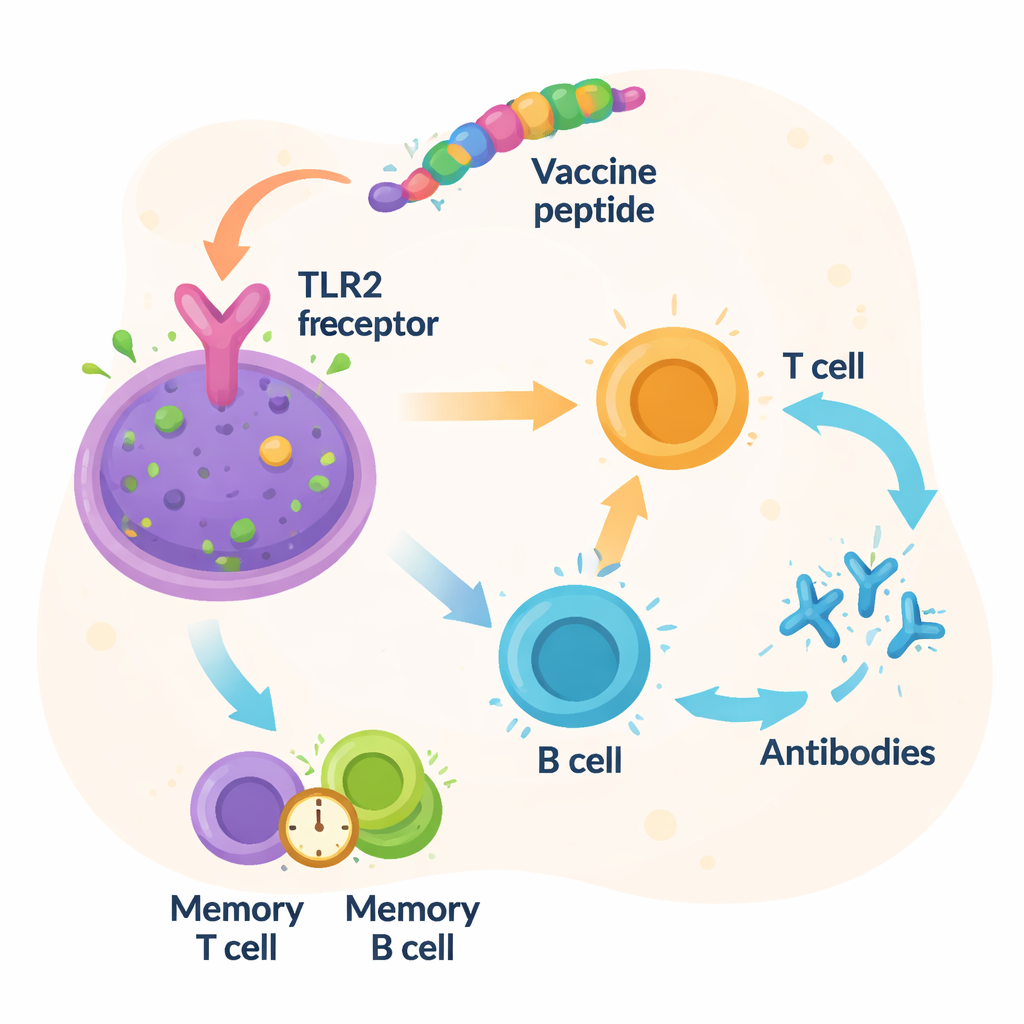
Da un progetto digitale a uno scudo nel mondo reale
In termini pratici, questo lavoro offre un “progetto” digitale per un futuro vaccino contro Vibrio fluvialis costruito solo con i frammenti più importanti del batterio, organizzati per essere ampiamente efficaci e potenzialmente più sicuri dei vaccini a cellule intere. Lo studio mostra che questo costrutto dovrebbe essere riconoscibile dalla maggior parte dei sistemi immunitari umani, legarsi bene a un sensore immunitario chiave e poter essere prodotto con strumenti standard. Tuttavia, tutti questi risultati derivano da modelli al computer. I passaggi successivi richiederanno la produzione del vaccino in laboratorio, test in colture cellulari e animali e infine studi clinici sull’uomo per confermare che protegga realmente dall’infezione senza causare danni. Se tali test avranno successo, vaccini multi‑epitopo di questo tipo potrebbero diventare potenti nuovi strumenti contro i batteri trasmessi dagli alimenti in un mondo che si scalda e si urbanizza sempre di più.
Citazione: Naveed, M., Husnain, M., Aziz, T. et al. Immunoinformatics-based design and evaluation of a multi-epitope vaccine against Vibrio fluvialis. Sci Rep 16, 4100 (2026). https://doi.org/10.1038/s41598-026-35434-4
Parole chiave: Vibrio fluvialis, vaccino multi-epitopo, infezione alimentare, immunoinformatica, resistenza agli antibiotici