Clear Sky Science · it
Sviluppo di un sistema di screening globale per rilevare interazioni proteina–proteina mediante completamento di luminescenza in lievito fissione
Illuminare la vita nascosta delle proteine
Ogni battito cardiaco, pensiero e respiro nel nostro corpo dipende dal fatto che le proteine si associno all’interno delle cellule. Queste piccole collaborazioni, chiamate interazioni proteina–proteina, controllano tutto, da come vengono letti i geni a come le cellule rispondono allo stress. Molte di queste associazioni però sono fugaci o delicate, il che le rende difficili da rilevare con gli strumenti attuali. Questo studio descrive un nuovo sistema di screening “a luce” altamente sensibile, costruito in un semplice organismo modello, il lievito fissione, per svelare migliaia di connessioni proteiche nascoste in una sola volta.
Perché le partnership proteiche sono così difficili da vedere
Le proteine raramente lavorano da sole. Si legano a partner diversi in momenti diversi, talvolta solo per brevi istanti, e il loro comportamento può essere alterato da modifiche chimiche o dalla loro posizione nella cellula. I metodi tradizionali per studiare queste interazioni o estraggono le proteine dal loro ambiente naturale o si basano su stratagemmi genetici che non catturano ogni associazione. Di conseguenza, le mappe esistenti di chi interagisce con chi nella cellula sono incomplete. Gli autori si sono posti l’obiettivo di migliorare questo quadro creando un sistema più flessibile e sensibile in grado di sondare quasi tutte le proteine del lievito fissione in cellule vive.
Trasformare il contatto in luce
Al centro del nuovo approccio c’è un enzima divisibile che emette luce. Una parte, chiamata LgBiT, è collegata a una proteina “esca” che i ricercatori vogliono studiare. L’altra parte, SmBiT, è collegata a molti possibili partner “preda”, uno per ciascun ceppo di lievito. Da sole, queste due porzioni di enzima interagiscono pochissimo. Ma quando proteina esca e preda si legano all’interno della cellula, i due frammenti si riuniscono, ricostituendo un enzima funzionante che brilla in presenza di un combustibile chimico. Misurando quanta luce produce ciascun ceppo, il team può capire quali proteine si incontrano realmente nella cellula e quanto forte è la loro interazione. Per evitare di perdere partner perché il marcatore blocca la funzione normale, la proteina esca è prodotta in due versioni, con LgBiT attaccato a uno o all’altro estremo, aumentando notevolmente le probabilità che almeno un’orientazione funzioni. 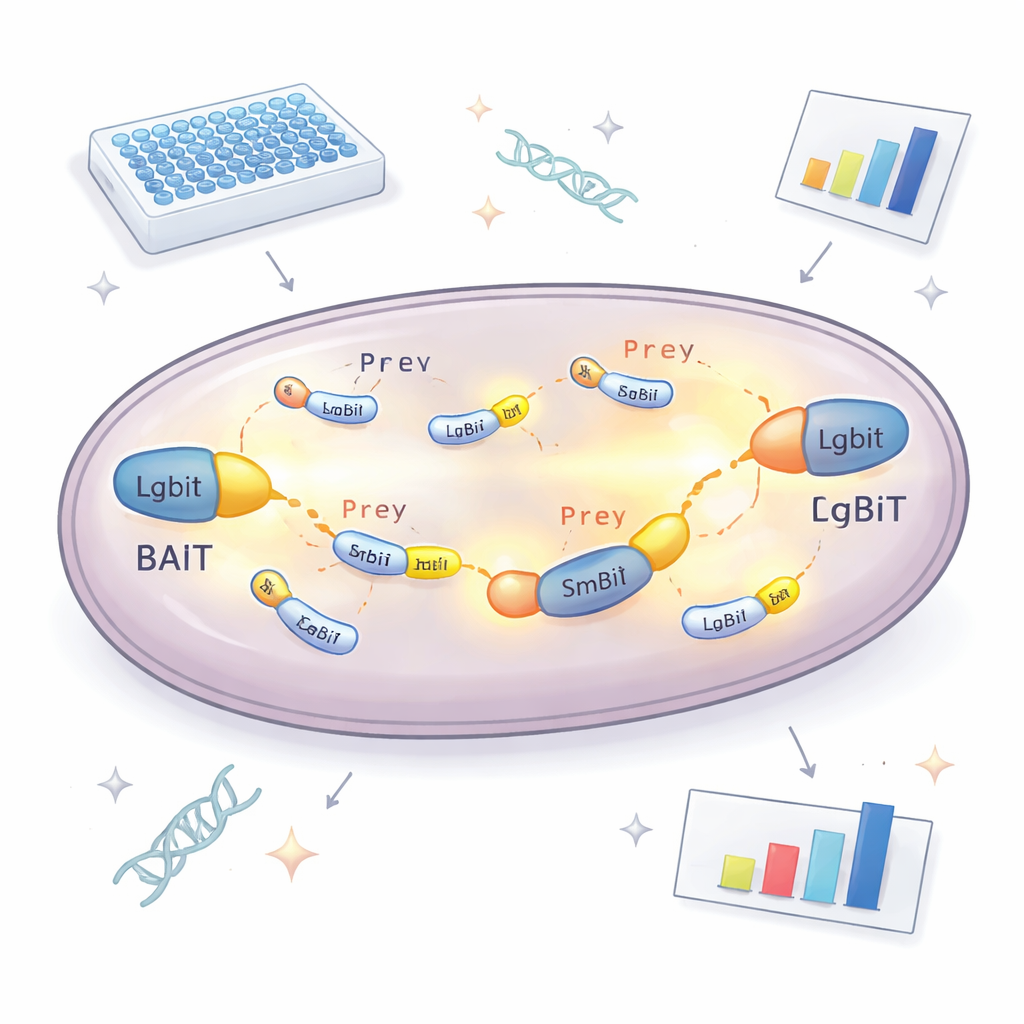
Progettare una libreria di lieviti e un sistema di ceppi
Costruire questa piattaforma ha richiesto più di un enzima intelligente. I ricercatori hanno dovuto anche introdurre migliaia di proteine preda nel lievito in modo controllato e a copia singola. Hanno progettato un vettore di DNA speciale per le proteine preda che si inserisce in un punto definito del genoma del lievito e porta un marcatore fluorescente rosso. L’intensità di questo segnale rosso riflette il numero di copie inserite, permettendo al team di selezionare facilmente colonie con esattamente una copia, essenziale per confronti affidabili. Hanno inoltre creato vettori dedicati per l’esca che posizionano LgBiT all’inizio o alla fine della proteina esca, separato da link flessibili in modo che la proteina possa ancora ripiegarsi e muoversi normalmente. Ceppi di lievito attentamente ingegnerizzati sono stati poi costruiti per ospitare due costrutti di esca e un costrutto di preda contemporaneamente, utilizzando marcatori nutrizionali per garantire che sopravvivano solo le cellule correttamente combinate.
Mettere il sistema alla prova
Per verificare se il loro progetto migliorasse davvero il rilevamento, gli scienziati hanno prima esaminato proteine con partner ben noti. Hanno confermato che l’intensità del segnale dipendeva fortemente da dove era attaccato il marcatore luminoso: alcune interazioni comparivano solo quando LgBiT era su un estremità dell’esca e non sull’altra. L’espressione simultanea di entrambe le versioni ha aumentato l’emissione luminosa, dimostrando che la strategia a doppia esca facilita l’individuazione di interazioni deboli o sensibili all’orientamento. Il sistema ha inoltre rilevato contatti che coinvolgono proteine legate alle membrane, una classe notoriamente difficile per i metodi tradizionali di lievito two-hybrid. Con questa validazione, il team è passato a uno screening a livello genomico, usando come esca una proteina correlata alla trascrizione chiamata Tfs1. Screenando oltre 4.600 proteine preda, hanno trovato 31 candidati forti, inclusi diversi partner già noti e molti nuovi, alcuni localizzati fuori dal nucleo in aree come i mitocondri e la superficie cellulare. 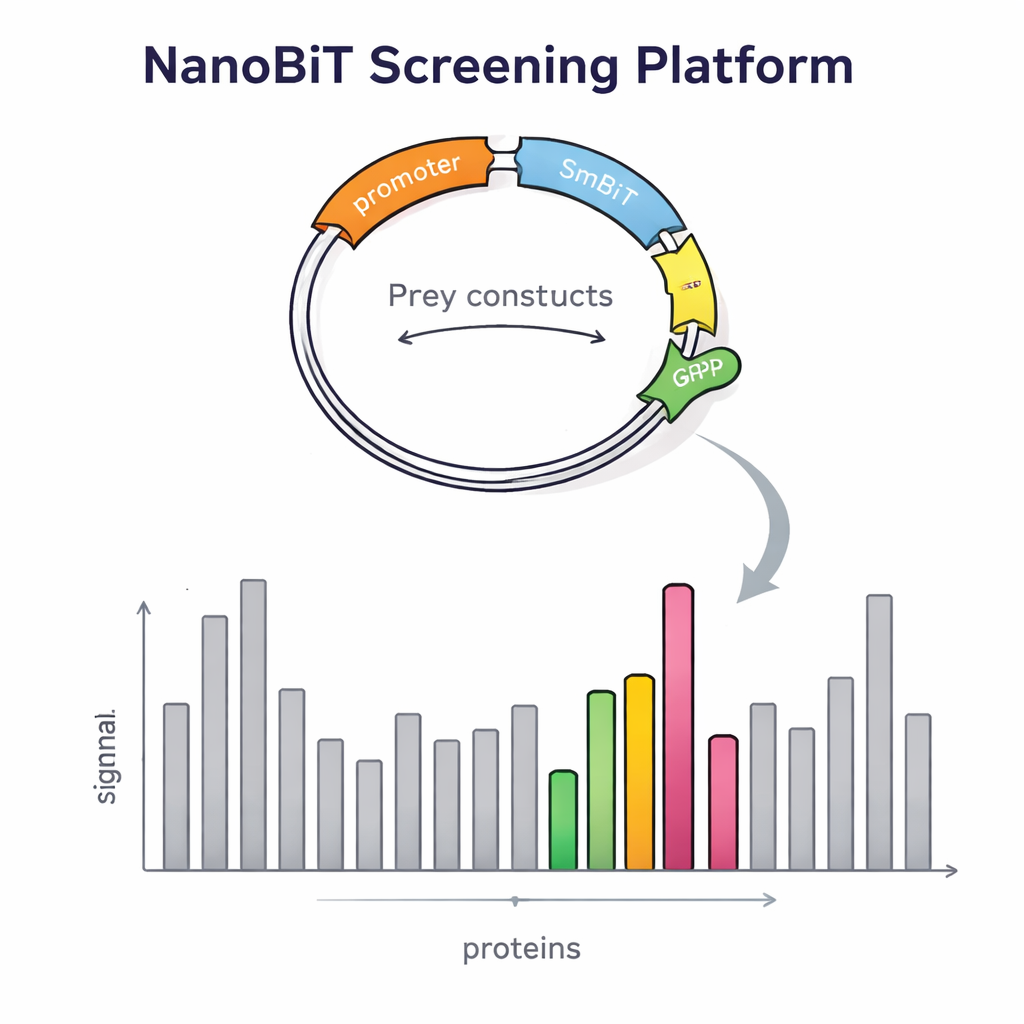
Cosa significa per la biologia e la scoperta di farmaci
Per un non specialista, il messaggio chiave è che gli autori hanno costruito un “radar di interazioni” più sensibile all’interno delle cellule di lievito. Convertendo brevi strette di mano proteiche in lampi di luce misurabili e disponendo ingegnosamente la genetica in modo che tre proteine marcate possano essere espresse insieme, il loro sistema scopre sia partner noti sia partner precedentemente invisibili. Pur essendo necessari ulteriori controlli con altre tecniche per confermare ciascuna nuova associazione, questa piattaforma colma importanti lacune nelle nostre mappe delle reti cellulari. Poiché i ceppi sono stati anche ingegnerizzati per essere più sensibili a piccole molecole, lo stesso setup potrebbe essere adattato per cercare composti che interrompono partnership proteiche dannose o stabilizzano quelle benefiche, offrendo un nuovo e potente strumento sia per la biologia di base sia per le fasi iniziali della scoperta di farmaci.
Citazione: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Parole chiave: interazioni proteiche, lievito fissione, saggio di luminescenza, screening ad alta produttività, strumenti per la scoperta di farmaci