Clear Sky Science · it
Secretoma dipendente dalla particella di riconoscimento del segnale nell’uomo
Come le cellule decidono quali proteine lasciano la cellula
Le nostre cellule spediscono costantemente proteine che formano ormoni, anticorpi e l’impalcatura tra i tessuti. Ma non tutte le proteine sono destinate a viaggiare. Questo studio affronta una domanda fondamentale ancora in parte irrisolta: come decidono le cellule umane quali proteine si affidano a un aiuto chiave chiamato particella di riconoscimento del segnale (SRP) per raggiungere il centro di smistamento interno della cellula e quali invece possono arrivarci senza di essa? Mappando questa decisione su migliaia di proteine contemporaneamente, gli autori rivelano chi dipende dall’SRP, chi non ne ha bisogno e cosa accade quando questo sistema si guasta — un argomento rilevante per molte malattie legate a proteine secrete mal instradate o mancanti.
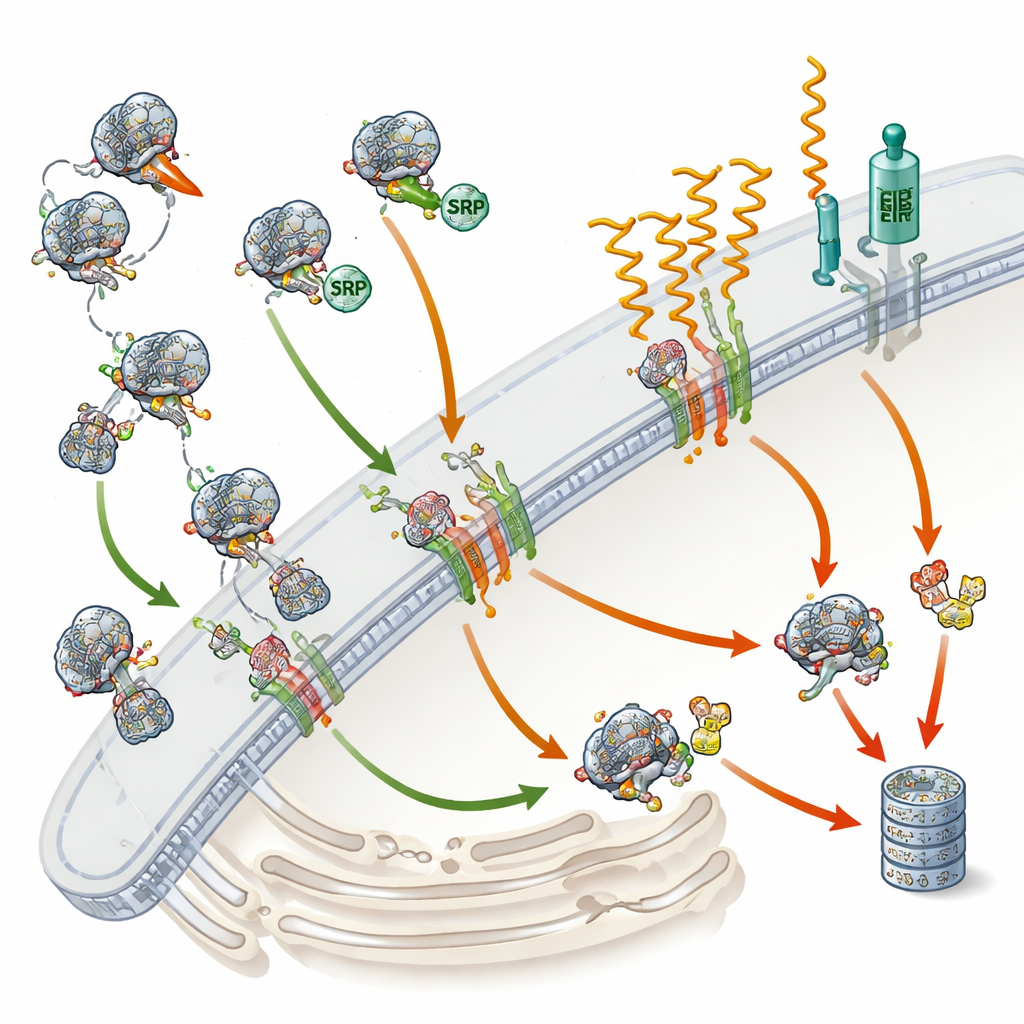
Il molo di spedizione della cellula e la sua guida principale
Circa una proteina su tre nell’uomo è destinata alla superficie cellulare, alle membrane o al rilascio all’esterno della cellula. Per raggiungere il posto giusto, la maggior parte di queste proteine deve prima entrare in una rete di membrane interne chiamata reticolo endoplasmatico, il molo di spedizione della cellula. L’SRP funge da guida: riconosce un piccolo “etichetta d’indirizzo” all’inizio delle proteine neoformate e ne sospende temporaneamente la sintesi. Questa pausa dà al ribosoma — la macchina che produce le proteine — il tempo di agganciarsi al reticolo endoplasmatico, dove la produzione riprende e la proteina in crescita viene infilata nella membrana o attraverso di essa. Alcune proteine, tuttavia, usano rotte alternative che non richiedono l’SRP, specialmente proteine molto piccole o quelle ancorate all’estremità terminale. Fino a oggi, gli scienziati non sapevano, su scala globale, quali proteine umane richiedono realmente l’SRP e quali possono aggirarlo.
Ridurre l’SRP per vedere cosa si rompe
Per rispondere, i ricercatori hanno ridotto selettivamente i livelli di un componente essenziale dell’SRP, SRP54, in cellule HeLa umane. Hanno poi usato una tecnica sensibile chiamata spettrometria di massa per misurare oltre 6.000 proteine all’interno delle cellule e quasi 2.000 proteine presenti nel liquido circostante, noto come mezzo condizionato. Confrontando cellule con SRP54 normale e cellule con SRP54 ridotto hanno potuto vedere quali proteine diminuiscono, quali aumentano e quali rimangono invariate. Un forte calo nel livello di una proteina — soprattutto sia all’interno della cellula sia nel mezzo — è stato interpretato come segno che quella proteina dipende dall’SRP per essere prodotta e instradata correttamente.
Chi dipende dall’SRP e chi se la cava senza
L’analisi ha mostrato che la maggior parte delle proteine normalmente secrete nel mezzo dipende chiaramente dall’SRP. Quando SRP54 è stato ridotto, la maggioranza di queste proteine secrete, in particolare quelle che portano una classica etichetta di segnale, è diminuita bruscamente. Molte proteine di membrana all’interno della cellula sono anch’esse diminuite, rivelandole come clienti dell’SRP. Un insieme più piccolo di proteine con etichette simili è rimasto in gran parte non influenzato, segnalandole come indipendenti dall’SRP; queste probabilmente usano rotte alternative per raggiungere il reticolo endoplasmatico. I ricercatori hanno anche scoperto che specifiche caratteristiche dell’etichetta di segnale — come una regione carica positivamente all’inizio — erano più comuni tra le proteine dipendenti dall’SRP, suggerendo regole sottili che aiutano l’SRP a scegliere il suo carico. Allo stesso tempo, alcune proteine coinvolte nel marcare le proteine danneggiate per la distruzione e nella funzione mitocondriale sono aumentate, suggerendo che le cellule attivano sistemi di riserva e la produzione di energia quando la loro guida principale allo smistamento viene compromessa.
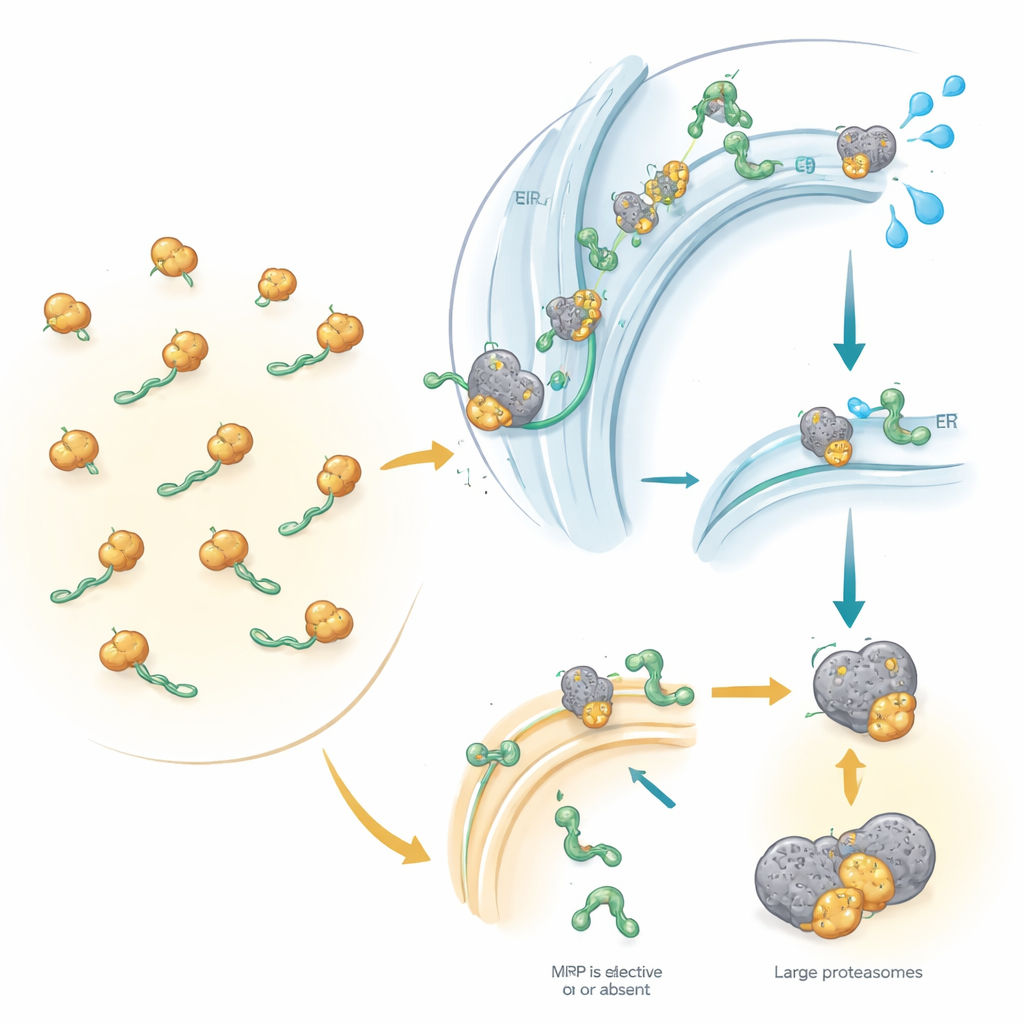
Controllo qualità quando il targeting fallisce
Lo studio è andato oltre il conteggio delle proteine: ha confrontato questi cambiamenti con le variazioni nell’RNA messaggero, i progetti usati per creare le proteine. Molte proteine dipendenti dall’SRP hanno perso non solo la proteina ma anche il relativo RNA, implicando una via di controllo qualità nota come RAPP. Quando l’SRP non riesce a ingaggiare correttamente una proteina secretoria o di membrana in formazione, questa via sembra innescare la degradazione dell’RNA corrispondente, impedendo la produzione di una proteina mal instradata. Allo stesso tempo, le proteine incompiute che non raggiungono il reticolo endoplasmatico vengono probabilmente marcate con piccole bandiere molecolari e indirizzate ai “tritacarne” cellulari chiamati proteasomi. È interessante notare che le classiche vie di stress del reticolo endoplasmatico non sono risultate fortemente attivate, suggerendo che il difetto dell’SRP provoca un tipo distinto di risposta di stress cellulare.
Che cosa significa per la salute e la malattia
Mappando, per la prima volta in cellule umane, quali proteine secrete e di membrana sono dipendenti dall’SRP e quali indipendenti, questo lavoro fornisce una mappa di riferimento delle regole di smistamento cellulare. I risultati mostrano che la maggior parte delle proteine esportate dipende davvero dall’SRP e che, quando l’SRP viene meno, le cellule rispondono degradando sia le proteine sia i loro progetti e attivando meccanismi alternativi di adattamento. Poiché molte mutazioni che causano malattie interessano le “etichetta d’indirizzo” delle proteine secrete, comprendere esattamente come l’SRP riconosce i suoi clienti e come la RAPP elimina quelli difettosi potrebbe aiutare a spiegare perché certe mutazioni portano a carenze ormonali, problemi immunitari o neurodegenerazione — e potrebbe infine indicare nuovi modi per ritoccare l’instradamento delle proteine nella salute umana.
Citazione: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Parole chiave: secrezione proteica, particella di riconoscimento del segnale, secretoma, controllo qualità delle proteine, reticolo endoplasmatico