Clear Sky Science · it
Inibizione sequenziale di platino e PARP potenzia l’efficacia dell’immunoterapia anti‑PD1 nel cancro pancreatico murino con mutazione BRCA2
Perché questa ricerca conta per i pazienti
Il cancro pancreatico è uno dei tumori più letali e, anche quando i medici identificano una vulnerabilità sfruttabile—come una mutazione nel gene BRCA2—le terapie attuali raramente tengono la malattia sotto controllo a lungo. Questo studio utilizza un modello murino realistico per affrontare una domanda pratica che molti pazienti e oncologi si pongono oggi: dopo una chemioterapia intensa e un inibitore PARP, aggiungere l’immunoterapia moderna può prolungare significativamente la sopravvivenza, e perché i tumori spesso ricompaiono?
Un cancro ostinato con un punto debole genetico
L’adenocarcinoma duttale del pancreas è notoriamente difficile da trattare, con una sopravvivenza a cinque anni ancora in singole cifre. Una piccola frazione di pazienti porta difetti ereditari o specifici del tumore in BRCA2, un gene necessario per riparare il DNA rotto. Questi tumori sono insolitamente sensibili ai farmaci che danneggiano il DNA, come la chemioterapia a base di platino, e agli inibitori di PARP, che compromettono ulteriormente la capacità delle cellule tumorali di riparare il DNA. Lo standard attuale per il pancreas BRCA‑mutato avanzato prevede mesi di chemioterapia a base di platino seguiti da trattamento di mantenimento con un inibitore PARP. Tuttavia, nel principale trial clinico POLO questa strategia non ha prolungato la sopravvivenza globale, evidenziando la necessità di comprendere la resistenza e di progettare approcci di mantenimento migliori.
Costruire un modello murino più verosimile
Molti modelli di laboratorio esistenti eliminano le componenti immunitarie e stromali che circondano i tumori reali nei pazienti. Per superare questo limite, gli autori hanno ingegnerizzato topi che sviluppano tumori pancreatici carenti di BRCA2 in presenza di un sistema immunitario completamente funzionante. Da questi tumori spontanei hanno derivato linee cellulari clonali che potevano essere impiantate in topi geneticamente compatibili. Questi tumori mutanti Brca2 assomigliavano e si comportavano molto come i tumori pancreatici umani: erano densamente fibrotici, in gran parte privi di cellule T e mostravano alti livelli di danno DNA spontaneo. In modo cruciale, i tumori erano molto sensibili a una comune combinazione a base di platino (gemcitabina più cisplatino), mentre il trattamento con inibitore PARP da solo aveva effetti modesti e di breve durata negli animali, nonostante una forte attività contro le stesse cellule in coltura. 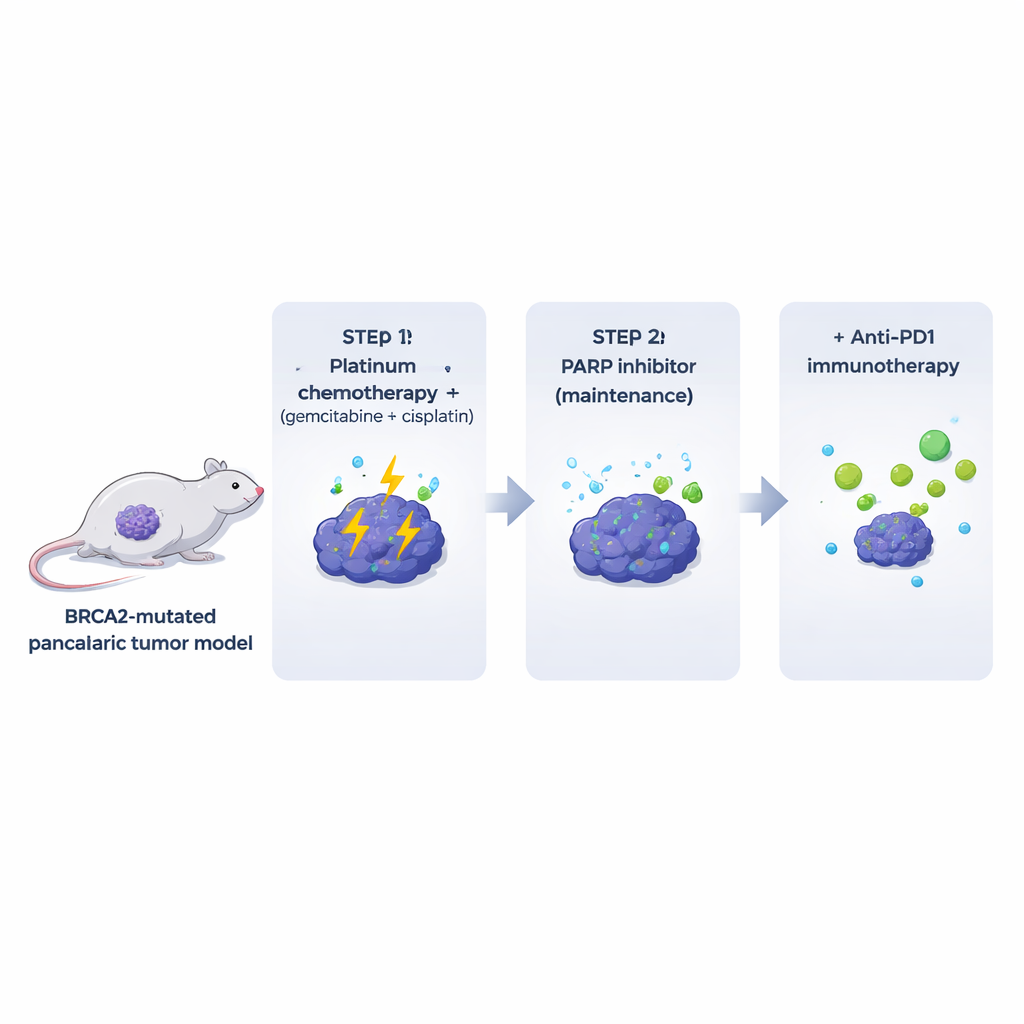
La chemioterapia rimodella il microambiente tumorale
Il gruppo ha quindi indagato cosa accade all’interno del tumore dopo la chemioterapia a base di platino. Dieci giorni dopo il trattamento i tumori si erano ridotti ma non erano stati eradicati. Le analisi dell’espressione genica hanno rivelato un marcato spostamento verso attività legate al sistema immunitario: vie correlate all’attivazione delle cellule T e all’immunità adattativa risultavano attivate. Più cellule T sono state trovate all’interno dei tumori trattati e molte di queste mostravano marcatori di esaurimento—segni che erano state attivate ma stavano diventando inefficaci. Schemi simili di aumento della presenza di cellule T sono stati osservati in tumori pancreatici umani con mutazioni BRCA o correlate a PALB2 dopo che i pazienti avevano ricevuto chemioterapia a base di platino prima dell’intervento chirurgico. Allo stesso tempo, le cellule tumorali aumentarono i livelli di PD‑L1, una proteina di superficie che può spegnere le cellule T legandosi al recettore PD‑1, suggerendo che i tumori si difendevano da questa nuova pressione immunitaria.
Perché il PARP da solo non basta—e dove emerge la resistenza
Riproducendo la cura clinica, i ricercatori somministrarono ai topi un ciclo iniziale di gemcitabina e cisplatino, seguito dal mantenimento con l’inibitore PARP olaparib. Questa sequenza migliorò il controllo tumorale e la sopravvivenza rispetto alla sola chemioterapia, confermando che la chemioterapia precedente può rendere i tumori più suscettibili all’inibizione di PARP. Tuttavia, nessun topo fu curato: i tumori alla fine ricrebsero durante il mantenimento con PARP. I tumori resistenti mostravano un aspetto più differenziato e livelli fortemente aumentati del regolatore dello sviluppo CDX2. Ciò suggerisce che, almeno in questo modello, la resistenza non deriva semplicemente dalla riparazione del difetto originale nella riparazione del DNA, ma può implicare uno spostamento nell’identità cellulare del tumore. CDX2 potrebbe potenzialmente servire come biomarcatore di resistenza emergente nei pazienti.
Sbloccare l’immunoterapia con la sequenza corretta
Farmaci che modulano i checkpoint immunitari come gli anticorpi anti‑PD1 hanno trasformato il trattamento di diversi tumori, ma il cancro pancreatico è rimasto in gran parte non responsivo. Coerentemente con questo, l’anti‑PD1 (con o senza un altro checkpoint, anti‑CTLA4) non portò benefici quando somministrato a tumori BRCA2‑mutanti non trattati, né ebbe molto effetto se semplicemente aggiunto alla terapia con inibitore PARP. Il quadro cambiò quando fu usata la sequenza completa: prima chemioterapia a base di platino, poi mantenimento con PARP più anti‑PD1. In questo contesto i tumori si ridussero più profondamente e i topi vissero più a lungo rispetto a chemioterapia più PARP o anti‑PD1 da soli. Aggiungere anti‑CTLA4 al mantenimento con PARP non diede benefici simili, suggerendo che l’ambiente tumorale primed dalla chemioterapia è specificamente predisposto a rispondere al blocco di PD‑1. 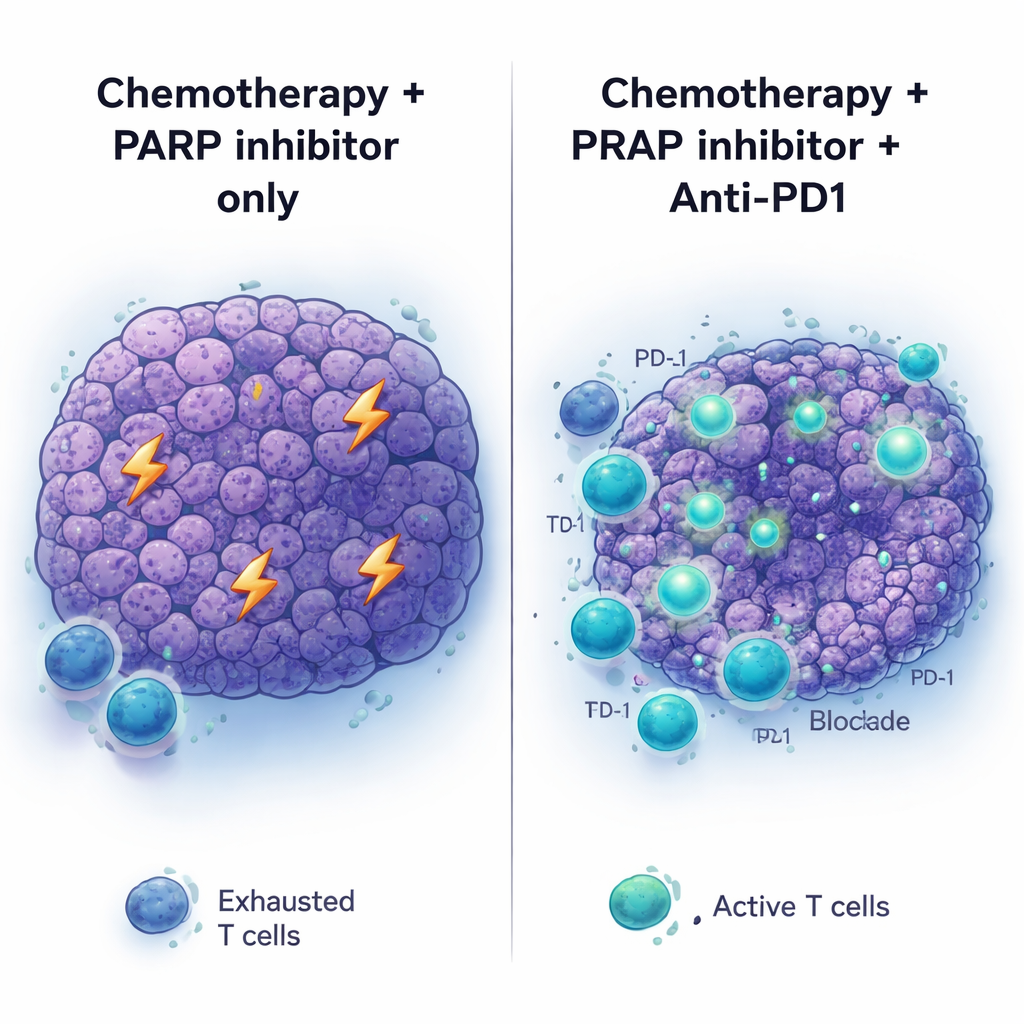
Cosa potrebbe significare per le cure future
Complessivamente, lo studio sostiene che per il cancro pancreatico con mutazione BRCA l’ordine e la combinazione delle terapie sono determinanti. Una chemioterapia fortemente danneggiante il DNA non solo attacca direttamente le cellule tumorali, ma suscita anche una risposta immunitaria, anche se inizialmente attenuata da esaurimento e difese mediate da PD‑L1. Gli inibitori PARP possono prolungare il beneficio ma difficilmente essere curativi da soli e possono spingere i tumori verso uno stato resistente ad alta espressione di CDX2. Sovrapporre l’immunoterapia anti‑PD1 al mantenimento con PARP dopo la chemioterapia a base di platino potrebbe convertire questo panorama immune brevemente infiammato ed esausto in un attacco antitumorale più efficace e duraturo. I trial clinici in corso che combinano inibitori PARP con immunoterapia nel cancro pancreatico correlato a BRCA saranno fondamentali per capire se questa strategia temporizzata con cura può tradursi in vite più lunghe e migliori per i pazienti.
Citazione: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Parole chiave: cancro pancreatico, mutazione BRCA2, chemioterapia a base di platino, inibitore PARP, immunoterapia anti‑PD‑1