Clear Sky Science · it
Classificazione multiclasse delle malattie oculari mediante tecniche di fusione EfficientNetB0 e deep learning
Perché sono importanti i controlli oculistici precoci
La perdita della vista spesso si insinua silenziosamente. Problemi oculari comuni come le cataratte, il glaucoma e i danni diabetici alla retina possono sottrarre la vista molto prima che i sintomi diventino evidenti. In tutto il mondo non ci sono abbastanza specialisti per visitare tutti in tempo, soprattutto nelle aree rurali o a basso reddito. Questo studio esplora come un sistema informatico intelligente che interpreta fotografie del fondo oculare potrebbe aiutare i medici a individuare precocemente e in modo affidabile diverse importanti malattie oculari, utilizzando lo stesso tipo di intelligenza artificiale che alimenta le moderne ricerche per immagini e il riconoscimento facciale.
Individuare la malattia in un unico scatto
Gli oculisti già utilizzano immagini a colori della retina — lo strato fotosensibile sul retro dell’occhio — per cercare segni di malattia. In queste immagini le cataratte si manifestano come opacità nel percorso ottico, il glaucoma modifica la forma del nervo ottico e la retinopatia diabetica punteggia la retina con piccole fuoriuscite e cicatrici. I ricercatori hanno raccolto 4.217 immagini retiniche ad alta risoluzione, bilanciate in modo accurato tra quattro gruppi: occhi sani, cataratta, glaucoma e retinopatia diabetica. Lavorando con una raccolta bilanciata proveniente da più fonti pubbliche, hanno ridotto il rischio che il computer impari scorciatoie legate a un singolo ospedale, una fotocamera o un tipo di dataset anziché ai veri segni della malattia. 
Far lavorare insieme due “cervelli”
I moderni programmi di lettura delle immagini, detti modelli di deep learning, sono molto bravi a individuare pattern ma ciascuno ha i propri punti di forza e i propri limiti. Invece di affidarsi a un unico modello, il team ha costruito sistemi “a doppio backbone” che eseguono in parallelo due reti di immagini note e poi fondono ciò che ciascuna rileva. Una di queste reti, EfficientNetB0, è un modello compatto ed efficiente che cattura la struttura generale delle immagini; è stata sempre usata come base. È stata abbinata a turno con tre altri modelli — ResNet50, InceptionV3 e AlexNet — che si specializzano in riconoscimento di pattern più profondo, multiscala o leggero. I sistemi hanno poi combinato i due insiemi di caratteristiche in diversi modi: unendole semplicemente, sommando, pesandole differentemente o lasciando che ogni modello esprimesse un voto per la decisione finale.
Mettere il sistema alla prova
I ricercatori hanno addestrato e ottimizzato 12 diverse combinazioni di modelli sulla maggior parte delle loro immagini retiniche, tenendone da parte alcune per verificare le prestazioni. In questo test interno, l’approccio migliore ha unito le feature di EfficientNetB0 e ResNet50, raggiungendo circa il 95% di accuratezza complessiva e un punteggio quasi perfetto su una misura standard della qualità diagnostica. Combinazioni analoghe con InceptionV3 e AlexNet hanno mostrato prestazioni altrettanto solide. Per verificare se il sistema potesse gestire la varietà del mondo reale invece di memorizzare il solo set di addestramento, il team ha poi testato tutti i modelli su 400 immagini provenienti da due collezioni indipendenti acquisite in ospedali diversi con fotocamere differenti. Qui l’accuratezza è salita ancora, attestandosi tra circa il 95% e il 98%, e tutti i modelli hanno mantenuto punteggi molto alti sulla capacità di separare occhi malati da occhi sani.
Guardare dentro la scatola nera
I medici e i regolatori chiedono sempre più spesso non solo “Quanto è accurato?” ma anche “Perché prende quella decisione?”. Per rispondere a questo, gli autori hanno utilizzato strumenti di visualizzazione come Score‑CAM e LIME. Questi strumenti evidenziano quali parti di un’immagine influenzano maggiormente il verdetto del modello, trasformando l’“attenzione” del sistema in mappe di calore sovrapposte alla retina. Nella retinopatia diabetica le aree evidenziate coincidevano con vasi sanguigni che perdono e macchie vicino alla macula, il centro della visione nitida. Nel glaucoma il focus era sulla testa del nervo ottico e sui tessuti circostanti, dove si verifica il danno. Le decisioni legate alla cataratta enfatizzavano un offuscamento diffuso lungo il percorso visivo. Fondamentalmente, gli occhi normali non mostravano punti caldi forti e falsi. Questa corrispondenza ravvicinata tra il focus del modello e l’anatomia da manuale suggerisce che il sistema si basa sulle stesse caratteristiche che i clinici utilizzano nella pratica. 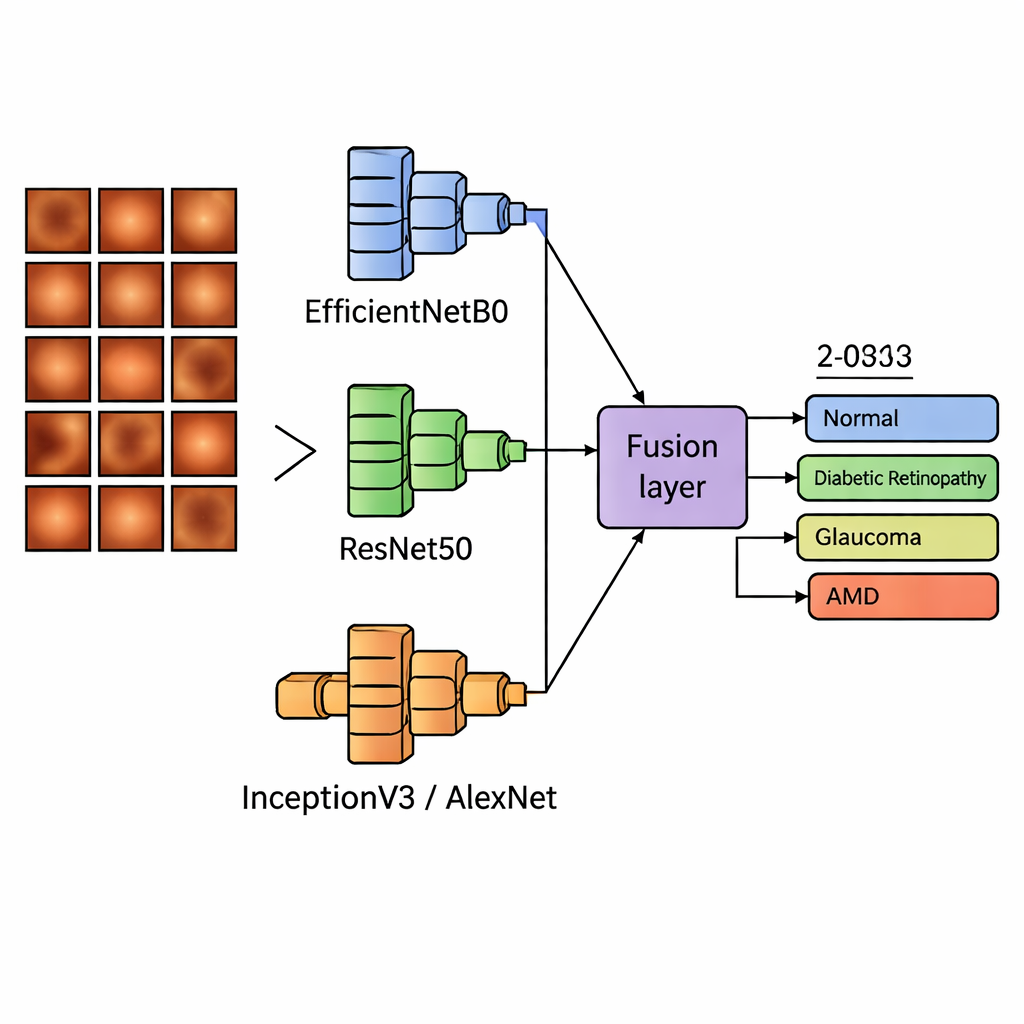
Cosa potrebbe significare per l’assistenza quotidiana
Per un non specialista, la conclusione è che una singola fotografia retinica, scattata con una fotocamera standard, potrebbe presto aiutare a screening per più cause principali di cecità contemporaneamente. Il design a doppia rete e i modi intelligenti di fondere i loro output hanno fornito non solo alta accuratezza ma anche risultati stabili quando le immagini provenivano da nuove cliniche e dispositivi — una condizione essenziale per l’uso nel mondo reale. Pur richiedendo ulteriori test su popolazioni più grandi e più varie, soprattutto prima che la tecnologia possa guidare autonomamente il trattamento, questo lavoro dimostra che combinare diversi tipi di “occhi” artificiali può produrre secondi pareri rapidi e affidabili. In ospedali affollati, piccole cliniche o unità mobili di screening, tali strumenti potrebbero aiutare a segnalare le persone che più urgentemente devono vedere un oculista, potenzialmente preservando la vista di milioni di persone.
Citazione: Sah, U.K., Chatterjee, J.M. & Sujatha, R. Multi-class eye disease classification using deep learning EfficientNetB0 fusion techniques. Sci Rep 16, 6368 (2026). https://doi.org/10.1038/s41598-026-35357-0
Parole chiave: malattie oculari, imaging retinico, deep learning, glaucoma, retinopatia diabetica