Clear Sky Science · it
Indagine sui residui 'hot-spot' funzionali di un enzima mediante monitoraggio in tempo reale della reazione enzimatica con NMR e approcci computazionali
Perché questo è importante per i futuri antivirali
Il favipiravir è una compressa già usata contro l’influenza e testata per il COVID-19, ma non combatte i virus nella forma che assumiamo. Le nostre cellule devono prima convertirlo in una molecola attiva che blocca il virus. Questo studio disseca, quasi atomo per atomo, come un enzima umano esegue un passaggio cruciale di attivazione e quali piccole parti dell’enzima fungono da “hot spot” che controllano la velocità e l’efficacia con cui il farmaco viene attivato. Comprendere questi dettagli potrebbe guidare la progettazione di antivirali di nuova generazione più potenti e più prevedibili nei pazienti.
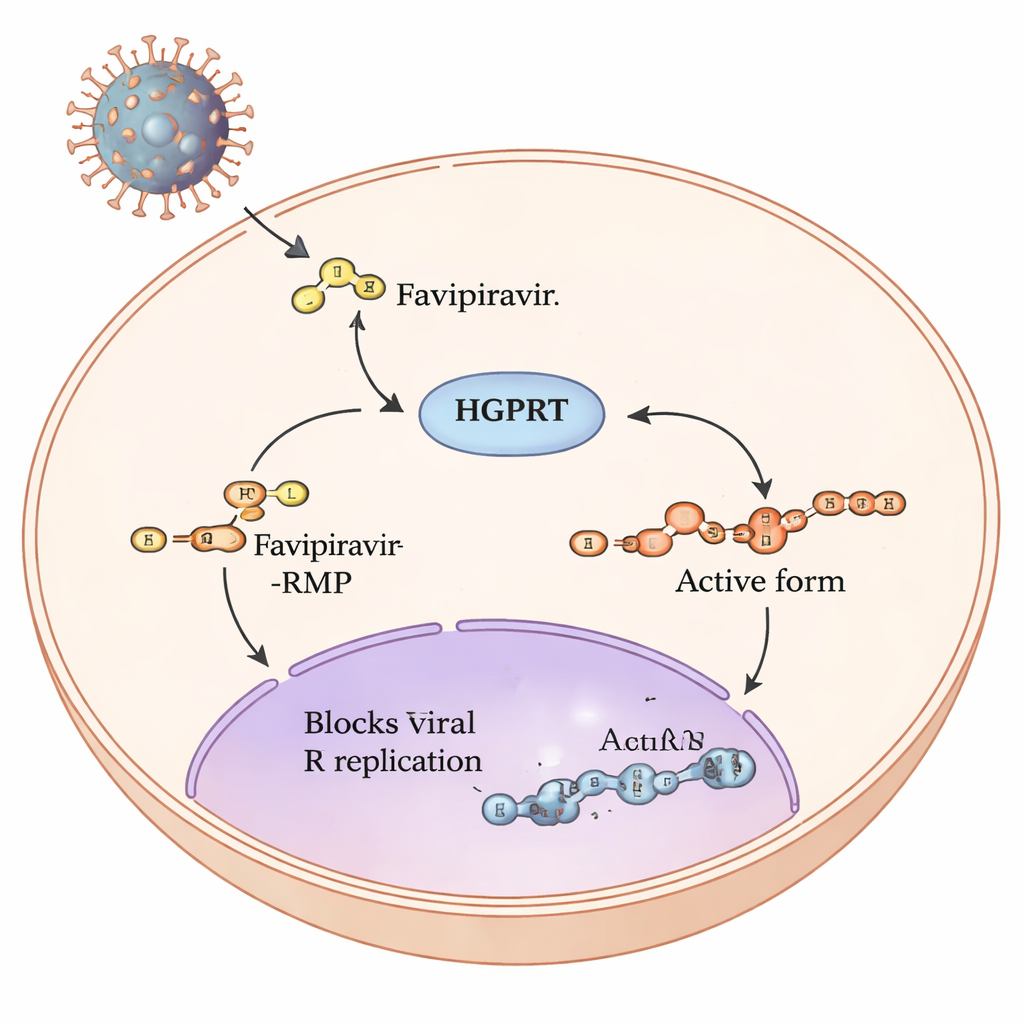
Il viaggio di un prodrug all’interno delle nostre cellule
Il favipiravir è un cosiddetto prodrug: una volta entrato nelle cellule umane, una serie di passaggi chimici lo rimodella in una forma in grado di inceppare la macchineria di replicazione degli RNA virus come l’influenza e SARS-CoV-2. Il primo e più lento passaggio di questa via è catalizzato da un enzima umano chiamato ipoxantina-guanina fosforibosiltransferasi, o HGPRT. HGPRT aggiunge al favipiravir un piccolo gruppo zucchero-fosfato, producendo favipiravir-RMP. Solo dopo questo passaggio altri enzimi possono costruire la forma triphosfato completamente attiva che interferisce direttamente con la RNA polimerasi virale. Poiché questo primo passaggio guidato da HGPRT funge da collo di bottiglia sulla quantità di farmaco attivo prodotta, gli autori hanno cercato di individuare quali parti di HGPRT sono più importanti per processare il favipiravir.
Osservare la chimica in tempo reale con l’NMR
In modo unico, il favipiravir contiene un atomo di fluoro che si comporta come un piccolo trasmettitore radio in un campo magnetico. Il gruppo ha sfruttato questo usando la spettroscopia di risonanza magnetica nucleare del fluoro-19 per osservare, in tempo reale, quanto favipiravir e quanto favipiravir-RMP fossero presenti in una provetta mentre la reazione procedeva. Poiché solo il farmaco contiene fluoro, i segnali NMR sono puliti e facili da seguire. Registrando ripetutamente gli spettri per 12 ore, i ricercatori hanno potuto seguire la scomparsa del farmaco iniziale e l’aumento del prodotto modificato, quindi ricavarne parametri cinetici standard come la velocità della reazione e quanto strettamente l’enzima sembra legare il farmaco.
Regolare posizioni chiave nell’enzima
Precedenti immagini a raggi X di HGPRT legato al favipiravir-RMP avevano suggerito una manciata di aminoacidi che avvolgono il farmaco in una tasca. Il nuovo lavoro testa tre di queste posizioni introducendo cambiamenti precisi a singola lettera nella proteina e confrontando ogni mutante con l’enzima naturale. Un cambiamento, denominato T138A, ha inaspettatamente reso l’enzima circa quattro-sei volte più veloce nel convertire il favipiravir, pur avendo rimosso un gruppo chimico che si pensava aiutasse a trattenere il farmaco. Un secondo cambiamento, K140M, ha rallentato moderatamente la reazione e leggermente indebolito il legame apparente. Un terzo cambiamento, D193N, ha abolito completamente la capacità dell’enzima di produrre favipiravir-RMP, nonostante la proteina alterata potesse ancora essere prodotta e legare il prodotto. Nel complesso, questi risultati mostrano che non tutti i punti di contatto hanno lo stesso ruolo: alcuni agiscono come regolatori sottili della velocità, mentre altri sono interruttori essenziali.
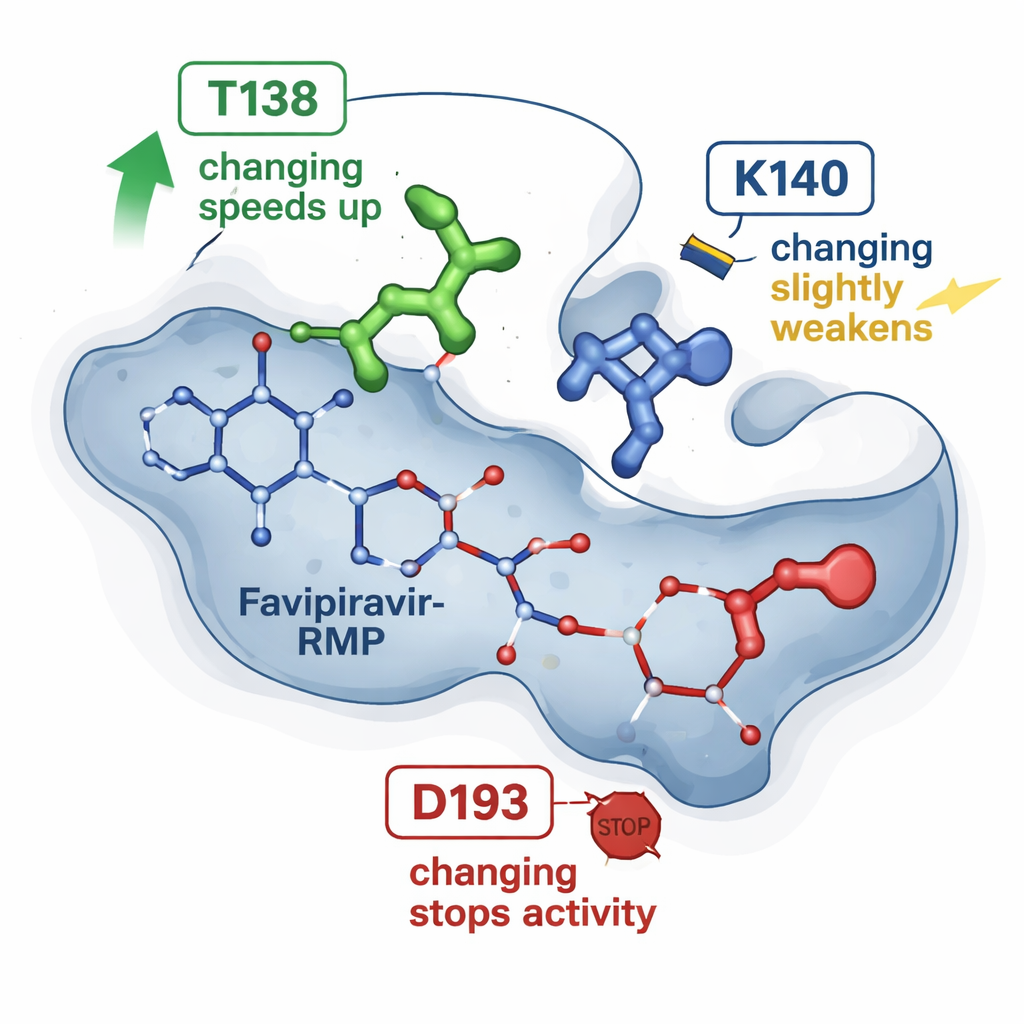
Simulare le parti in movimento su un computer
Per vedere oltre le strutture statiche, i ricercatori si sono rivolti alle simulazioni molecolari. Partendo dalla struttura tridimensionale nota di HGPRT con favipiravir-RMP, hanno utilizzato strumenti computazionali consolidati per stimare quanto forte sia il legame del farmaco in ogni mutante e per eseguire molte brevi simulazioni di dinamica molecolare. Queste simulazioni tracciano come gli atomi oscillano e interagiscono su decine di nanosecondi. I calcoli concordano con le tendenze derivate dall’NMR: la variante T138A tendeva a trattenere favipiravir-RMP in modo più favorevole ma mostrava anche episodi in cui il farmaco si spostava verso una via di “fuga”, guidato da un altro residuo (K140) che ancora temporaneamente ancora il gruppo fosfato prima del rilascio. Al contrario, la variante D193N continuava a stringere il prodotto, ma probabilmente falliva in un passaggio catalitico precedente che richiede uno ione magnesio, spiegando perché aveva perso attività nonostante un legame stabile.
Una mappa per una progettazione antivirale più intelligente
Combinando misure NMR in tempo reale con modelli computazionali dettagliati, questo studio mappa gli hot spot funzionali in HGPRT che governano l’efficienza con cui il favipiravir viene attivato. Per i non specialisti, la conclusione è che i nostri enzimi possono influenzare notevolmente quanto farmaco antivirale attivo si accumuli nelle cellule e che modificare la forma del farmaco o la tasca dell’enzima può cambiare radicalmente questo risultato. La strategia ibrida degli autori offre un progetto generale per sondare come altri medicinali interagiscono con le loro proteine target, accelerando potenzialmente lo sviluppo di nuovi composti antivirali meglio adattati ai meccanismi di attivazione dell’organismo.
Citazione: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Parole chiave: favipiravir, attivazione antivirale, enzima HGPRT, spettroscopia NMR, progettazione di farmaci