Clear Sky Science · it
Pattern informati spazialmente per dati di immunofluorescenza multiplex
Perché il quartiere intorno alle cellule tumorali conta
Il cancro pancreatico è uno dei tumori più letali, in parte perché i tumori vivono in un complesso “quartiere” di cellule immunitarie e di supporto che possono o combattere il cancro o aiutarlo a nascondersi. Questo studio introduce un nuovo modo di leggere la disposizione spaziale di queste cellule nelle immagini al microscopio, rivelando come il sistema immunitario si comporti in modo diverso nel carcinoma duttale pancreatico aggressivo (PDAC) rispetto al suo parente precanceroso, il neoplasma papillare mucinoso intraduttale (IPMN). Comprendere questi modelli nascosti potrebbe indicare diagnostiche migliori e terapie più intelligenti e mirate.
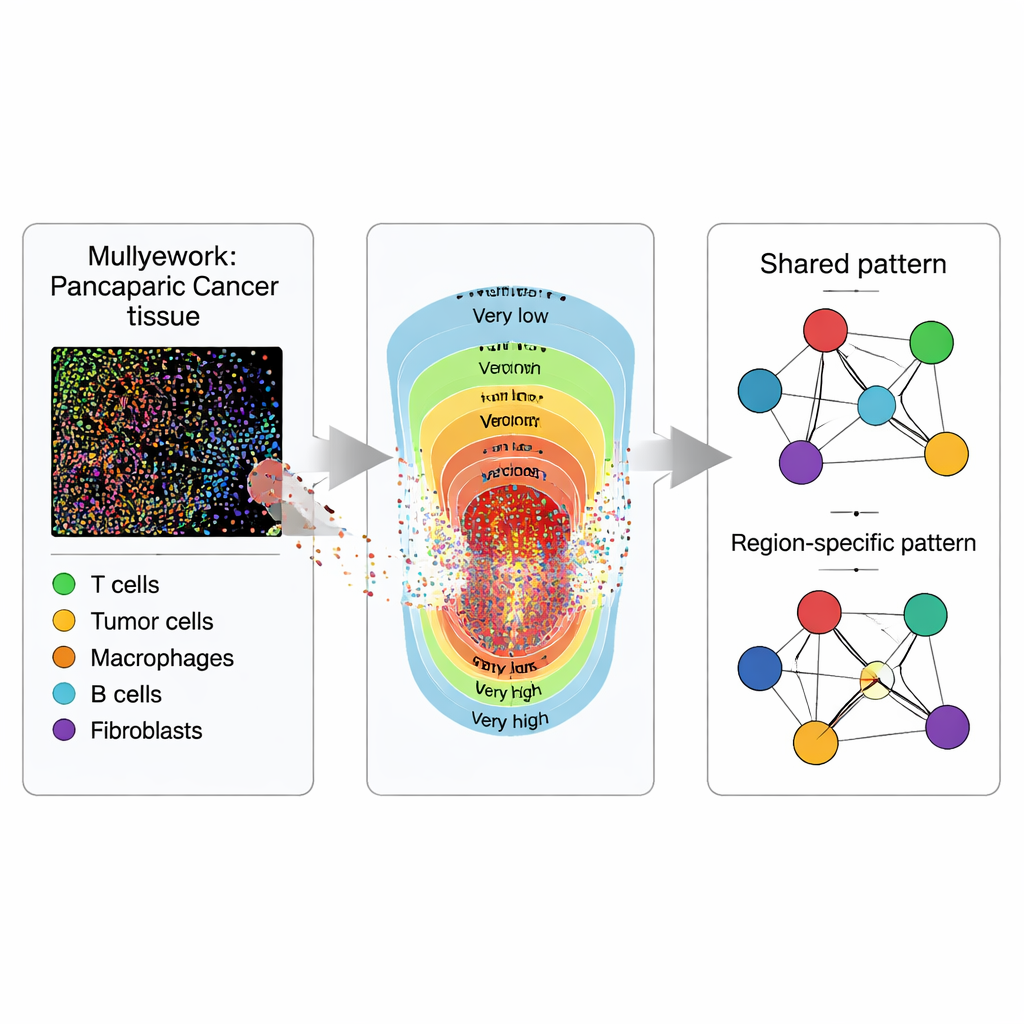
Vedere i tessuti come mappe, non solo immagini
Invece di trattare un taglio tumorale come una semplice immagine piatta, i ricercatori lo considerano come una mappa piena di punti. Usando l’imaging multiplexato con immunofluorescenza, colorano i campioni di tessuto di 119 pazienti con PDAC e 53 con IPMN in modo che diversi tipi di cellule brillino in colori distinti. Software specializzati trasformano ogni cellula visibile in un punto con coordinate e un’etichetta: cellule tumorali (epiteliali), diverse tipologie di cellule T che possono attaccare o regolare le risposte immunitarie, e cellule presentanti l’antigene che mostrano frammenti tumorali alle cellule T. La domanda chiave non è solo quante cellule di ciascun tipo sono presenti, ma dove si trovano rispetto alle altre nell’ambito del tessuto.
Dividere il tumore in zone
Per catturare come i tumori cambiano dal centro verso l’esterno, ogni campione di tessuto è suddiviso in cinque zone basate sulla densità delle cellule tumorali, da intensità tumorale “molto bassa” a “molto alta”. Queste zone rappresentano un gradiente di carico tumorale e affollamento cellulare che i patologi osservano spesso al microscopio ma raramente quantificano. All’interno di ciascuna zona, il team stima mappe di “intensità” smussate per ogni tipo cellulare, convertendo i punti sparsi in mappe di calore continue dei luoghi in cui ciascun tipo tende a raggrupparsi. Questa zonizzazione permette di confrontare non solo come le cellule interagiscono globalmente, ma come tali interazioni cambino passando da regioni tumorali sparse a regioni dense.
Trasformare i vicinati cellulari in reti
Successivamente, i ricercatori traducono i modelli spaziali in reti, dove ogni tipo cellulare è un nodo e i collegamenti rappresentano quanto due tipi cellulari tendono ad apparire insieme dopo aver tenuto conto di tutti gli altri. Utilizzando un quadro statistico bayesiano che chiamano ISPat (Informed Spatially aware Patterns), separano le caratteristiche condivise tra tutte le zone da quelle specifiche di ciascuna zona. ISPat può anche integrare conoscenze biologiche a priori quando disponibili, aiutando a stabilizzare le stime in dati complessi. Esperimenti di simulazione mostrano che ISPat può recuperare in modo affidabile pattern noti e lo fa molto più velocemente dei metodi tradizionali, rendendolo pratico per studi di imaging su larga scala.
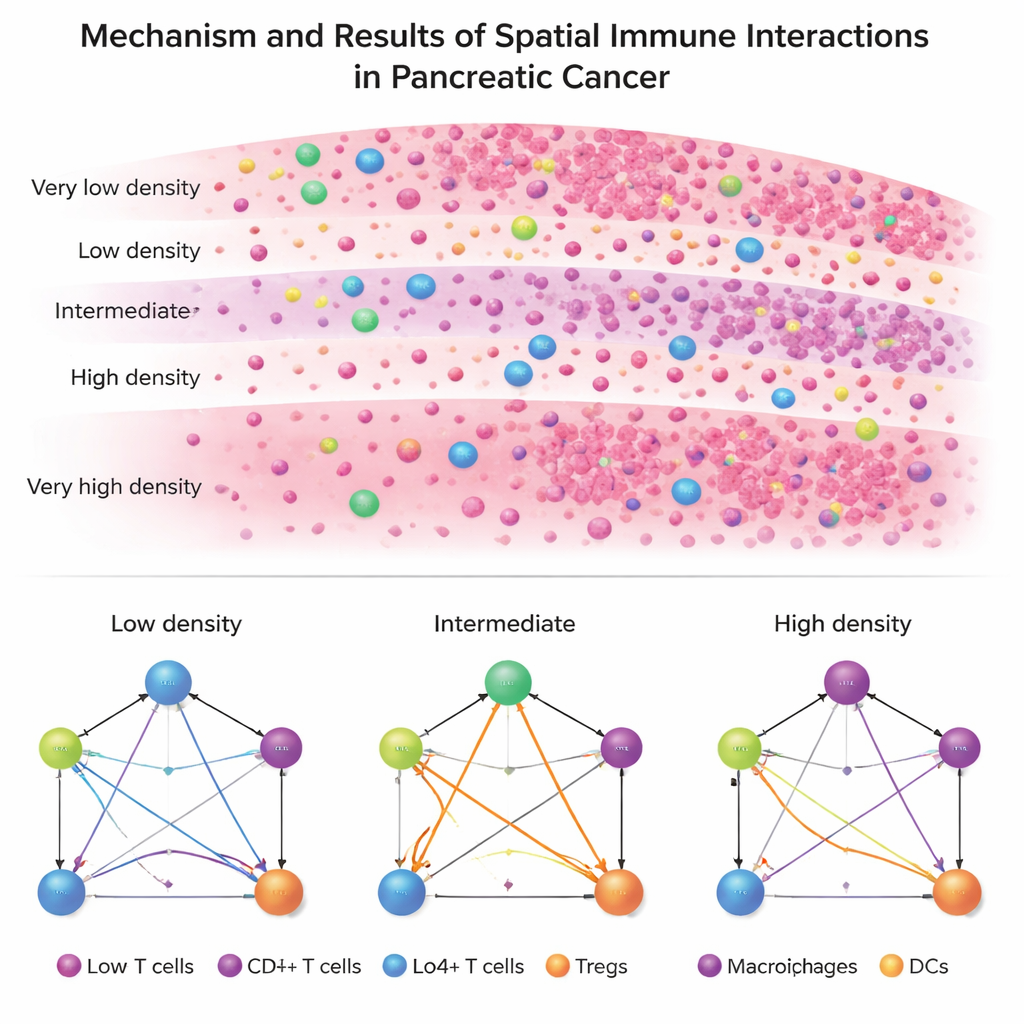
Due malattie, due architetture immunitarie
Applicando ISPat a dati clinici reali emerge un contrasto marcato tra PDAC e IPMN. Il PDAC mostra un’architettura immunitaria rigida e uniforme: in quasi tutte le zone, cellule tumorali, cellule T helper, cellule T citotossiche, cellule T regolatorie e cellule presentanti l’antigene mantengono quasi lo stesso schema di relazioni. Ciò suggerisce un ambiente immunosoppressivo stabile e radicato, difficile da modificare. Per contro, l’IPMN mostra molta più variazione da zona a zona, in particolare nel modo in cui le cellule T regolatorie si connettono con le altre cellule immunitarie. Nell’IPMN, le zone a densità intermedia—non completamente affollate di cellule tumorali né quasi prive di tumore—manifestano il rimodellamento più marcato delle interazioni immunitarie.
Punti caldi per l’evasione immunitaria e la terapia
Approfondendo l’analisi, lo studio individua coppie specifiche di tipi cellulari le cui interazioni differiscono in modo coerente tra PDAC e IPMN, in particolare in quelle zone a densità intermedia. Molte di queste coinvolgono le cellule T regolatorie, che possono attenuare gli attacchi immunitari, e le cellule presentanti l’antigene e le cellule T citotossiche, che avviano ed eseguono risposte antitumorali. In particolare, le interazioni che guidano la presentazione dell’antigene e l’uccisione diretta del tumore, così come quelle che rafforzano la soppressione immunitaria, divergono più nettamente in queste aree intermedie del gradiente, non nelle regioni tumorali più estreme. Questo schema suggerisce che il campo di battaglia cruciale per il controllo immunitario risiede nelle zone di transizione dove tumore e sistema immunitario sono ancora in fase di negoziazione attiva.
Cosa significa per i pazienti
Per un non specialista, il messaggio è che il posto in cui le cellule si trovano in un tumore conta tanto quanto quali cellule sono presenti. Il PDAC sembra cristallizzare una “mappa” immunitaria stabile e soppressiva, mentre il paesaggio immunitario dell’IPMN resta più flessibile e dipendente dalla regione. Queste impronte spaziali potrebbero diventare biomarcatori per distinguere tumori pericolosi da lesioni precancerose e per prevedere quali pazienti potrebbero trarre beneficio da specifiche immunoterapie. Il quadro ISPat offre uno strumento generale per leggere questi codici spaziali in molte malattie, sostenendo un futuro in cui il trattamento del cancro sia guidato non solo dalla genetica e dai tipi cellulari, ma dalla geografia dettagliata delle cellule all’interno del tumore di ciascun paziente.
Citazione: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
Parole chiave: cancro pancreatico, microambiente tumorale, imaging spaziale, interazioni immunitarie, oncologia di precisione