Clear Sky Science · it
Un sistema di tag REC privo di lisina per applicazioni di biotinilazione di prossimità
Perché i tag minuscoli sulle proteine sono importanti
All’interno di ogni cellula, le proteine raramente agiscono da sole: si associano in partnership dinamiche che guidano salute e malattia. Per studiare queste collaborazioni, gli scienziati spesso applicano alle proteine piccoli “tag identificativi” in modo da poterle tracciare, isolare da una miscela o osservare al microscopio. Un metodo diffuso, chiamato biotinilazione di prossimità, permette di mappare chi si trova vicino a chi all’interno della cellula, ma presenta un problema nascosto: molti di questi tag identificativi vengono chimicamente modificati e di fatto scompaiono proprio quando servono di più. Questo studio presenta un nuovo tipo di tag, chiamato REC, progettato per rimanere riconoscibile in queste condizioni impegnative.
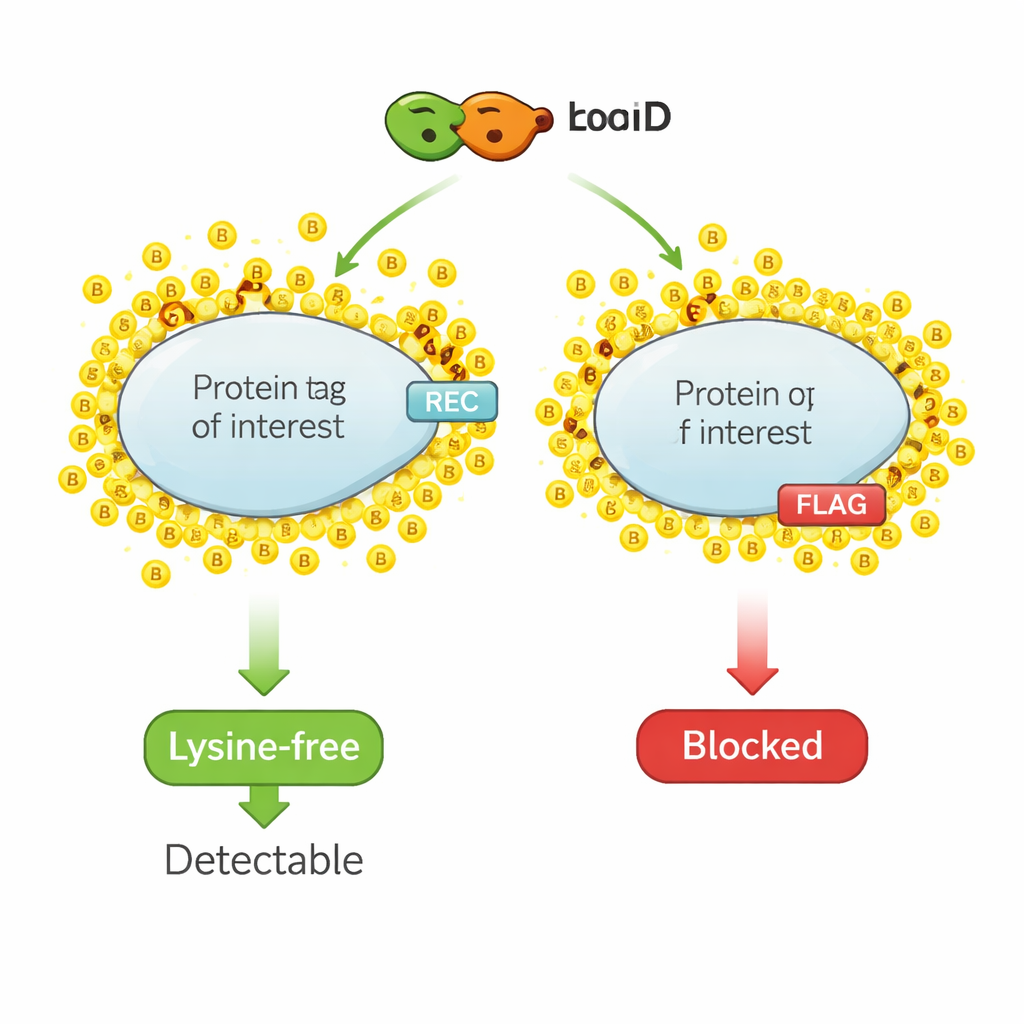
Un evidenziatore chimico per i vicini proteici
La biotinilazione di prossimità funziona come un evidenziatore molecolare. Un enzima ingegnerizzato, come TurboID, viene fuso a una proteina di interesse. Quando si aggiunge biotina — una piccola vitamina — TurboID lega rapidamente molecole di biotina alle proteine nelle vicinanze. I ricercatori poi isolano tutte le proteine marcate con biotina e le identificano, ottenendo un’istantanea del vicinato proteico. Tuttavia, la stessa chimica che marca le proteine vicine prende di mira anche i piccoli tag epitopici usati comunemente per la rilevazione, perché questi tag contengono di solito lisina, un amminoacido che rappresenta il principale sito di attacco per la biotina. Quando le lisine nel tag sono ricoperte di biotina, gli anticorpi non riconoscono più il tag e il segnale nelle metodiche di rilevazione standard diminuisce o scompare.
Progettare un tag che rifiuta la modifica
Per risolvere il problema, gli autori hanno cercato di creare un nuovo tag completamente privo di lisina. Hanno iniziato da un frammento di una proteina del parassita della malaria chiamata PfRipr5, che ha scarsa somiglianza con le proteine umane, riducendo il rischio di reazioni incrociate indesiderate. Usando un metodo di screening basato su microchip nei conigli, hanno generato 22 anticorpi monoclonali contro PfRipr5 e identificato uno, denominato clone n. 6, con legame particolarmente forte e specifico. Tramite l’accorciamento sistematico e la mutagenesi del frammento PfRipr5, hanno ridotto il bersaglio dell’anticorpo a un tratto di 11 amminoacidi. Questa sequenza minima conteneva una sola lisina, che hanno sostituito con un amminoacido simile, l’arginina. Sorprendentemente, l’anticorpo continuava a legare con la stessa efficacia. Questa sequenza ottimizzata, priva di lisina, è stata chiamata tag REC, e l’anticorpo corrispondente anticorpo REC.
Mettere alla prova il tag REC
Il gruppo ha quindi testato se il tag REC potesse sostituire tag ampiamente usati come FLAG nelle tecniche di laboratorio comuni. Quando fusi a proteine fluorescenti o di segnalazione e prodotti in sistemi cell-free e in cellule di mammifero, le proteine con tag REC venivano prontamente rilevate mediante immunoblotting, un saggio sensibile basato su luce chiamato AlphaScreen e mediante immunostaining nelle cellule. L’intensità della rilevazione era simile a quella del tag FLAG e a quella di un altro sistema di tag privo di lisina (AGIA), e l’anticorpo REC mostrava pochissimo rumore di fondo in diverse linee cellulari umane e di scimmia. È importante che il tag funzionasse sia se posizionato all’inizio sia alla fine della proteina, e su proteine localizzate in differenti compartimenti cellulari, inclusi nucleo, mitocondri, reticolo endoplasmatico e membrana cellulare.
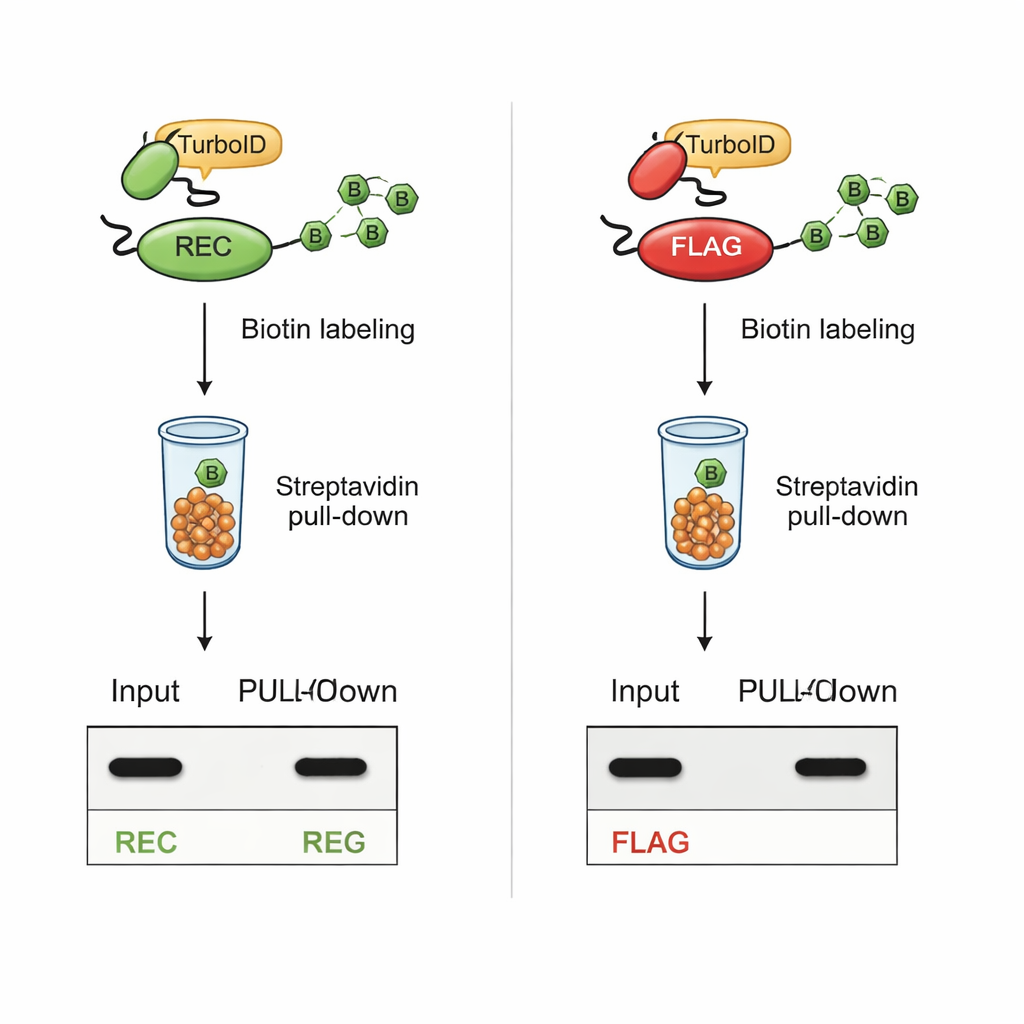
Rimanere visibili durante una marcatura intensa
La prova cruciale era se il REC sarebbe rimasto rilevabile dopo la biotinilazione mediata da TurboID. Nelle cellule in cui TurboID era fuso a partner di interazione noti, le proteine portatrici del tag REC restavano chiaramente visibili sia negli estratti di cellule intere sia nella frazione purificata marcata con biotina. Al contrario, le proteine con il classico tag FLAG perdevano il segnale FLAG una volta che TurboID era attivo, nonostante le proteine fossero ancora presenti. Ulteriori esperimenti con peptidi sintetici hanno mostrato che TurboID biotinila direttamente le lisine nella sequenza FLAG, bloccando fisicamente l’accesso degli anticorpi. Il tag REC, privo di lisine, rimaneva intatto al trattamento con TurboID e si manteneva facilmente rilevabile.
Cosa significa per gli esperimenti futuri
Per i ricercatori che esplorano le reti proteiche all’interno di cellule vive, il tag REC offre uno strumento pratico: si comporta come i tag familiari negli esperimenti di routine ma continua a funzionare anche quando enzimi potenti di marcatura di prossimità sono attivi. Ciò significa che gli scienziati possono confermare con maggiore affidabilità che le loro proteine taggate sono presenti e correttamente catturate, e possono studiare altre modificazioni basate sulla lisina — come ubiquitinazione e acetilazione — senza che il tag interferisca. In breve, REC è una piccola modifica di design con un grande impatto, che aiuta a rendere più chiari e affidabili gli esperimenti complessi di mappatura proteica.
Citazione: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Parole chiave: tagging delle proteine, biotinilazione di prossimità, TurboID, interazioni proteiche, tag epitope