Clear Sky Science · it
Interazione tra metilazione del DNA di ELMO1 e Med31 favorisce EMT e metaplasia intestinale indotte da H. pylori tramite polarizzazione M2
Perché i batteri gastrici sono importanti per il rischio di cancro
La maggior parte di noi ospita miliardi di batteri nel tratto digestivo, e uno di questi — Helicobacter pylori — può vivere silenziosamente nello stomaco per decenni. Per alcune persone questa infezione è innocua, ma per altre rappresenta il primo passo verso il cancro gastrico, uno dei tumori più letali al mondo. Questo studio indaga come una piccola modifica chimica del DNA nelle cellule gastriche aiuti a trasformare un’infezione persistente in un danno precanceroso e, infine, in un ambiente che favorisce la crescita tumorale.
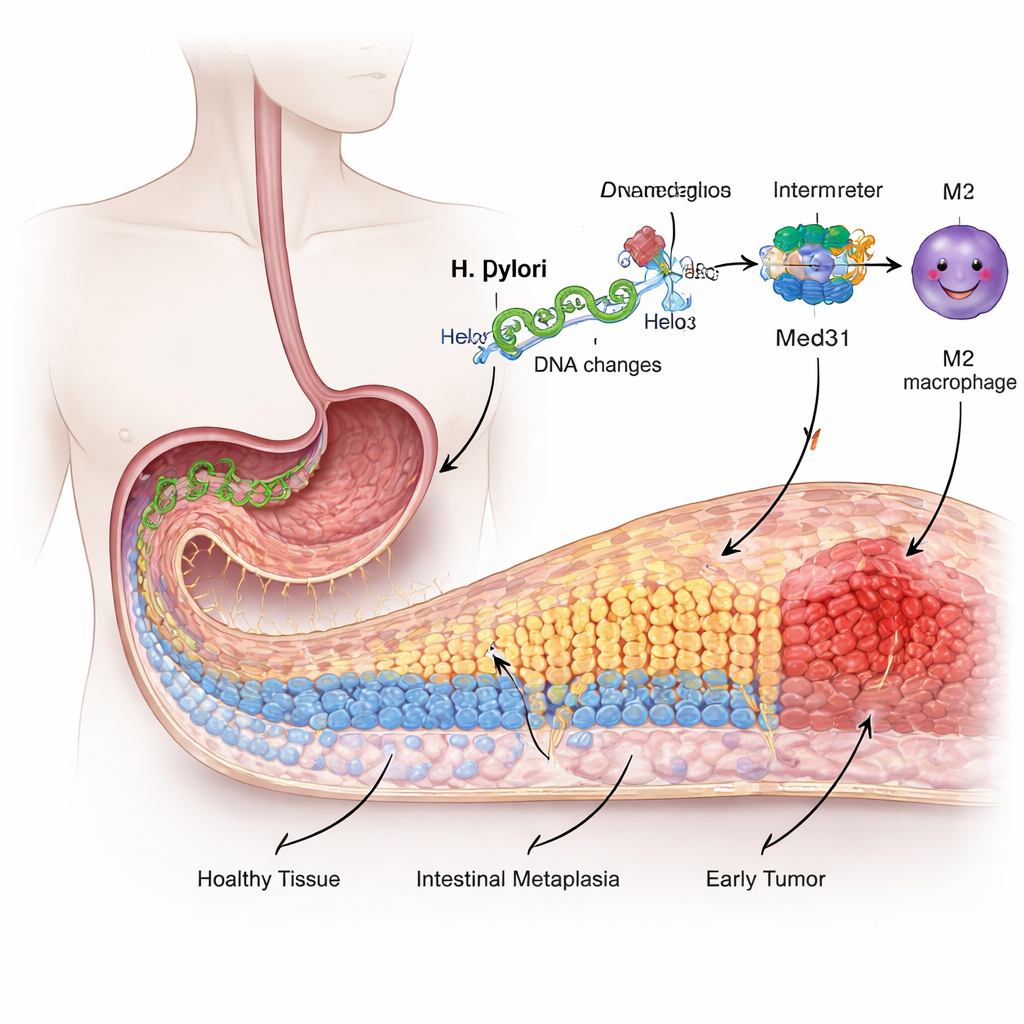
Dalla mucosa amica a un cambiamento rischioso
La superficie interna dello stomaco è rivestita da cellule specializzate adattate a gestire l’acidità intensa, non la digestione degli alimenti come l’intestino. Dopo anni di irritazione e infiammazione causate da H. pylori, alcune di queste cellule gastriche iniziano a “ridecorarsi”, acquisendo caratteristiche delle cellule intestinali in un processo chiamato metaplasia intestinale. Questo cambiamento è considerato uno stadio precanceroso. I ricercatori hanno usato una linea cellulare gastrica umana per mimare l’infezione e hanno scoperto che l’esposizione a H. pylori rendeva queste cellule più proliferative, più mobili e attivava marcatori di tipo intestinale, tutti segnali che il rivestimento stava perdendo la sua identità normale.
Piccoli tag chimici con grandi conseguenze
Il nostro DNA può essere segnato da minuscoli tag chimici chiamati gruppi metilici che agiscono come interruttori on–off per i geni senza alterare il codice genetico. Il gruppo si è concentrato su un gene chiamato ELMO1, già noto per il suo ruolo nel movimento cellulare e nella diffusione tumorale. Hanno mostrato che l’infezione da H. pylori aumentava la metilazione del gene ELMO1 e, in modo apparentemente controintuitivo, ne incrementava l’attività e i livelli proteici nelle cellule gastriche. Quando hanno usato un farmaco che rimuove questi segni metilici, le cellule hanno perso molti dei cambiamenti indotti dall’infezione: si dividevano meno, si muovevano meno e mostravano meno segnali di metaplasia intestinale. Ciò indica la metilazione di ELMO1 come un interruttore cruciale attivato dal batterio.
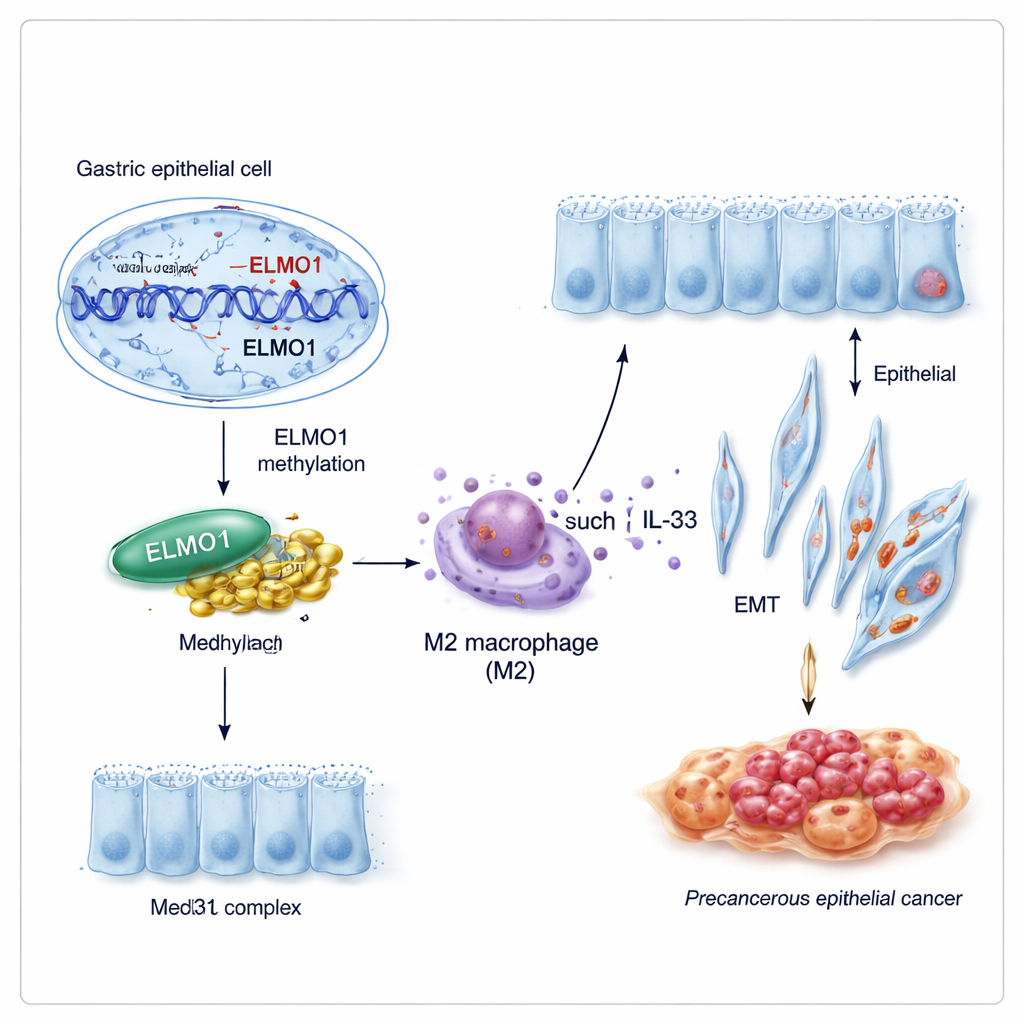
Una nuova collaborazione che riorienta il comportamento cellulare
I geni raramente agiscono da soli. I ricercatori hanno scoperto che ELMO1 metilato favorisce una collaborazione con un’altra proteina, Med31, parte di una grande “centralina” che contribuisce a decidere quali geni una cellula attiva. In condizioni che promuovono la metilazione del DNA, i livelli di ELMO1 aumentavano, Med31 aumentava e i due si legavano fisicamente, mentre un partner noto più anziano di ELMO1, DOCK10, veniva messo da parte. Questa nuova coppia ELMO1–Med31 sembra riorchestrare il programma di espressione genica delle cellule gastriche in modi che le spingono ad adottare caratteristiche intestinali e a comportarsi in modo più aggressivo.
Come le cellule immunitarie vengono spinte ad aiutare il tumore
Il cancro non si sviluppa in isolamento; cresce all’interno di un quartiere complesso di cellule immunitarie e di supporto. Lo studio mostra che le cellule gastriche infette con ELMO1 metilato rilasciano livelli più elevati di IL‑33, un segnale che induce le cellule immunitarie vicine chiamate macrofagi a polarizzarsi verso uno stato “M2” favorevole al tumore. Usando un sistema di co-coltura, gli autori hanno trovato che i macrofagi esposti a questi segnali si orientavano fortemente verso il fenotipo M2 e, a loro volta, secernevano fattori che spingevano nuove cellule gastriche a diventare più mobili, più invasive e più simili a cellule intestinali. I marcatori della transizione epitelio‑mesenchimale — quando le cellule epiteliali stanziali si trasformano in cellule migranti e invasive — aumentavano nettamente sotto l’influenza di questi macrofagi M2.
Cosa significa per la prevenzione del cancro dello stomaco
Nel complesso, il lavoro dipinge una catena di eventi: l’infezione da H. pylori altera la metilazione del DNA di ELMO1, questo ELMO1 modificato si associa a Med31, le cellule infette inviano segnali che convertono le cellule immunitarie vicine in aiutanti M2, e questi aiutanti poi promuovono sia la metaplasia intestinale sia uno stato cellulare più invasivo. Per i non esperti, l’idea chiave è che un comune batterio gastrico può rimodellare sia il rivestimento dello stomaco sia la risposta immunitaria locale tramite segni chimici reversibili sul DNA. Comprendere questa via potrebbe aprire la strada a nuovi test ematici per individuare precocemente schemi di metilazione a rischio, così come a farmaci che interrompono l’asse ELMO1–Med31–M2 prima che un’infezione cronica progredisca verso il cancro gastrico.
Citazione: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Parole chiave: cancro gastrico, Helicobacter pylori, metilazione del DNA, metaplasia intestinale, microambiente tumorale