Clear Sky Science · it
Modellazione e verifica sperimentale della precipitazione di nanoparticelle di policaprolattone
Perché piccole sfere di plastica contano per la medicina
Immaginate di rinchiudere un farmaco potente in un granello così piccolo da poter scivolare nei vasi sanguigni e rilasciare il suo contenuto esattamente dove serve. Questi granelli, chiamati nanoparticelle polimeriche, sono al centro di molti trattamenti e strumenti di imaging emergenti. Ma produrle con dimensioni corrette e riproducibili è sorprendentemente difficile. Questo studio mostra come un semplice modello computerizzato basato sulla fisica possa prevedere e regolare le dimensioni di una nanoparticella biodegradabile ampiamente utilizzata, riducendo potenzialmente anni di tentativi ed errori nello sviluppo di nuove nanomedicine.
Dalla miscelazione in cucina alla precisione di laboratorio
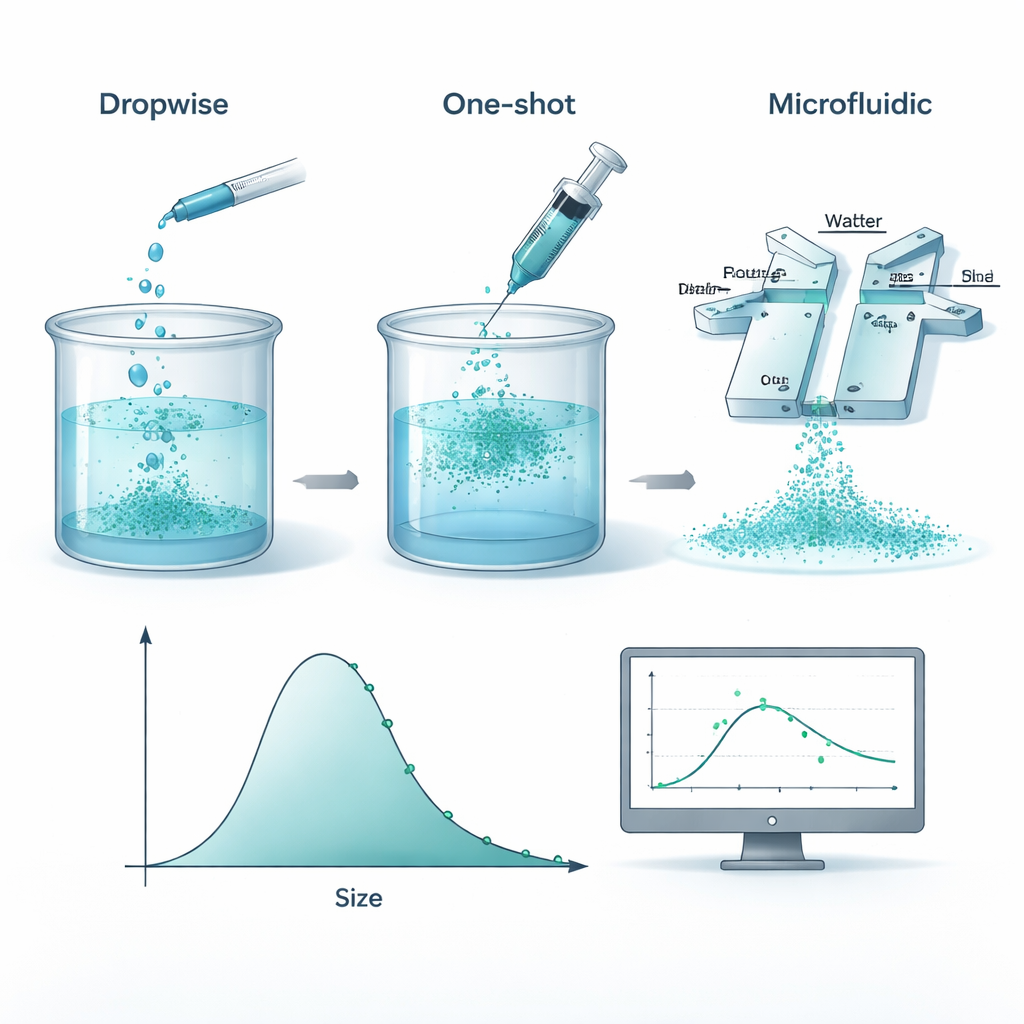
Per creare queste nanoparticelle, i ricercatori sciolgono una plastica biodegradabile chiamata policaprolattone (PCL) in un solvente organico e poi la mescolano con acqua, facendo sì che il polimero «precipiti» dalla soluzione e formi piccole sfere. Il gruppo ha confrontato tre modalità pratiche per farlo: aggiungere lentamente la soluzione polimerica goccia a goccia, versarla tutta in una volta e far scorrere entrambi i liquidi attraverso un piccolo chip microfluidico dove si incontrano in canali stretti. In condizioni controllate, tutti e tre gli approcci hanno prodotto particelle con dimensioni medie e dispersioni molto simili. Ciò significa che, almeno negli intervalli studiati, ciò che conta più del dispositivo di miscelazione è ciò che si mette dentro—la quantità di polimero e stabilizzante—piuttosto che come si mescola.
Come viscosità e molecole ausiliarie plasmano le particelle
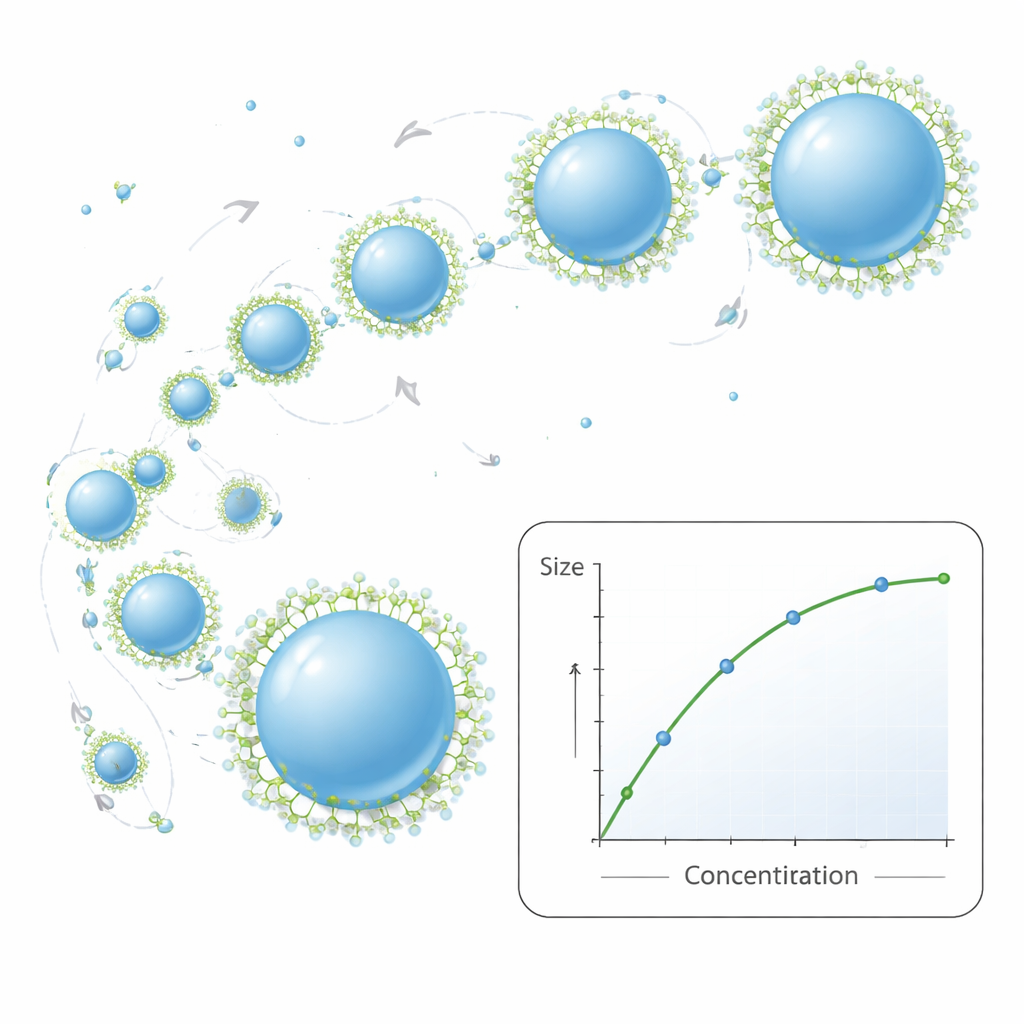
I ricercatori hanno poi esplorato come gli ingredienti della ricetta controllino la dimensione finale delle particelle. Aumentare la quantità di PCL nella fase organica rende quel liquido più spesso, ossia più viscoso. Pensate a mescolare sciroppo nell’acqua invece che succo: lo sciroppo più denso si frammenta in gocce più grandi. Qui, soluzioni polimeriche più viscose hanno prodotto nanoparticelle più grandi e distribuzioni delle dimensioni leggermente più ampie. Aggiungere un secondo solvente, etanolo, ha aiutato a mantenere il processo stabile anche a livelli molto alti di polimero, ma al prezzo di particelle più grandi nella fascia alta di concentrazione. Un secondo ingrediente, un tensioattivo chiamato Pluronic F‑127, funziona come un agente molecolare anti‑aggregazione. A bassi livelli di tensioattivo, le particelle tendono a urtarsi e aggregarsi, diventando più grandi e meno uniformi. Con l’aumento della concentrazione di tensioattivo, questo si deposita sulle superfici delle particelle, impedisce la fusione e produce nanoparticelle più piccole e stabili—fino a un certo punto, oltre il quale i miglioramenti sono modesti e la distribuzione delle dimensioni può diventare più eterogenea.
Una semplice regola di crescita che corrisponde alla realtà
Al centro del lavoro c’è un modello matematico compatto che descrive come le nanoparticelle crescono dopo la loro formazione iniziale. Tratta il loro moto come un’agitazione casuale nel liquido, in cui le collisioni a volte portano alla fusione di due particelle in una più grande. I modelli precedenti assumevano che ogni incontro tra particelle portasse a una fusione istantanea e alla formazione di sfere perfette. Il nuovo modello introduce due aspetti realistici: primo, permette un tempo finito perché due particelle a contatto si rilassino da una forma allungata a una singola sfera; secondo, consente alle molecole di tensioattivo di «bloccare» progressivamente la superficie, rallentando o fermando ulteriori fusioni. Con pochi input misurabili—come temperatura, viscosità del liquido e concentrazione iniziale di polimero—il modello predice come la dimensione media delle particelle dovrebbe cambiare con le condizioni della ricetta. In molti esperimenti, le dimensioni previste coincidono strettamente con quelle misurate mediante scattering di luce, cogliendo anche le tendenze generali su quanto si allarga la distribuzione delle dimensioni.
Usare il modello come strumento di progettazione
Per verificare se questo approccio fosse davvero utile, il team ha invertito il problema: invece di chiedere al modello di spiegare dati passati, gli ha chiesto di suggerire ricette che dovessero produrre tre dimensioni specifiche di nanoparticelle e gradi di uniformità. Hanno poi preparato in laboratorio queste formulazioni «progettate». I diametri misurati differivano dagli obiettivi di solo l’1–7 percento—ben entro la variabilità sperimentale tipica—dimostrando che il modello può guidare affidabilmente le scelte di formulazione. Le predizioni sulla larghezza della distribuzione sono risultate meno precise, ma comunque sufficienti a distinguere popolazioni relativamente strette da quelle più ampie. Rispetto a metodi di simulazione pesanti che tracciano ogni molecola o ogni vortice di flusso, questo modello semplificato gira rapidamente su computer modesti ed è facile da adattare ad altri polimeri e configurazioni di processo.
Cosa significa per la nanomedicina futura
Per i non specialisti, il messaggio chiave è che produrre nanoparticelle utili non deve più basarsi esclusivamente su laboriosi tentativi ed errori. Catturando la fisica essenziale di come piccole gocce polimeriche si muovono, collidono e vengono protette dai tensioattivi, questo lavoro fornisce una «mappa» pratica che collega le scelte di formulazione—quanta quantità di polimero, quale miscela di solventi, quanto stabilizzante—alla dimensione finale delle particelle. Poiché il PCL è un materiale biodegradabile comune usato nella somministrazione di farmaci, negli impianti e negli agenti di imaging, questo modello potrebbe aiutare i ricercatori a progettare nanomedicine più sicure ed efficaci più rapidamente e con meno materiali sprecati. Gli stessi principi possono essere estesi ad altri polimeri, portando maggiore prevedibilità ed efficienza nel mondo delle terapie su scala nanometrica.
Citazione: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Parole chiave: nanoparticelle polimeriche, nanoprecipitazione, veicolazione di farmaci, modellazione numerica, policaprolattone