Clear Sky Science · it
La nicorandil attenua il dolore neuropatico e infiammatorio tramite le vie di segnalazione TNF-α, IL6/MAPKERK1/2 e NO/cGMP
Perché ridurre il dolore nervoso è importante
Milioni di persone convivono con un dolore bruciante, lancinante o formicolante che persiste molto tempo dopo la guarigione di una lesione. Questo dolore “neuropatico” può risultare ostinato e resistente agli analgesici comuni e spesso comporta effetti collaterali legati all’uso prolungato di farmaci. Lo studio qui riassunto esplora se la nicorandil — un medicinale cardiaco già somministrato a pazienti con dolore toracico — possa anche placare le vie del dolore iperattive nel sistema nervoso e come lo faccia a livello cellulare.
Un medicinale per il cuore entra nella ricerca sul dolore
La nicorandil è prescritta di routine per trattare l’angina perché rilassa i vasi sanguigni. Agisce tramite due principali meccanismi: dona piccole quantità di monossido di azoto, una molecola di segnalazione, e apre specifici canali del potassio nelle cellule. Studi precedenti su animali suggerivano che la nicorandil possa anche ridurre il dolore agendo su recettori nervosi implicati nelle sensazioni di calore e di capsaicina (il principio attivo del peperoncino) e coinvolgendo il sistema oppioide endogeno. Nel presente studio i ricercatori hanno cercato di mappare cosa accade a valle di questi effetti iniziali, concentrandosi su infiammazione, stress ossidativo (una sorta di “arrugginimento” chimico) e su specifiche vie di segnalazione all’interno delle cellule nervose.
Testare la nicorandil in modelli di dolore persistente
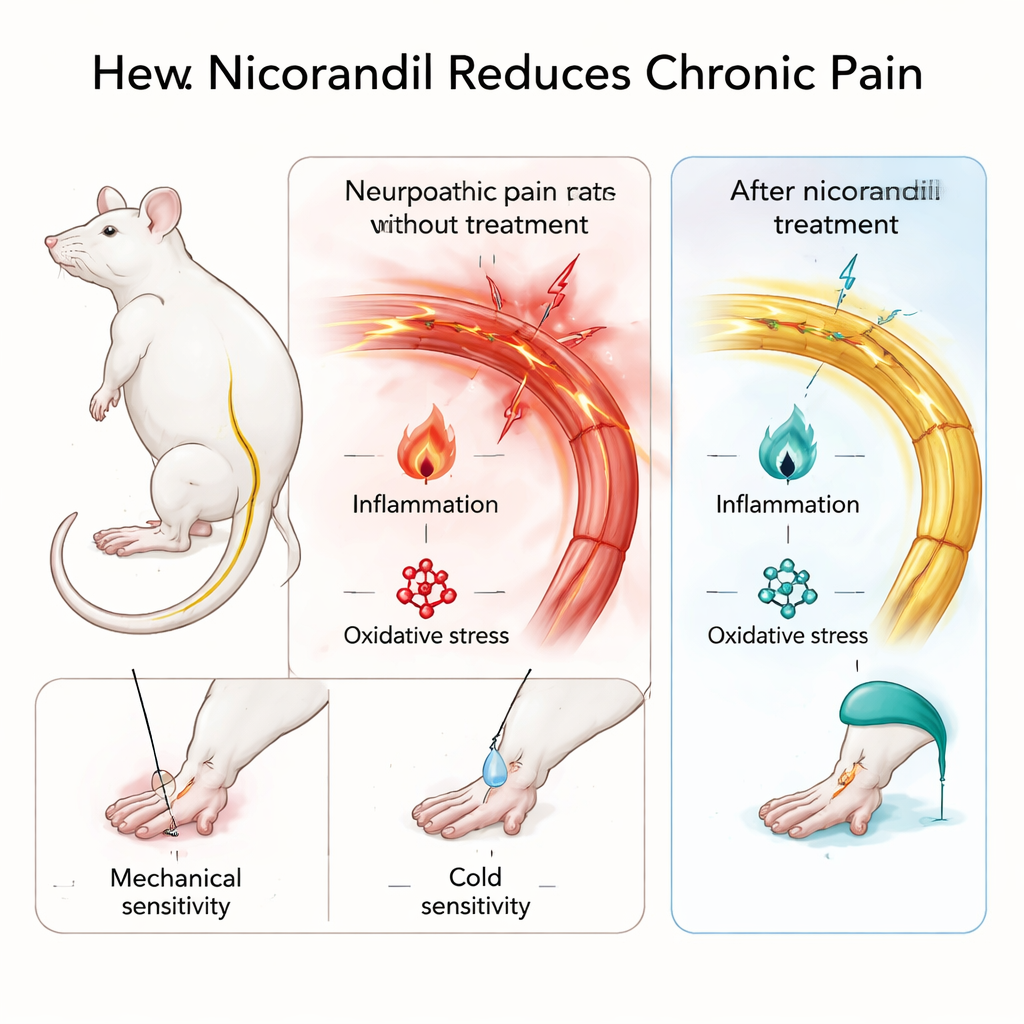
Per simulare il dolore nervoso di lunga durata, il team ha allentato la legatura del nervo sciatico nei ratti, una procedura classica che induce ipersensibilità al tatto e al freddo simile al dolore neuropatico umano. Hanno inoltre usato il test della formalina, in cui un lieve irritante chimico viene iniettato in una zampa per provocare un dolore infiammatorio ben definito e prolungato. I ratti hanno ricevuto nicorandil per via orale in due dosi e gli scienziati hanno misurato la reattività al tocco leggero e al freddo della zampa lesa, oltre alla frequenza di leccamento o contrazione dopo la formalina. È importante notare che la nicorandil non ha indotto sonnolenza o instabilità nel test dell’open-field, suggerendo che la riduzione del comportamento doloroso non era semplicemente dovuta a sedazione.
Ridurre i “segnali d’allarme” chimici
La nicorandil ha chiaramente attenuato sia il dolore indotto dalla lesione nervosa sia il dolore evocato dalla formalina. I ratti trattati hanno tollerato meglio il tatto e il freddo e hanno mostrato meno contrazioni e tempi di leccamento più brevi. Le analisi del sangue hanno rivelato che la nicorandil ha ridotto i livelli di potenti messaggeri infiammatori — il fattore di necrosi tumorale alfa (TNF-α) e l’interleuchina‑6 (IL‑6) — così come della cicloossigenasi‑2, un enzima che contribuisce alla produzione di prostaglandine legate al dolore. Ha inoltre ridotto i livelli di malondialdeide, un marcatore di stress ossidativo, indicando meno danno chimico alle membrane cellulari. Al microscopio, i nervi degli animali trattati apparivano più sani: si osservava meno danno strutturale e gonfiore nel nervo sciatico e nel raggruppamento di corpi cellulari sensoriali noto come ganglio della radice dorsale.
Districare la rete di segnalazione nei nervi del dolore
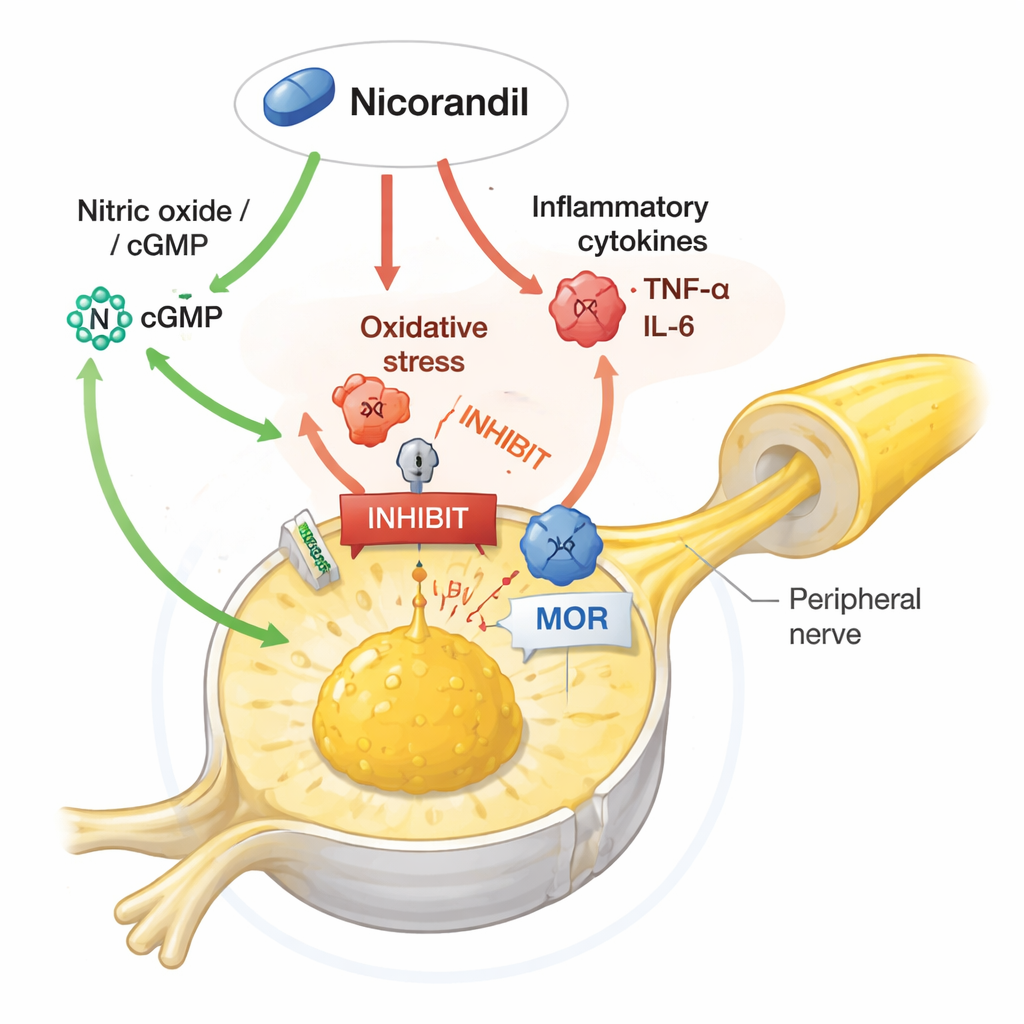
Lo studio è andato oltre indagando quali vie molecolari fossero necessarie per i benefici della nicorandil. Quando i ricercatori somministravano farmaci che aumentavano il monossido di azoto o elevavano il GMP ciclico (una molecola messaggera collegata al NO), attenuavano parzialmente la capacità della nicorandil di ridurre il dolore e di normalizzare proteine chiave. La nicorandil ha impedito il consueto aumento di ERK1/2, un membro della famiglia delle chinasi MAP che amplifica i segnali dolorifici, e ha ridotto i livelli di TRPV1, un canale che rende i nervi più sensibili al calore e agli irritanti chimici. L’aumento della segnalazione del NO o del cGMP ha invertito questi effetti protettivi, mentre il blocco degli enzimi che producono NO a volte ha rafforzato l’azione antalgica della nicorandil. Sorprendentemente, il blocco dei canali del potassio che la nicorandil apre di solito non ha abolito i suoi effetti antinocicettivi, suggerendo che in questo contesto il suo potere analgesico dipenda più dalla modulazione del monossido di azoto, dello stress ossidativo, dell’infiammazione e della segnalazione oppioide che dalla sua classica azione vascolare.
Cosa potrebbe significare per le persone che soffrono
Nel complesso, i risultati dipingono la nicorandil come un modulatore del dolore a bersaglio multiplo: calma le vie nervose iperattive riducendo il danno ossidativo e i messaggeri infiammatori, quietando ERK1/2 e TRPV1 all’interno dei neuroni sensoriali e interagendo con il monossido di azoto e con il sistema oppioide endogeno. Pur provenendo da modelli su ratto e somministrazioni a breve termine, questi risultati suggeriscono che un farmaco già in uso clinico per le malattie cardiache potrebbe un giorno essere riproposto o adattato per aiutare a trattare condizioni dolorose neuropatiche e infiammatorie difficili. Studi futuri sugli esseri umani saranno necessari per determinare dosaggi sicuri, effetti a lungo termine e se gli stessi meccanismi protettivi operino nei nervi umani.
Citazione: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Parole chiave: dolore neuropatico, nicorandil, infiammazione, stress ossidativo, segnalazione del monossido di azoto