Clear Sky Science · it
La riprogrammazione metabolica aumenta la resistenza allo stress ossidativo nei cardiomiociti in differenziamento
Perché la lotta delle cellule cardiache con l’ossigeno è importante
Ogni battito del cuore dipende da cellule muscolari specializzate chiamate cardiomiociti. Man mano che cresciamo, queste cellule affrontano un cambiamento drastico: passano da un ambiente a basso contenuto di ossigeno e alimentato da zuccheri nel grembo materno a un mondo ricco di ossigeno dopo la nascita. L’ossigeno è essenziale, ma genera anche prodotti secondari dannosi che possono danneggiare il DNA e uccidere le cellule. Questo studio esplora come le cellule cardiache in maturazione riconfigurino il loro metabolismo per tollerare maggiori livelli di ossigeno, produrre più energia e contemporaneamente proteggersi dai danni ossidativi — conoscenze che potrebbero guidare futuri trattamenti per le malattie cardiache e la rigenerazione.
Da semplici costruttori ad atleti energetici
I cardiomioblasti immaturi sono cellule piccole e in divisione che si affidano principalmente alla degradazione del glucosio per ottenere energia. Quando si differenziano in cardiomiociti maturi, interrompono la divisione e aumentano di dimensioni, spesso fondendosi in cellule polinucleate, allungate e più adatte a contrazioni potenti. Con microscopia ad alta risoluzione, i ricercatori hanno osservato questa trasformazione nell’arco di dieci giorni in un modello cellulare di laboratorio. I marcatori della proliferazione cellulare sono diminuiti, mentre le cellule si sono allungate e riorganizzate in strutture fibrose simili al tessuto cardiaco, confermando l’ingresso in uno stato più adulto e contrattile. 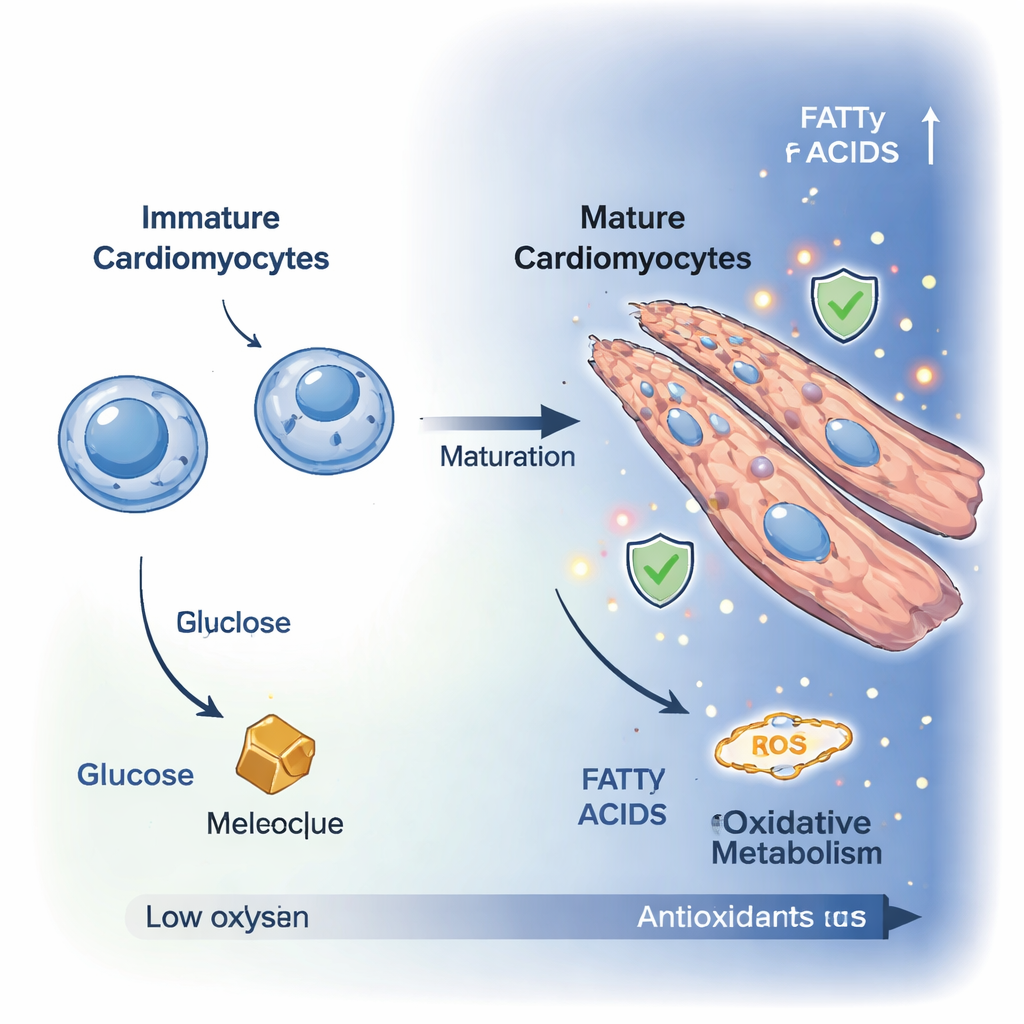
Cambio di carburante e nuovi percorsi energetici
Per capire cosa succede al livello molecolare, il gruppo ha misurato centinaia di piccole molecole all’interno delle cellule e ha impiegato l’imaging avanzato della fluorescenza naturale cellulare per tracciare l’uso di energia in tempo reale. Insieme, queste tecniche hanno mostrato un chiaro spostamento da uno stato glicolitico, in cui le cellule bruciano principalmente glucosio, a uno stato ossidativo dominato dalla respirazione mitocondriale. I livelli di glucosio e fruttosio sono diminuiti, mentre sono aumentati gli intermedi del ciclo degli acidi tricarbossilici (TCA) — come acido citrico, malato e ossoglutarato. L’analisi dei percorsi metabolici ha rivelato una maggiore attività nelle vie che convogliano carburante ai mitocondri, inclusa la navetta malato–aspartato e la degradazione degli amminoacidi, indicando che i cardiomiociti maturi ampliano le loro opzioni di combustibile e indirizzano l’energia in modo più efficiente alle loro centrali energetiche.
Vivere con più ossigeno—e più stress
Consumare carburante più efficacemente nei mitocondri ha un costo: maggiore produzione di specie reattive dell’ossigeno (ROS), molecole chimicamente aggressive che possono danneggiare lipidi, proteine e DNA. I ricercatori hanno osservato che, con la maturazione dei cardiomiociti, i mitocondri diventavano più grandi e allungati e aumentavano i marcatori di stress ossidativo. L’imaging a fluorescenza ha rivelato più granuli simili alla lipofuscina, un segno distintivo di lipidi ossidati, e una sonda nucleare ha mostrato livelli più elevati di ROS nelle cellule differenziate. La metabolomica ha indicato cambiamenti nel metabolismo del glutatione, un sistema antiossidante centrale che utilizza il glutatione — sintetizzato da amminoacidi come glutammato e glicina — per neutralizzare le ROS. Questi risultati suggeriscono che, mentre le cellule cardiache incrementano il metabolismo ossidativo, regolano anche le vie antiossidanti per mantenere sotto controllo i danni. 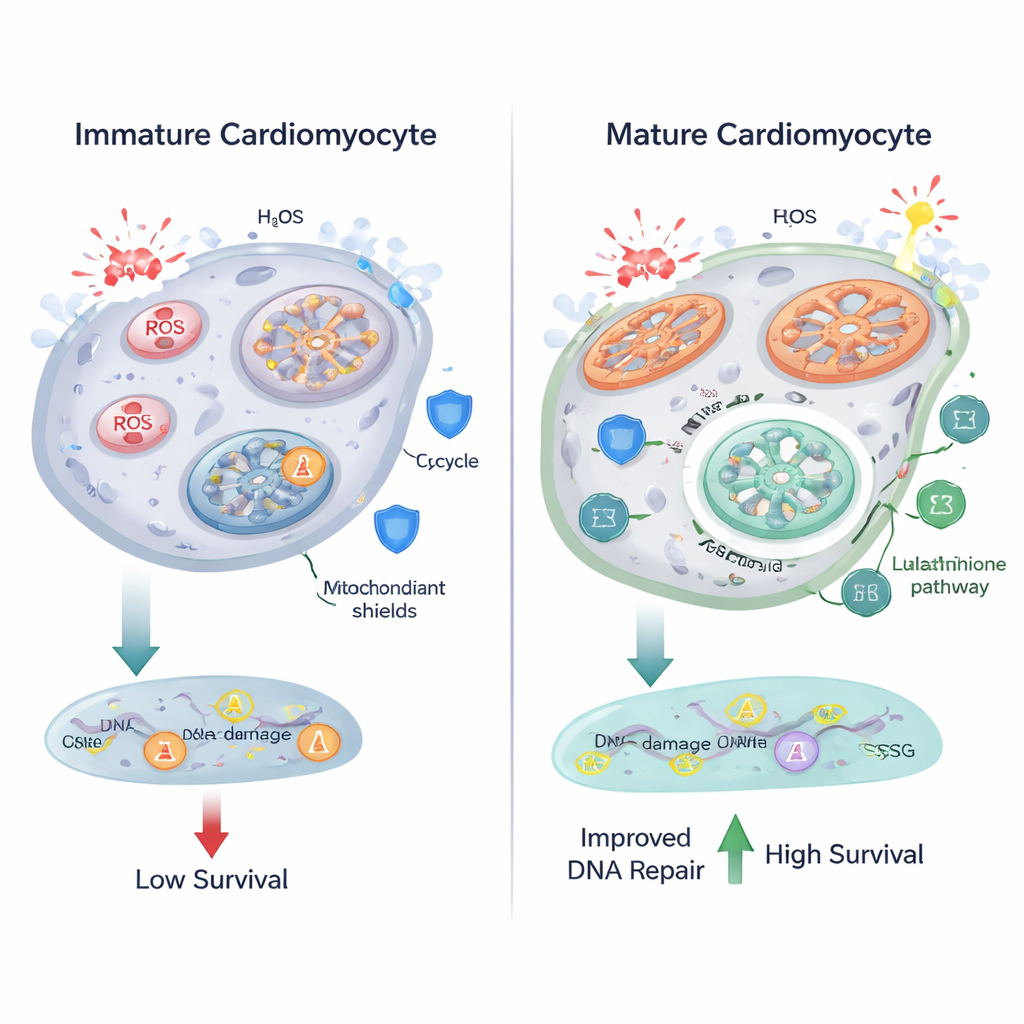
Danni contenuti, difese potenziate
Sorprendentemente, nonostante l’aumento delle ROS, i cardiomiociti differenziati non presentavano più rotture del DNA rispetto ai loro omologhi immaturi quando valutati tramite i foci γ-H2AX, un marcatore sensibile del danno al DNA. Quando il gruppo ha sfidato le cellule con perossido di idrogeno, un forte agente ossidante, sia le cellule immature sia quelle mature hanno accumulato ROS e rotture del DNA — ma le cellule mature si sono comportate meglio. Hanno mostrato proporzionalmente meno lesioni al DNA rispetto ai loro livelli superiori di ROS, erano meno propense ad attivare segnali legati alla morte cellulare come PUMA e presentavano tassi di sopravvivenza notevolmente più elevati. Questi risultati indicano che i cardiomiociti in maturazione non solo adattano il loro metabolismo ma potenziano anche i meccanismi di riparazione del DNA e di sopravvivenza, permettendo loro di resistere a condizioni ossidative più severe.
Cosa significa per la protezione del cuore
In termini semplici, questo studio mostra che man mano che le cellule cardiache maturano, imparano a funzionare a potenze maggiori senza bruciarsi. Passano da uno stile di vita a basso ossigeno e ricco di zuccheri a uno intensivo di ossigeno guidato dai mitocondri e, allo stesso tempo, costruiscono scudi e squadre di riparazione migliori per affrontare lo stress ossidativo. Comprendere questo equilibrio finemente regolato tra produzione di energia e autoprotezione potrebbe aiutare gli scienziati a progettare strategie per rendere il tessuto cardiaco adulto danneggiato più resistente o per indirizzare le cellule staminali verso cardiomiociti più sicuri e durevoli per terapie rigenerative.
Citazione: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Parole chiave: differenziazione dei cardiomiociti, stress ossidativo, mitocondri, metabolismo cellulare, malattie cardiache