Clear Sky Science · it
Predizione della malattia di Alzheimer mediante deep learning e selezione interpretabile delle caratteristiche basata su XAI dai dati di espressione genica nel sangue
Perché questa ricerca è importante
La malattia di Alzheimer sottrae lentamente memoria e autonomia alle persone; tuttavia, i test più accurati oggi disponibili spesso richiedono esami cerebrali o punture lombari costose, invasive e difficili da ripetere. Questo studio esplora un’alternativa meno invasiva: usare un semplice prelievo di sangue e analisi computazionali avanzate per individuare schemi nell’attività genica che segnalano l’Alzheimer, potenzialmente aprendo la strada a una diagnosi più precoce e accessibile.
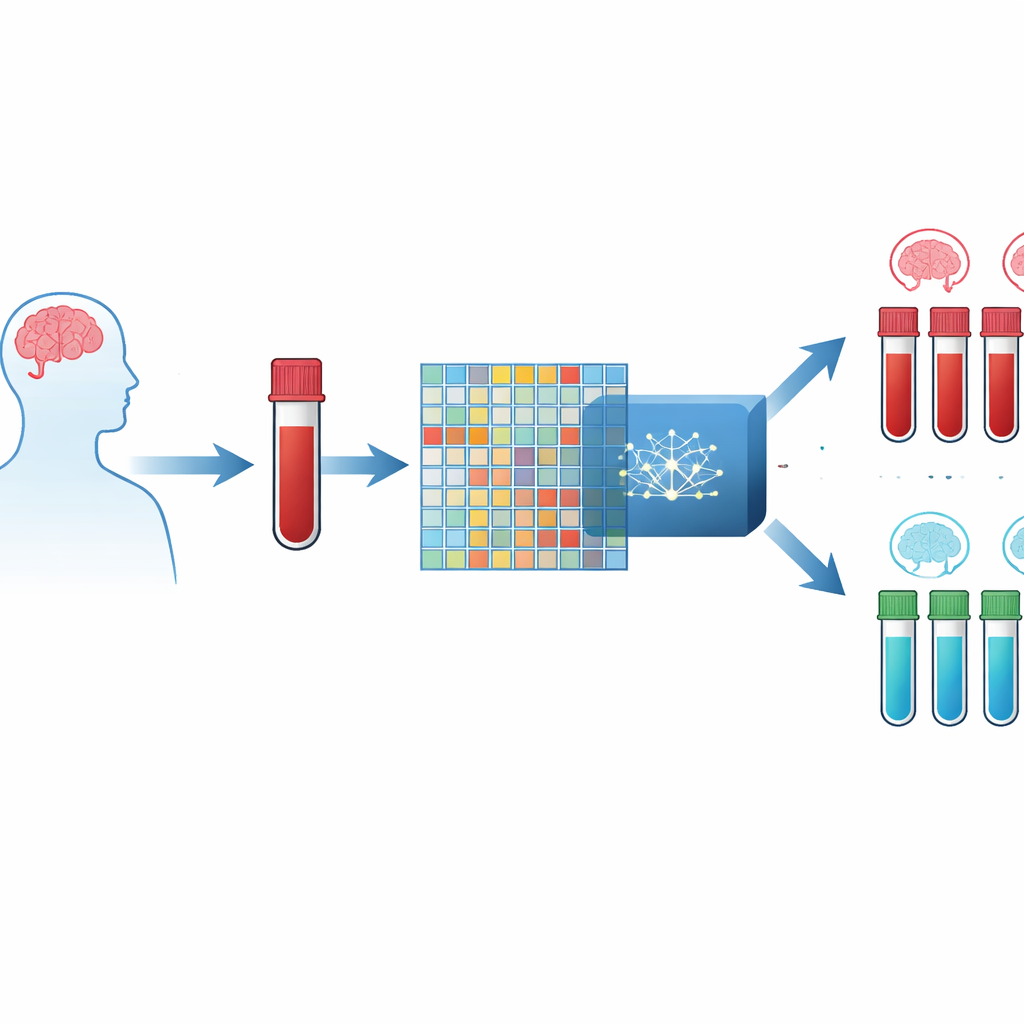
Un esame del sangue al posto della risonanza
Gli autori si concentrano su piccoli cambiamenti nel modo in cui i geni vengono attivati o disattivati nelle cellule del sangue. Le moderne tecnologie di laboratorio possono misurare l’attività di migliaia di geni simultaneamente, generando per ogni individuo una grande tabella di valori. La difficoltà è che le misure genetiche sono molto più numerose dei pazienti, il che può facilmente fuorviare i modelli computazionali. Per ovviare a questo, i ricercatori hanno combinato tre grandi dataset pubblici di campioni di sangue di persone con Alzheimer e di volontari sani, creando una risorsa integrata con oltre dodicimila geni comuni misurati in centinaia di individui.
Insegnare ai computer a individuare i segnali chiave
Invece di chiedere a un algoritmo di elaborare tutte le dodicimila variabili, il team lo ha prima istruito a selezionarne un sottoinsieme molto più piccolo e particolarmente informativo. Hanno confrontato diversi metodi, inclusi test statistici semplici, tecniche che rimuovono progressivamente i geni meno utili e approcci che incorporano la selezione direttamente nel modello. Questi strumenti di “feature selection” hanno ridotto la lista a qualche centinaio o poco più di mille geni che discriminano meglio i pazienti dai controlli sani. Gli insiemi di geni ridotti hanno aiutato a evitare che i modelli memorizzassero il rumore e hanno migliorato le prestazioni sui dati non visti.
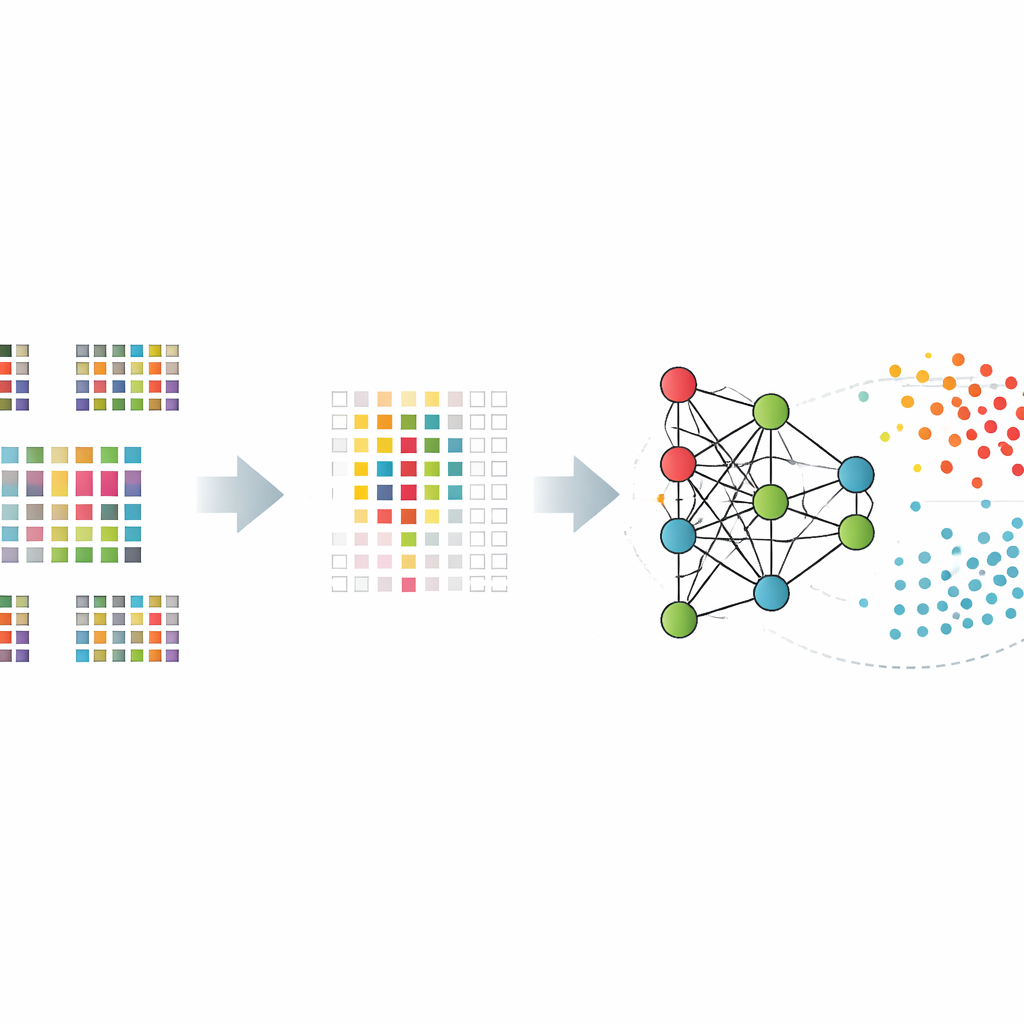
Dare senso a una scatola nera
Per evitare una fiducia cieca in una previsione da scatola nera, i ricercatori hanno applicato tecniche di intelligenza artificiale spiegabile per comprendere quali geni erano più rilevanti e come influenzavano ciascuna decisione. Un metodo chiamato SHAP, mutuato dalla teoria dei giochi, valuta il contributo di ciascun gene all’esito finale per ogni individuo. Applicandolo ai loro modelli migliori, gli autori hanno messo in evidenza un gruppo centrale di geni i cui schemi di attività inclinavano costantemente la bilancia verso una classificazione Alzheimer o sana. Molti di questi geni sono già stati associati alla salute cerebrale o alla funzione immunitaria, conferendo credibilità biologica al funzionamento interno del modello.
Potenziare la potenza statistica con pazienti sintetici
Anche dopo aver unito i dataset, il numero di campioni ematici reali restava modesto. Per rafforzare i loro modelli, gli autori hanno addestrato un tipo specializzato di rete neurale, nota come generative adversarial network, per creare profili genici sintetici realistici somiglianti a quelli dei pazienti reali. Questi campioni artificiali sono stati aggiunti solo ai dati di addestramento, mai a quelli di test, in modo che le verifiche delle prestazioni rimanessero oneste. Con questo pool di addestramento aumentato e geni scelti con cura, una rete neurale profonda è stata in grado di identificare i casi di Alzheimer con circa il 91% di accuratezza complessiva e il 95% di precisione, indicando che pochissimi soggetti sani sono stati classificati erroneamente come malati.
Cosa significano i risultati per i pazienti
Questo lavoro suggerisce che un futuro test ematico per l’Alzheimer, alimentato da algoritmi intelligenti che selezionano ed esplicitano i segnali genici chiave, potrebbe integrare o ridurre la dipendenza da esami costosi e procedure invasive. Pur richiedendo ulteriori validazioni su gruppi di pazienti indipendenti e un migliore controllo delle differenze tra metodi di laboratorio, lo studio dimostra che combinare più dataset, eliminare informazioni poco utili e aprire la “scatola nera” dell’IA può avvicinarci a un test ematico pratico e interpretabile per una diagnosi di Alzheimer più precoce e confortevole.
Citazione: Hariharan, J., Jothi, R. Alzheimer’s disease prediction using deep learning and XAI based interpretable feature selection from blood gene expression data. Sci Rep 16, 8022 (2026). https://doi.org/10.1038/s41598-026-35260-8
Parole chiave: Diagnosi di Alzheimer, biomarcatori ematici, espressione genica, deep learning, intelligenza artificiale spiegabile