Clear Sky Science · it
La deglicosilazione induce una nuova conformazione distale nel recettore della mannosa CD206
Perché le coperture zuccherine sui recettori immunitari contano
Le nostre cellule immunitarie si affidano ad «antenne» molecolari per rilevare minacce come microrganismi e cellule tumorali. Una di queste antenne, chiamata recettore della mannosa CD206, aiuta le cellule immunitarie ad afferrare molecole decorate di zuccheri e persino a localizzare i tumori. Come molte proteine, CD206 è a sua volta rivestito da brevi catene zuccherine. Questo studio pone una domanda apparentemente semplice ma di grande portata: cosa succede alla forma e alla funzione di CD206 quando quegli zuccheri vengono rimossi?
Un braccio flessibile che legge segnali zuccherini
CD206 si trova sulla superficie di alcune cellule immunitarie, in particolare dei macrofagi che pattugliano i tessuti e i tumori. Ha una struttura lunga e articolata che si protende dalla membrana cellulare e termina con diversi segmenti «lectinici» che riconoscono zuccheri su molecole in transito. CD206 può anche essere rilasciato nel flusso sanguigno, dove i suoi livelli si correlano con malattie infiammatorie e fibrotiche, rendendolo un potenziale marcatore di malattia. La proteina è pesantemente decorata con catene zuccherine N-collegate, e lavori precedenti hanno mostrato che queste possono influenzare l’affinità dei diversi segmenti nel riconoscere gli zuccheri. Molti di questi siti zuccherini si trovano lontano dalle principali tasche di legame, suggerendo che possano agire più come interruttori remoti che come semplici ostruzioni.
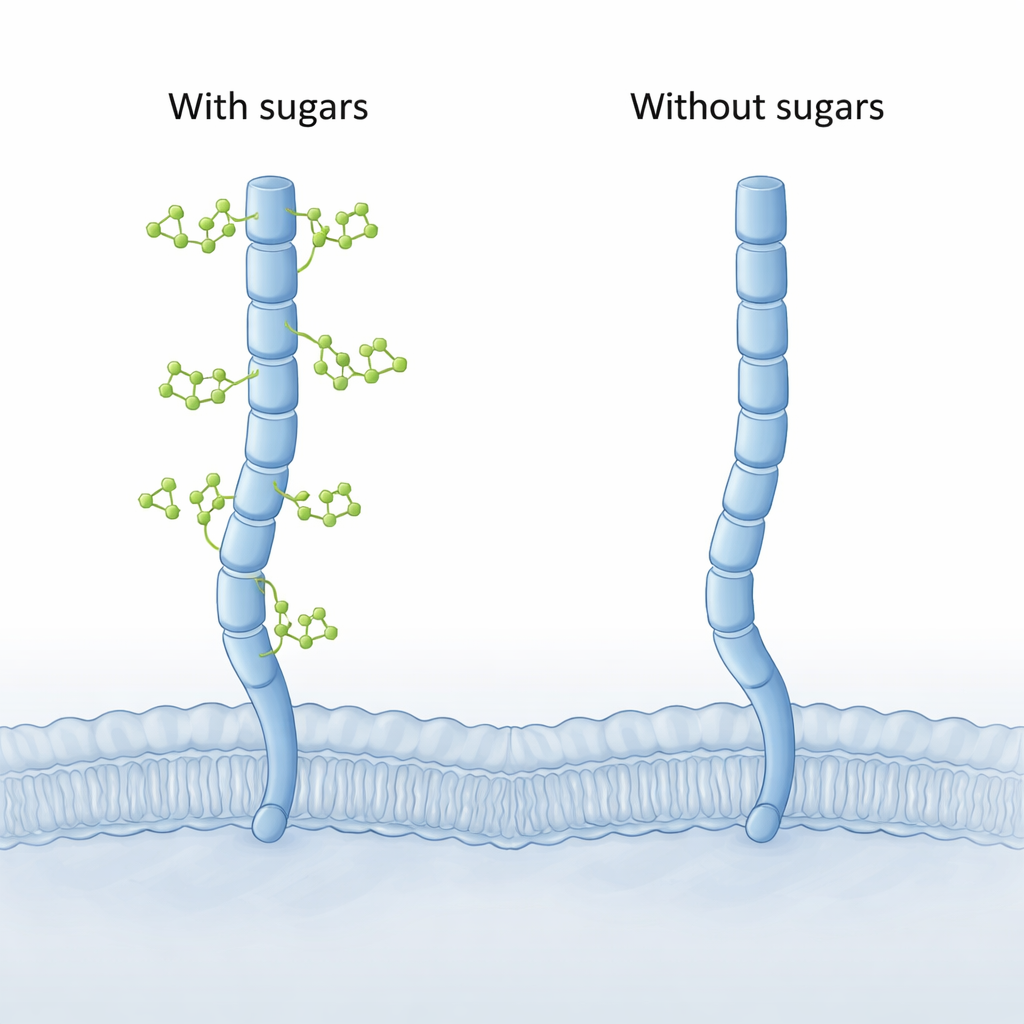
I modelli al computer rivelano una piegatura nascosta
Poiché la struttura tridimensionale completa di CD206 non è ancora stata determinata sperimentalmente, gli autori si sono rivolti a strumenti computazionali moderni. Hanno prima utilizzato AlphaFold per costruire modelli a lunghezza intera del recettore, poi hanno eseguito simulazioni di dinamica molecolare lunghe e dettagliate di CD206 con e senza gli zuccheri attaccati. Entrambe le versioni si comportavano come un braccio molecolare esteso, ma la forma «senza zuccheri» mostrava un movimento nuovo e sorprendente alla sua estremità distale. Gli ultimi due segmenti lectinici (chiamati CTLD7 e CTLD8) potevano oscillare verso l’interno formando una punta concava piegata verso l’interno, una conformazione mai osservata nella versione glicosilata, che restava invece più curvata verso l’esterno, ovvero convessa.
Come un piccolo cambiamento rimodella il movimento
Per capire questa differenza, il team ha analizzato i moti dominanti nelle loro simulazioni. Ha scoperto che il movimento principale che distingue le due forme è questa flessione della punta distale, e che essa compare solo quando gli zuccheri sono assenti. La rimozione degli zuccheri rende in generale il recettore più flessibile, specialmente nei segmenti lectinici lontani e, in misura minore, vicino all’estremità N-terminale. Mappe di correlazione di come le diverse parti della proteina si muovono insieme hanno mostrato che, senza zuccheri, gli ultimi due segmenti lectinici si muovono in modo più concertato e sono più strettamente accoppiati ad altre regioni. In sostanza, gli zuccheri non si limitano a stare sulla superficie; contribuiscono a regolare come tutto il braccio si flette e comunica lungo la sua lunghezza.
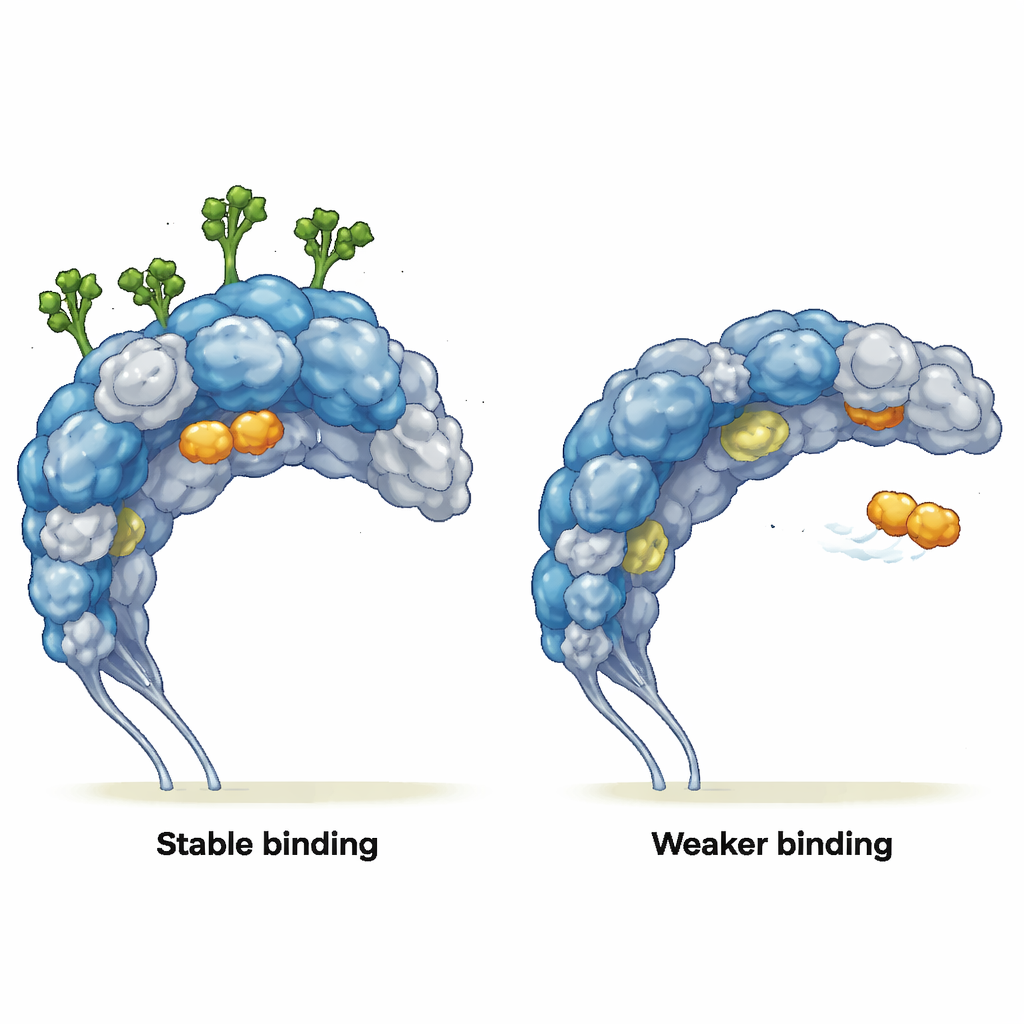
Modificare il modo in cui i partner si legano
Gli autori si sono poi chiesti come questo moto alterato influenzi i partner di legame reali. Hanno simulato le interazioni con due ligandi: un semplice zucchero simile alla mannosa (MMA), che si inserisce in una tasca ben definita, e un peptide che indirizza i tumori chiamato mUNO, che prende di mira i macrofagi associati ai tumori positivi per CD206. Quando erano presenti gli zuccheri, MMA rimaneva comodamente nella sua tasca di legame per tutta la durata della simulazione, mantenendo contatti chiave, sebbene la struttura proteica vicina cambiassero poco. In assenza di zuccheri, MMA sfuggiva dalla tasca, scivolando sulla superficie della proteina e formando solo contatti brevi e superficiali. Per mUNO, il recettore glicosilato mostrava diverse pose di legame stabili con contatti frequenti e duraturi. Nel recettore deglicosilato, il legame di mUNO era più debole e più disperso, e il peptide iniziava anche a esplorare regioni normalmente bloccate dalle catene zuccherine, rivelando nuovi siti di interazione precedentemente nascosti.
Cosa significa per malattia e terapia
Nel complesso, questi risultati mostrano che gli zuccheri attaccati a CD206 agiscono come regolatori remoti della sua forma e della sua adesività. Limitando determinate piegature e organizzando come i suoi segmenti si muovono insieme, la glicosilazione aiuta il recettore a trattenere alcuni ligandi più saldamente e a indirizzarne altri verso siti di ancoraggio preferenziali, oltre a schermare parti della sua superficie. In malattie come il cancro, dove i modelli complessivi di glicosilazione delle proteine sono spesso alterati, CD206 può assumere forme e comportamenti di legame differenti, cambiando il modo in cui le cellule immunitarie percepiscono l’ambiente. Comprendere questo «interruttore conformazionale» dipendente dagli zuccheri non solo chiarisce il funzionamento di CD206, ma suggerisce anche nuovi approcci per progettare farmaci o agenti di imaging che sfruttino il suo paesaggio variabile nei tumori e in altre condizioni patologiche.
Citazione: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Parole chiave: recettore della mannosa, glicosilazione delle proteine, riconoscimento immunitario, macrofagi associati ai tumori, dinamica molecolare