Clear Sky Science · it
Perdita di Snhg5 altera la regolazione del ciclo cellulare senza modificare la cistogenesi in un modello murino della malattia policistica renale
Perché un gene renale con un nome curioso conta
La malattia policistica renale (PKD) è un disturbo ereditario comune in cui innumerevoli sacche piene di liquido lentamente invadono i reni, portando spesso all’insufficienza renale. I ricercatori sanno che difetti in due geni, PKD1 e PKD2, guidano la malattia, ma molti altri fattori genetici possono influenzare la sua velocità di progressione. Questo studio si concentra su un tipo insolito di gene chiamato RNA lungo non codificante, denominato Snhg5, ponendosi una domanda semplice ma importante: questa molecola modella in modo significativo l’evoluzione della PKD, o è per lo più un osservatore?
Uno sguardo più ravvicinato a un messaggero genetico oscuro
A differenza dei geni tipici che forniscono lo schema per le proteine, gli RNA lunghi non codificanti agiscono più come organizzatori molecolari o interruttori all’interno delle cellule. Studi precedenti hanno mostrato che Snhg5 è fortemente aumentato in modelli murini di PKD ed è stato collegato a diversi tumori e a danni renali, suggerendo che potrebbe promuovere una crescita dannosa. I ricercatori hanno prima mappato dove e quando Snhg5 è attivo nei topi normali. Hanno scoperto che è espresso in molti organi, con livelli particolarmente elevati nell’intestino, e che la sua attività nel rene cala nettamente dopo la nascita, quando l’organo passa da una fase di rapida crescita a uno stato più stabile e maturo. All’interno delle cellule renali, quasi tutte le molecole di Snhg5 si trovano nel nucleo, il centro di comando che ospita il DNA, suggerendo che Snhg5 aiuti a controllare l’attività genica piuttosto che a produrre direttamente proteine.
I pattern nei reni malati non raccontano tutta la storia
Il team ha poi confrontato i livelli di Snhg5 in una serie di modelli murini di PKD. Nei modelli a rapida evoluzione, dove le cisti si formano rapidamente, Snhg5 risultava aumentato di due-tre volte nei reni malati, e l’imaging a livello di singola cellula mostrava forti segnali nucleari nelle cellule che rivestono le cisti e nei tessuti circostanti. Sorprendentemente, in un modello murino più lento e più lieve, che ricrea meglio il lungo decorso della PKD umana, Snhg5 non aumentava. Ancora più evidente, nel tessuto renale di persone con PKD autosomica dominante avanzata, l’omologo umano del gene, chiamato SNHG5, risultava in realtà ridotto di oltre il 90 percento. Nel complesso questi risultati suggeriscono che le variazioni di questo RNA accompagnano la formazione delle cisti, ma la direzione e i tempi del cambiamento differiscono tra specie e stadi della malattia, sollevando dubbi sul fatto che Snhg5 da solo sia un motore diretto della crescita cistica.
Cosa succede quando il gene viene rimosso
Per andare oltre la correlazione, i ricercatori hanno usato l’editing genomico CRISPR per eliminare completamente il gene Snhg5 nei topi, creando una linea “knockout” globale. Contrariamente alle preoccupazioni che la rimozione di una molecola così fortemente alterata potesse essere dannosa, i topi privi di Snhg5 sono nati in proporzioni normali, hanno vissuto una vita normale e avevano reni che apparivano e funzionavano come quelli dei loro fratellastri sani. L’esame microscopico ha rivelato una struttura renale normale senza cicatrici o infiammazione, e gli esami del sangue non hanno mostrato segni di filtrazione renale compromessa. A livello molecolare, tuttavia, sono emerse modifiche più sottili: sia i reni dei topi sia le cellule dei tubuli renali coltivate senza Snhg5 mostravano spostamenti coerenti nell’attività di geni legati alla divisione cellulare e alla duplicazione del DNA. in coltura cellulare, un maggior numero di cellule rimaneva bloccato nelle fasi tardive del ciclo cellulare e in uno stato danneggiato, sub-G1. Una proteina in particolare, ARPC5, parte di un complesso che aiuta le cellule a dividersi riorganizzando il loro impalcatura interna, risultava ridotta in assenza di Snhg5, suggerendo una possibile catena di causa-effetto.
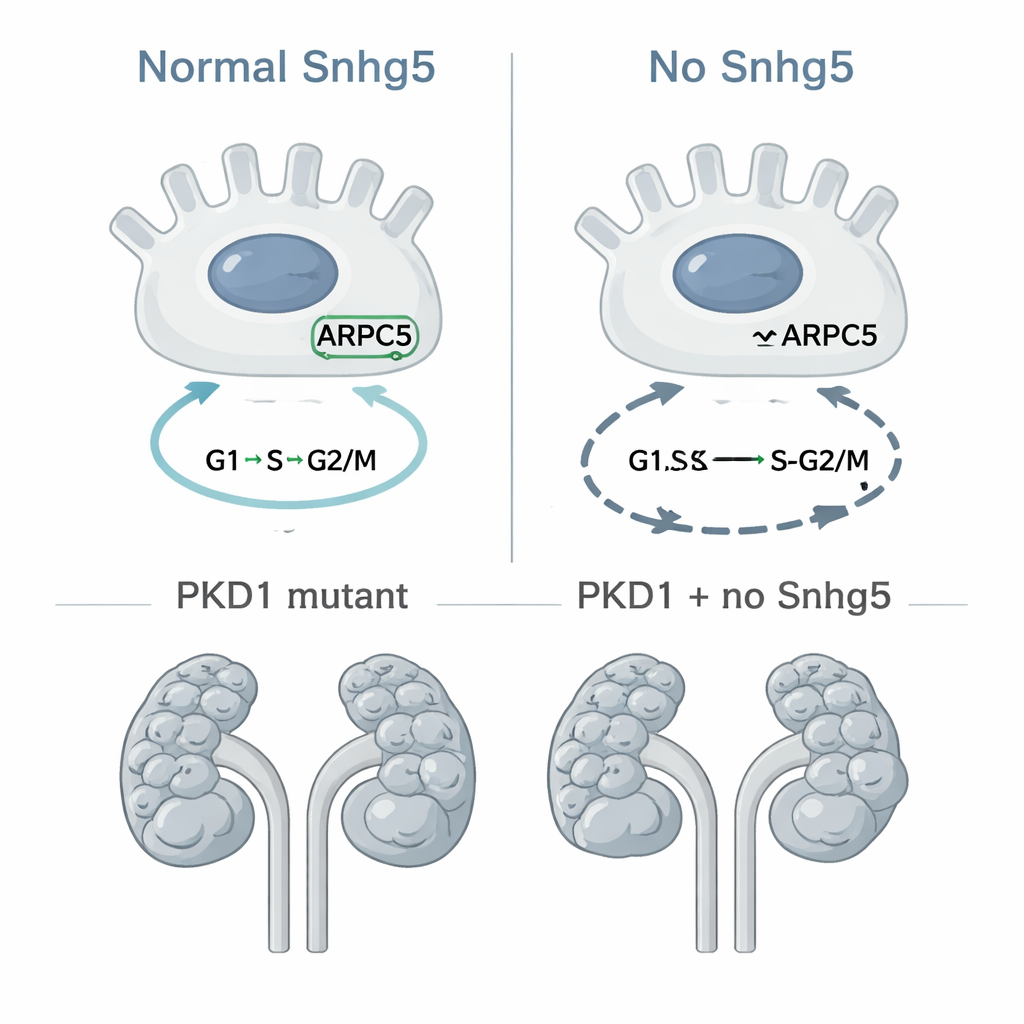
Testarne direttamente il ruolo nella crescita delle cisti
Poiché la divisione cellulare incontrollata è una caratteristica centrale della PKD, il team ha quindi chiesto se la rimozione di Snhg5 rallentasse la formazione delle cisti in un modello murino consolidato in cui il gene PKD1 è disattivato specificamente nelle cellule del dotto collettore, fonte di molte cisti. Hanno incrociato i topi in modo che alcuni presentassero solo la mutazione PKD1, mentre altri mancassero sia di PKD1 sia di Snhg5. All’esame degli animali a 10 giorni di età, entrambi i gruppi mostravano reni gravemente cistici, e misurazioni accurate delle dimensioni renali, dell’area cistica e del numero di cisti non hanno rivelato alcuna protezione significativa dalla delezione di Snhg5. Se mai, i topi doppi-mutanti tendevano ad avere un carico cistico leggermente maggiore, sebbene la differenza fosse piccola e non statisticamente convincente. In altre parole, anche se Snhg5 influenza i geni del ciclo cellulare nelle cellule renali, la sua assenza non modifica in modo evidente la rapidità con cui le cisti compaiono o si ingrandiscono in questo modello specifico di PKD.
Cosa significa per i trattamenti futuri
Per pazienti e sviluppatori di farmaci, la conclusione principale è che Snhg5, nonostante sia uno dei segnali genetici più fortemente alterati nella PKD murina, non è un perno della formazione cistica—almeno non nella fase iniziale e a rapida crescita della malattia derivata dai dotti collettori. Il gene sembra comunque modulare il modo in cui le cellule renali procedono attraverso il ciclo di divisione, probabilmente tramite il suo impatto su fattori come ARPC5, ma questa influenza è abbastanza sottile da lasciare lo sviluppo renale e la progressione precoce della PKD sostanzialmente invariati in caso di perdita completa. Questi risultati sottolineano una lezione più ampia: non ogni cambiamento molecolare evidente nei tessuti malati rappresenta un bersaglio terapeutico promettente. Per distinguere causa e conseguenza sarà necessario testare RNA lunghi non codificanti come Snhg5 in molteplici modelli di malattia e in diversi momenti prima di poterli perseguire con sicurezza come candidati farmacologici.
Citazione: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Parole chiave: malattia policistica renale, RNA lungo non codificante, Snhg5, ciclo cellulare, cisti renali