Clear Sky Science · it
Nanocapsule a base di chitosano e destra solfato per migliorare l’efficacia della tigeciclina contro Salmonella enterica non tifoidea
Perché questo è importante per la sicurezza alimentare
La maggior parte delle persone conosce Salmonella come una causa spiacevole di intossicazione alimentare, spesso associata a pollame poco cotto. Meno persone sanno che alcuni ceppi sono diventati così resistenti agli antibiotici che anche farmaci potenti di “ultima risorsa” possono fallire. Questo studio esplora un approccio basato sulla nanotecnologia per recuperare uno di questi farmaci, la tigeciclina, confezionandolo all’interno di minuscole capsule a base di zucchero che ne facilitano l’ingresso nelle cellule infette e disattivano i principali meccanismi di resistenza in Salmonella.
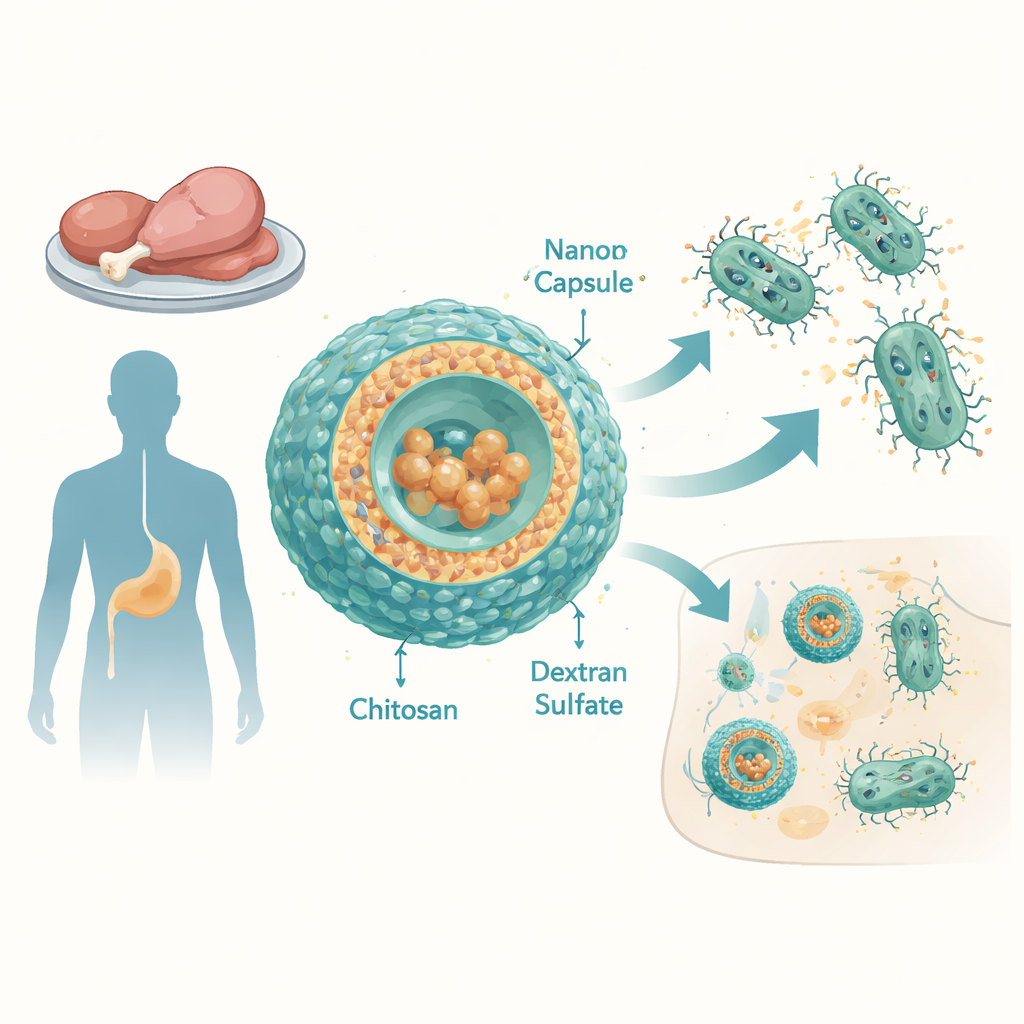
La minaccia crescente delle Salmonella resistenti
I sierotipi di Salmonella non tifoidea (NTS) sono una delle principali cause di diarrea e infezioni ematiche a livello mondiale, specialmente nei paesi a basso e medio reddito. I ricercatori hanno esaminato 12 ceppi di Salmonella enterica isolati da carne di pollo e anatra in Egitto. Questi ceppi erano resistenti a molti antibiotici comunemente usati, inclusi penicilline, cefalosporine, tetracicline e altri, e mostravano punteggi elevati di resistenza multipla. Anche la tigeciclina, un farmaco a largo spettro riservato ai casi difficili, funzionava male: i batteri tolleravano concentrazioni molto alte. Una ragione principale era l’iperattività delle “pompe di efflusso” — macchine molecolari nella membrana batterica che espellono continuamente gli antibiotici dalla cellula.
Costruire una capsula farmacologica più intelligente
Per superare questo problema, il team ha progettato capsule su scala nanometrica fatte di due polimeri di origine naturale: chitosano, ottenuto dalla chitina (il materiale nei gusci dei crostacei), e destra solfato, una molecola zuccherina ramificata. Ottimizzando accuratamente le proporzioni di questi componenti, hanno ottenuto particelle stabili di circa 100–150 nanometri di diametro, con una carica superficiale positiva che favorisce l’interazione con le membrane batteriche e delle cellule ospiti. La tigeciclina è stata caricata in queste particelle con un’efficienza notevolmente elevata — praticamente tutto il farmaco è finito dentro le capsule. Nei test in vitro che simulavano le condizioni ematiche, le capsule hanno rilasciato la maggior parte della tigeciclina nell’arco di poche ore, suggerendo la capacità di somministrare un forte rilascio di antibiotico nei siti di infezione.
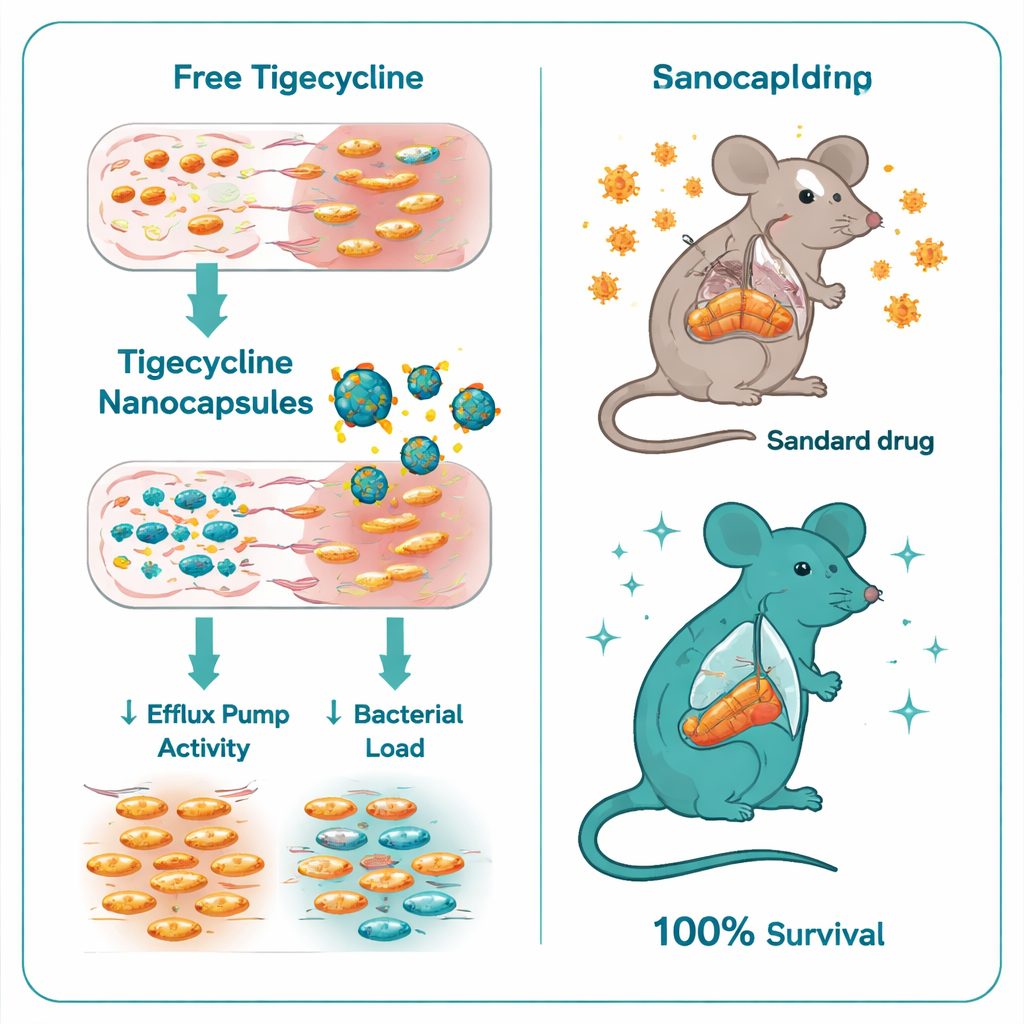
Indebolire le difese batteriche
Quando i ricercatori hanno confrontato la tigeciclina libera con la tigeciclina incapsulata nei nanocapsule chitosano–destra solfato, la differenza è stata marcata. La concentrazione minima di farmaco necessaria per arrestare la crescita batterica è passata da 32–128 microgrammi per millilitro per la tigeciclina libera a soli 0,5–1 microgrammi per millilitro con le nanocapsule — un miglioramento di sei‑/sette volte. Esperimenti di time‑kill hanno mostrato che la forma incapsulata uccideva Salmonella molto più rapidamente e in modo più completo. A livello genetico, le nanocapsule hanno anche silenziato regolatori chiave della resistenza: l’espressione dei geni ramA e acrB, che controllano e costituiscono importanti pompe di efflusso, è diminuita di diverse volte nei batteri trattati. In altre parole, le capsule non si limitavano a portare più farmaco; contribuivano a spegnere una delle principali vie di fuga dei batteri.
Proteggere i topi infetti dalla malattia letale
Successivamente il team ha testato la nuova formulazione in un modello murino di grave infezione da Salmonella Typhimurium. I topi infetti non trattati morivano tutti entro otto giorni. I topi trattati con tigeciclina standard andavano meglio ma mostravano comunque alta mortalità, con solo il 40% di sopravvivenza. Al contrario, tutti i topi trattati con le nanocapsule cariche di tigeciclina sono sopravvissuti. Questi animali avevano molti meno batteri nel fegato e nell’intestino, esami del sangue con parametri di funzione epatica e renale più vicini alla normalità e danni tissutali molto più lievi all’esame microscopico. Anche le capsule “vuote” di chitosano–destra solfato, senza antibiotico, hanno offerto una certa protezione, probabilmente perché il chitosano possiede modesti effetti antimicrobici e antinfiammatori, ma la combinazione con la tigeciclina è risultata chiaramente superiore.
Cosa potrebbe significare per i trattamenti futuri
Per i non specialisti, il messaggio principale è che confezionare un antibiotico esistente all’interno di una nanocapsula intelligente e biocompatibile può ridare efficacia contro Salmonella altamente resistente. Facilitando l’accesso del farmaco ai batteri che si nascondono dentro le cellule e attenuando le pompe che normalmente espellono il farmaco, il sistema chitosano–destra solfato ha trasformato un antibiotico di ultima istanza in difficoltà in un trattamento altamente efficace nei topi, con il 100% di sopravvivenza. Pur richiedendo ulteriori studi prima di poter essere impiegato nell’uomo o negli animali da allevamento, questa strategia offre una via promettente per prolungare la vita utile di antibiotici importanti e migliorare la sicurezza della filiera alimentare senza dover inventare ex novo nuovi farmaci.
Citazione: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Parole chiave: Salmonella, resistenza agli antibiotici, nanoparticelle, somministrazione di farmaci, tigeciclina