Clear Sky Science · it
Proteomica e metabolomica integrate rivelano che le lattoni sesquiterpenici vegetali inibiscono l’attività delle cellule TNBC esaurendo la sintesi di ATP e riprogrammando il metabolismo primario
Composti vegetali che affamano il cancro mammario aggressivo
Il carcinoma mammario triplo negativo è una delle forme di cancro al seno più difficili da trattare perché manca dei recettori ormonali “maniglie” a cui molti farmaci si legano. Questo studio esplora due molecole estratte da una pianta medicinale che sembrano spegnere le centrali energetiche interne di queste cellule tumorali, interrompendone l’approvvigionamento di energia mentre risparmiano le cellule mammarie normali. Capire come funziona questo meccanismo potrebbe aprire la strada a trattamenti più mirati e meno tossici per pazienti che oggi hanno opzioni limitate.
Perché colpire la fonte di energia del cancro è importante
Ogni cellula dipende da piccole strutture chiamate mitocondri per produrre ATP, il carburante di base della cellula. Le cellule tumorali, soprattutto quelle aggressive, spesso dipendono in modo anomalo dai mitocondri per sostenere la crescita rapida, la diffusione e la sopravvivenza sotto stress. I ricercatori si sono concentrati sulle cellule di carcinoma mammario triplo negativo, che costituiscono circa il 15–20% dei tumori al seno e tendono a recidivare e metastatizzare più spesso di altri tipi. Hanno studiato una molecola naturale, la deossielefantopina (DET), e la sua variante raffinata DETD‑35, entrambe lattoni sesquiterpenici provenienti dalla pianta medicinale Elephantopus. Lavori precedenti avevano mostrato che questi composti inducono stress ossidativo e forme atipiche di morte cellulare nelle cellule tumorali, ma non era ben compreso come disturbassero le “fabbriche” energetiche cellulari.
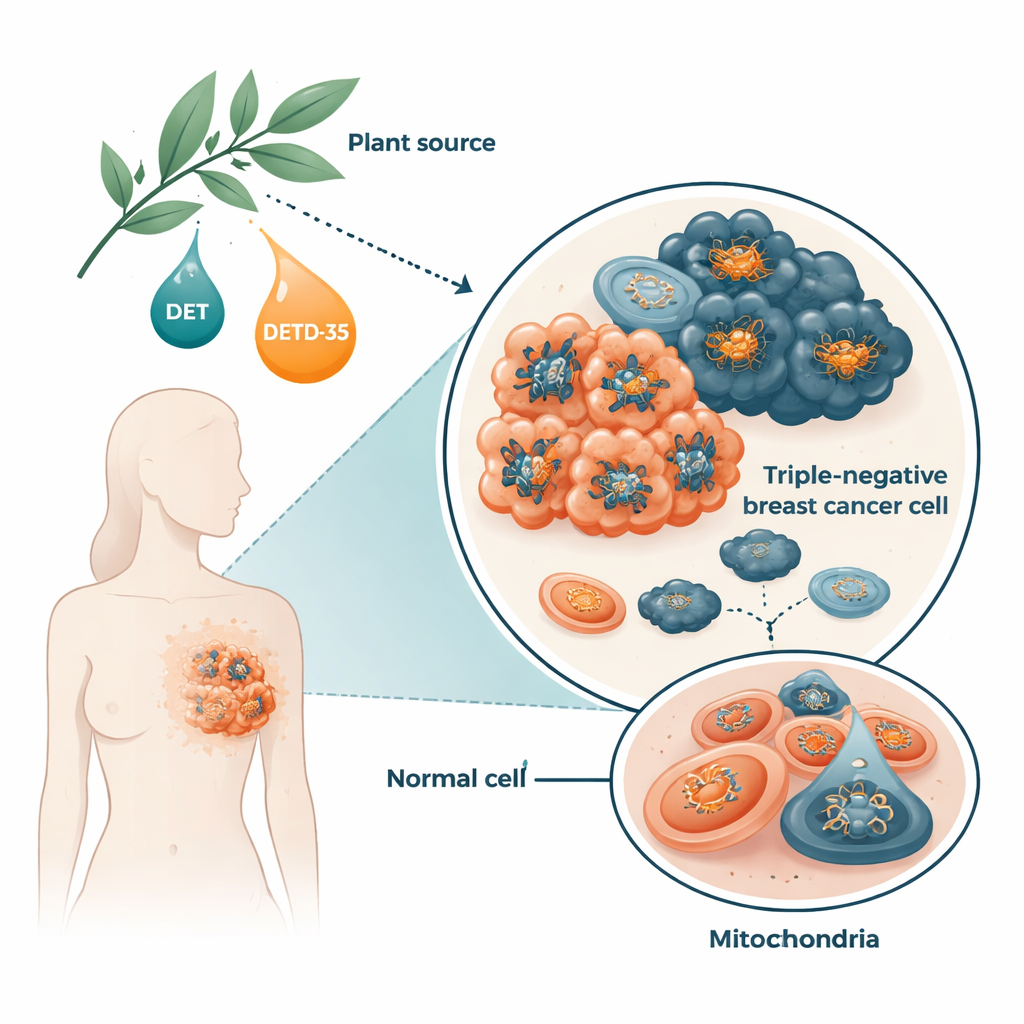
Come le molecole vegetali compromettono i mitocondri delle cellule tumorali
Utilizzando cellule umane di carcinoma mammario triplo negativo coltivate in laboratorio, il gruppo ha scoperto che DET e DETD‑35 aumentano rapidamente la produzione di specie reattive dell’ossigeno, un tipo di “scarico” chimico generato durante la produzione di energia. In risposta, le cellule incrementano alcuni enzimi protettivi, ma non abbastanza da ripristinare l’equilibrio. I composti forzano inoltre l’apertura di un canale nella membrana mitocondriale noto come poro di transizione della permeabilità, un cambiamento collegato a rigonfiamento, perdita del potenziale di membrana e alle fasi iniziali della morte cellulare. Nell’arco di poche ore, i livelli di ATP all’interno delle cellule tumorali diminuiscono drasticamente. Quando i ricercatori hanno pretrattato con un antiossidante, questi effetti dannosi sono stati in gran parte invertiti, dimostrando che lo stress ossidativo è una componente chiave del processo.
Mappare il danno a proteine e metabolismo
Per comprendere il quadro generale, gli scienziati hanno combinato due potenti approcci “omici”. Hanno catalogato migliaia di proteine mitocondriali e misurato numerosi piccoli metaboliti in cellule trattate rispetto a quelle non trattate. Questa visione integrata ha rivelato che DET e DETD‑35 perturbano proteine coinvolte nella fosforilazione ossidativa, il principale percorso mitocondriale per la produzione di ATP, e attivano segnali legati alla morte cellulare. Allo stesso tempo, i percorsi metabolici centrali che gestiscono aminoacidi, lipidi e i mattoni per il DNA sono stati riprogrammati. Alcuni lipidi che contribuiscono a modellare la membrana interna mitocondriale, così come molecole legate alle difese antiossidanti e alla degradazione degli zuccheri, sono variate in modi coerenti con cellule tumorali sotto stress e povere di energia. Elemento cruciale: questi cambiamenti diffusi non sono stati osservati nelle cellule mammarie normali esposte alle stesse dosi, suggerendo un certo grado di selettività per le cellule tumorali.
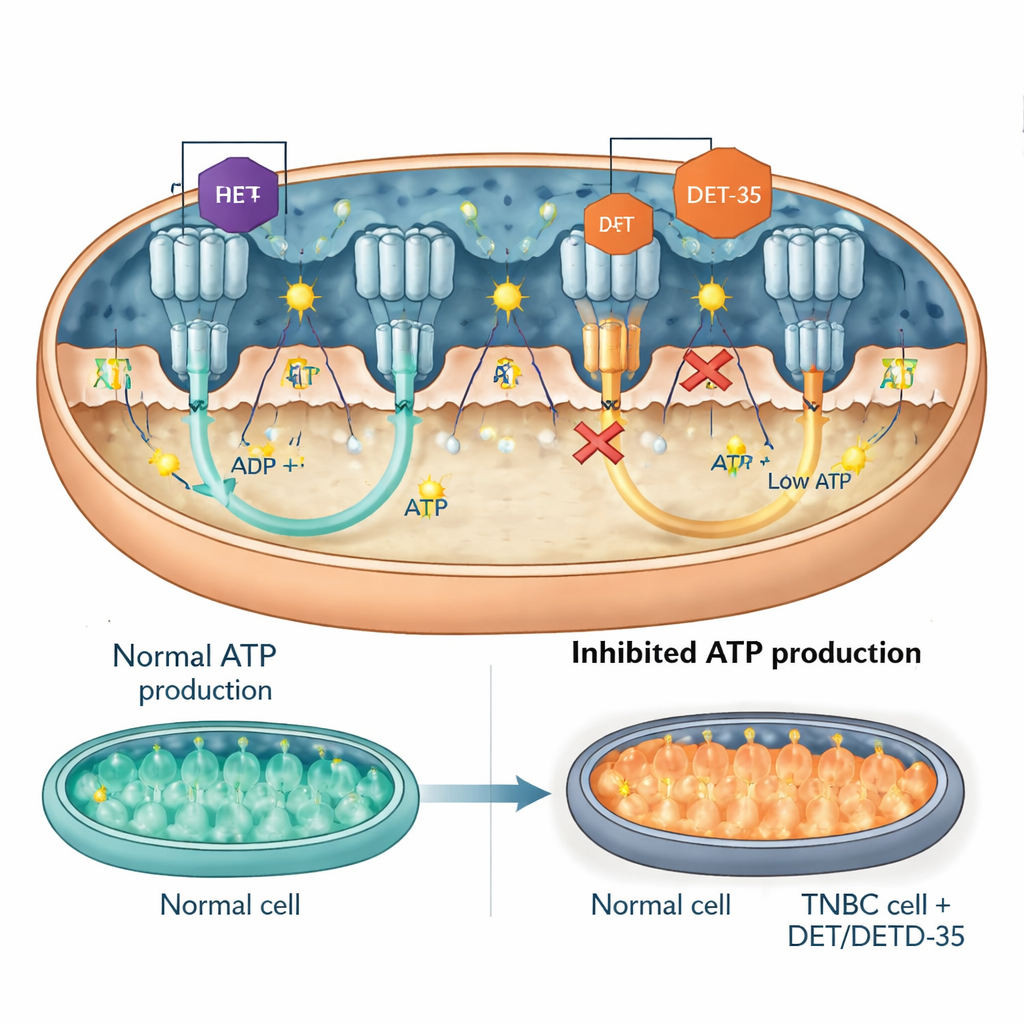
Una proteina di segnalazione chiave e la turbina dell’ATP stessa
Il team si è poi concentrato su attori specifici all’interno di queste reti alterate. Uno è PRKCA, una proteina di segnalazione che può trasferirsi nei mitocondri e influenzare sia la produzione di energia sia le risposte allo stress. DET e DETD‑35 aumentano i livelli di PRKCA nelle cellule tumorali. Quando i ricercatori hanno ridotto l’espressione di PRKCA con strumenti genetici, la tossicità dei farmaci è diminuita: le cellule tumorali avevano maggiori probabilità di sopravvivere, producevano più ATP e mostravano meno segni di malfunzionamento mitocondriale e apoptosi. Un altro bersaglio è stata l’ATP sintasi, la “turbina” molecolare che ruota per generare ATP. Le misurazioni hanno mostrato che DET e DETD‑35 riducono direttamente l’attività dell’ATP sintasi nei mitocondri delle cellule tumorali. Modelli di docking al computer hanno suggerito che entrambi i composti si alloggiano in interfacce critiche dell’enzima, le stesse regioni generali dove si legano noti inibitori dell’ATP sintasi, ostacolandone fisicamente il movimento e riducendo la produzione di ATP. In modelli murini con tumori umani triplo negativi, il trattamento con uno dei due composti ha abbassato i livelli delle componenti dell’ATP sintasi nel tessuto tumorale, a sostegno dei risultati osservati in coltura cellulare.
Cosa potrebbe significare per i futuri trattamenti del cancro
Nel complesso, lo studio delinea un quadro coerente: questi composti di origine vegetale spingono le cellule di carcinoma mammario triplo negativo in una crisi energetica sovraccaricandole di stress ossidativo, aprendo i pori mitocondriali e bloccando direttamente la macchina che produce ATP. Con l’ATP che si esaurisce e il metabolismo disorganizzato, le cellule tumorali perdono la capacità di crescere e sopravvivere, mentre le cellule mammarie normali rimangono in gran parte indenni alle stesse condizioni. Per un lettore non specialistico, il messaggio è che gli scienziati potrebbero sfruttare la forte dipendenza del cancro dalle sue “centrali” interne, usando molecole progettate con cura—alcune ispirate alle piante—per scaricare le batterie delle cellule tumorali senza staccare la spina ai tessuti sani. Serve ancora molto lavoro prima che tali agenti possano arrivare in clinica, ma questa visione integrata di proteine, metaboliti e flusso energetico offre una strada promettente.
Citazione: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Parole chiave: carcinoma mammario triplo negativo, mitocondri, ATP sintasi, prodotti naturali, metabolismo del cancro