Clear Sky Science · it
Batteri presenti negli alimenti e microbiota intestinale producono metilgliossale e questo metabolita porta alla formazione di alcaloidi bioattivi 1‑acetil‑β‑carboline
Perché il laboratorio chimico del tuo intestino conta
All’interno del nostro intestino e in molti alimenti fermentati, trilioni di batteri trasformano continuamente gli zuccheri che mangiamo in una serie di sottoprodotti chimici. Questo studio esplora in dettaglio una di queste vie: come alcuni batteri comuni convertono gli zuccheri in un composto altamente reattivo chiamato metilgliossale, e poi in una famiglia di molecole bioattive chiamate 1‑acetil‑β‑carboline. Poiché queste sostanze sono collegate sia a processi patologici sia a potenziali nuovi farmaci, comprendere quando e come i batteri le producono potrebbe cambiare il nostro modo di pensare al cibo, al microbioma e alla salute.
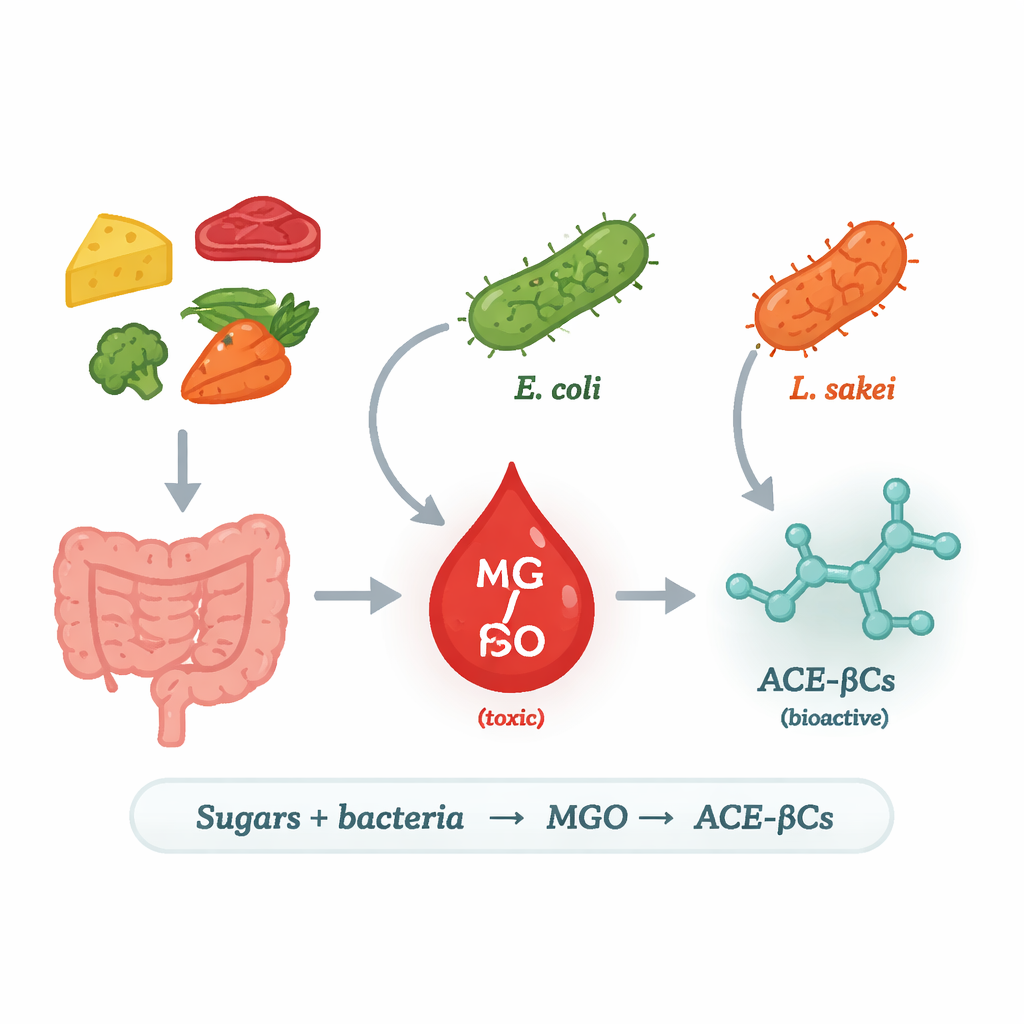
Dagli zuccheri quotidiani a una molecola rischiosa
I ricercatori si sono concentrati sul metilgliossale (MGO), un sottoprodotto molto reattivo e tossico della degradazione degli zuccheri. Negli esseri umani l’eccesso di MGO è associato a diabete, malattie cardiovascolari e neurodegenerazione perché può danneggiare proteine e DNA. Le nostre cellule normalmente controllano il MGO mediante sistemi di detossificazione, ma non sono l’unica fonte: anche i batteri possono produrlo. In alcuni microrganismi un enzima chiamato methylglyoxal synthase (MgsA) converte un intermedio del metabolismo degli zuccheri direttamente in MGO, creando una “scorciatoia” nel metabolismo energetico. Il gruppo ha indagato quali batteri alimentari e intestinali usano questa via, in quali condizioni e cosa accade al MGO che rilasciano.
Chi sono i produttori batterici?
Per rispondere, gli scienziati hanno coltivato diversi ceppi di batteri lattici spesso presenti negli alimenti, insieme a un ceppo di laboratorio di Escherichia coli, in un mezzo controllato contenente glucosio o galattosio. Hanno quindi monitorato nel tempo il MGO e due alcaloidi correlati nel liquido di coltura usando cromatografia ad alta precisione e spettrometria di massa. Solo E. coli e la specie associata alla carne Lactilactobacillus sakei hanno prodotto quantità significative di MGO e degli alcaloidi; gli altri batteri lattici testati non l’hanno fatto. Una ricerca genomica ha rivelato la differenza chiave: E. coli e L. sakei possiedono il gene per MgsA, mentre la maggior parte dei loro parenti lattici non ce l’ha. Quando i ricercatori hanno inserito il gene mgsA di L. sakei in un ceppo non produttore, quel batterio ingegnerizzato ha cominciato a produrre sia MGO sia gli alcaloidi, collegando in modo netto MgsA a questa via.
Come il MGO tossico diventa alcaloidi bioattivi
La domanda successiva era cosa accade al MGO una volta prodotto. Il gruppo si è concentrato sugli alcaloidi 1‑acetil‑β‑carboline (ACE‑βC), piccole molecole con attività antibatterica, antiinfiammatoria e antitumorale riportate in letteratura. Hanno mostrato che quando i batteri produttori di MGO venivano coltivati in presenza dell’amminoacido L‑triptofano, i livelli di due ACE‑βC — 1‑acetil‑β‑carbolina e la sua forma 3‑carbossilica — aumentavano nettamente. L’aggiunta di MGO extra al mezzo ha aumentato anch’essa la loro formazione. Ciò indica che il MGO fuoriesce dalle cellule e reagisce spontaneamente con il L‑triptofano nel liquido circostante, senza enzimi aggiuntivi, generando queste molecole bioattive. In altre parole, la stessa chimica che rende il MGO pericoloso lo trasforma anche in composti più complessi che possono avere effetti utili.
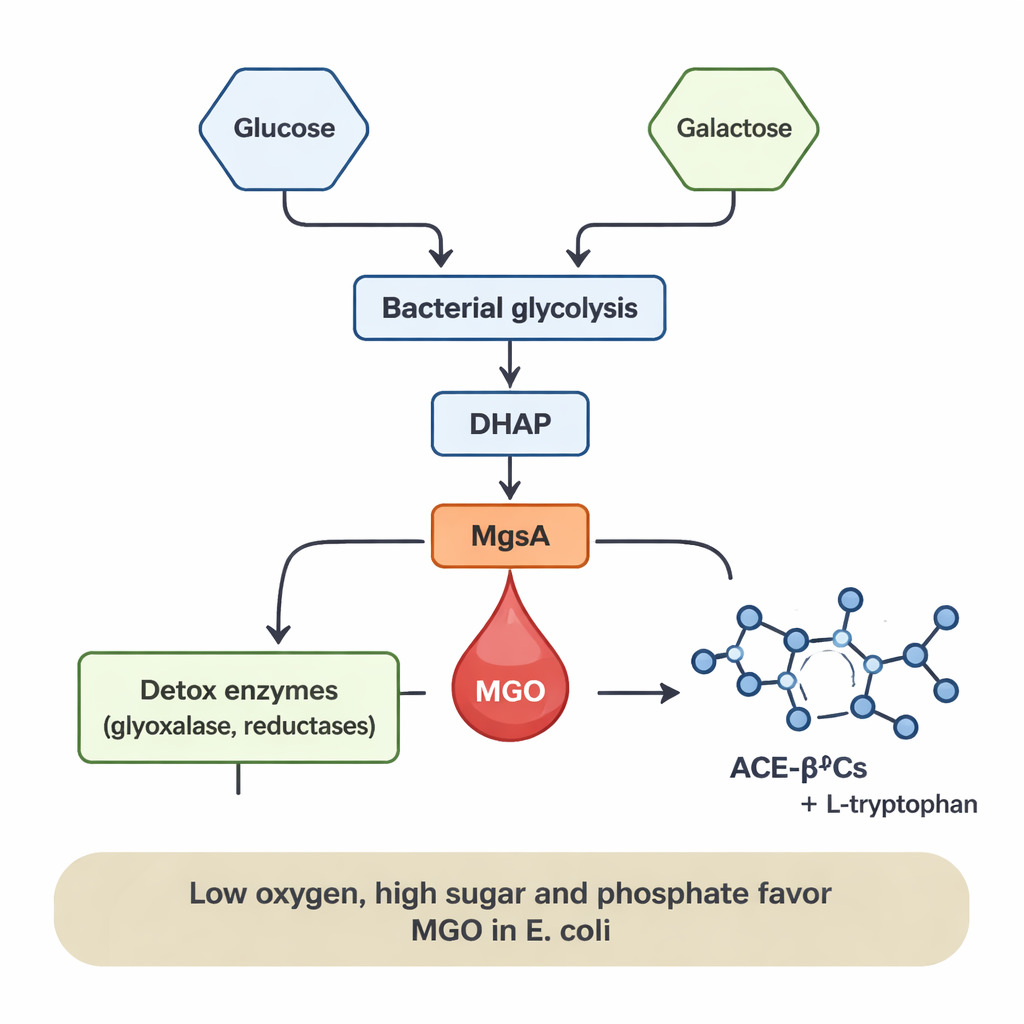
Che cosa alza o abbassa la produzione
La produzione di MGO non era fissa; dipendeva fortemente dalla dieta e dall’ambiente batterico. In E. coli il MGO è comparso solo in presenza di glucosio, e i suoi livelli sono aumentati con la concentrazione di glucosio. L’aggiunta di fosfato, un nutriente minerale comune, ha amplificato ulteriormente la formazione di MGO di diversi ordini di grandezza, probabilmente perché favorisce l’accumulo di intermedi zuccherini fosforilati che alimentano la scorciatoia mediata da MgsA. Condizioni a basso ossigeno (anaerobiche) — simili a quelle nell’intestino umano — hanno inoltre favorito il rilascio di MGO, mentre condizioni ben ossigenate lo hanno fortemente ridotto, nonostante i batteri crescessero comunque bene. Al contrario, L. sakei ha generato principalmente MGO quando coltivata su galattosio, e la produzione aumentava con livelli più elevati di galattosio. Questi schemi suggeriscono che quando il flusso di zuccheri attraverso il metabolismo batterico è intenso e l’ossigeno è limitato, il MGO può agire come una “valvola di sfogo”, alleviando la pressione dell’accumulo di intermedi zuccherini.
Quali implicazioni per cibo e salute
I risultati suggeriscono che non tutti i batteri del cibo o dell’intestino sono uguali nella loro capacità di produrre MGO e ACE‑βC. Specie che possiedono l’enzima MgsA, come alcuni ceppi di L. sakei e E. coli, possono essere contributori significativi, soprattutto in contesti ricchi di zuccheri e poveri di ossigeno come l’intestino o alcune fermentazioni. Il MGO che espellono potrebbe aumentare il carico chimico complessivo sui tessuti dell’ospite, ma la sua conversione in alcaloidi ACE‑βC potrebbe anche in parte “smaltire” questo composto reattivo generando al contempo molecole con effetti biologici propri. Anche se lo studio è stato condotto in colture di laboratorio, mette in luce una via plausibile attraverso la quale dieta, composizione del microbiota e metabolismo batterico insieme modellano l’equilibrio tra sostanze dannose e potenzialmente benefiche nel nostro organismo, e indica gli ACE‑βC come possibili marcatori della produzione batterica di MGO negli alimenti e nell’intestino.
Citazione: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Parole chiave: microbiota intestinale, metilgliossale, metabolismo batterico, fermentazione alimentare, alcaloidi beta-carboline