Clear Sky Science · it
Derivazione di un biomarcatore di attività cerebrale intrinseca per la previsione più precoce del declino cognitivo
Perché i cambiamenti cerebrali precoci sono importanti
Molti anziani notano lievi vuoti di memoria molto prima che un medico possa diagnosticare una demenza. In questa fase, le scansioni cerebrali standard e gli esami del sangue spesso risultano normali, eppure il processo patologico sottostante può essere già in corso. Questo studio indaga se un semplice test non invasivo delle onde cerebrali — l’elettroencefalogramma, o EEG — possa rivelare cambiamenti molto precoci nella funzione cerebrale e prevedere in modo affidabile chi è più probabile che vada incontro a un declino cognitivo consistente negli anni successivi.
Ascoltare i segnali silenziosi del cervello
I ricercatori si sono concentrati su persone con «declino cognitivo soggettivo» (SCI): anziani che percepiscono un peggioramento della memoria ma che ottengono risultati normali nei test standard. Ottantotto volontari di età compresa tra 52 e 85 anni hanno effettuato 20 minuti di EEG a riposo con gli occhi chiusi e sono stati poi seguiti per 5–7 anni. Durante il follow-up, i medici hanno monitorato lo stato cognitivo di ciascuno usando scale di valutazione consolidate. Alla fine del periodo, alcuni partecipanti sono rimasti stabili, mentre altri sono peggiorati fino a un deterioramento cognitivo lieve o hanno sviluppato demenza. Questi esiti hanno permesso al team di valutare se pattern sottili nell’EEG iniziale avrebbero potuto prevedere chi si sarebbe poi deteriorato.
Trasformare le onde cerebrali in un’impronta predittiva
Invece di esaminare l’EEG visivamente, il gruppo ha impiegato l’EEG quantitativo (qEEG), che converte le onde cerebrali grezze in migliaia di caratteristiche numeriche. Queste caratteristiche descrivono l’intensità di diverse bande di frequenza (come i ritmi alfa e theta), quanto efficacemente regioni cerebrali distanti si sincronizzano tra loro (connettività e fase ritardata) e quanto complesso o disorganizzato appare il pattern di attività complessivo. Poiché l’invecchiamento normale altera anch’esso l’EEG, i ricercatori hanno correttamente adattato matematicamente tutte le caratteristiche per l’età e le hanno poi standardizzate in modo che “zero” rappresentasse il valore atteso per una persona sana della stessa età. Per evitare l’overfitting, hanno ridotto sistematicamente oltre 6.000 misure candidate a un set compatto di caratteristiche stabili, non ridondanti e migliori nel separare chi sarebbe rimasto stabile da chi sarebbe peggiorato.
Il machine learning come sfera di cristallo
Con questo set di caratteristiche ridotto, il team ha addestrato diversi modelli di apprendimento automatico — regressione logistica, macchine a vettori di supporto e foreste casuali — per stimare la probabilità che ogni partecipante subisse un declino futuro. Sono state usate ripetute procedure di cross-validation e un metodo bootstrap specializzato per valutare le prestazioni nel modo più realistico possibile. Tra i modelli, l’accuratezza predittiva è stata di circa l’80%, con un’area sotto la curva ROC (AUC) attorno a 0,90, indice di una forte capacità discriminativa tra individui stabili e in declino. I modelli finali bloccati utilizzavano solo 14 caratteristiche qEEG, per lo più provenienti da regioni frontali registrate con un piccolo set di elettrodi, rendendo l’approccio pratico per un uso clinico di routine.
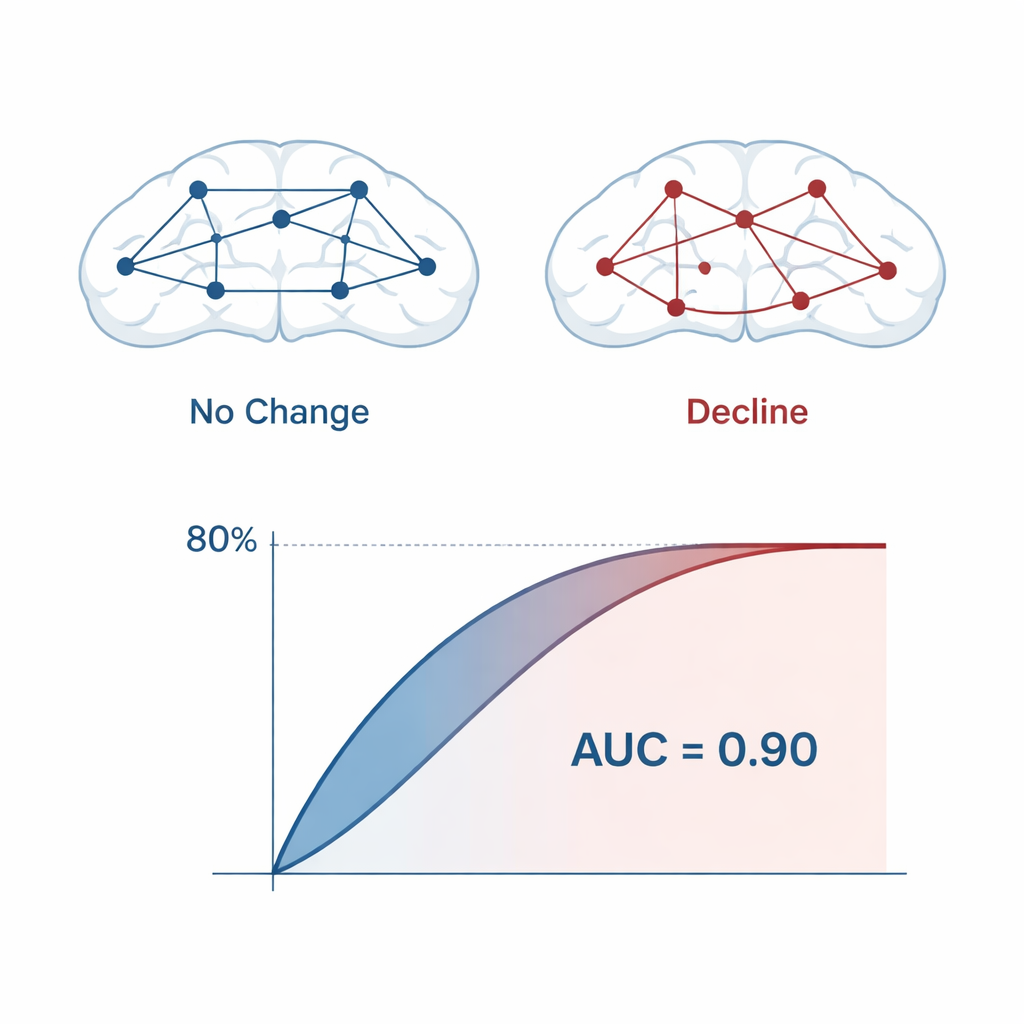
Cosa sta cambiando nel cervello
Le caratteristiche maggiormente responsabili della previsione accurata indicavano una precoce interruzione del modo in cui le aree cerebrali comunicano tra loro. Misure di connettività, in particolare il phase lag e l’asimmetria tra le regioni frontali sinistra e destra, sono state centrali nel modello. Anomalie nelle bande di frequenza alfa e theta spiccavano: un aumento o uno spostamento dell’attività theta è stato associato in altre ricerche ad atrofia dell’ippocampo e assottigliamento corticale, mentre cambiamenti nella potenza e nella frequenza alfa possono riflettere i primi tentativi del cervello di compensare il danno emergente. È importante notare che nessuna singola misura EEG racconta l’intera storia. È stata la combinazione specifica — l’«impronta» del biomarcatore — a segnalare un rischio aumentato anni prima della comparsa dei sintomi conclamati.
Mettere lo strumento alla prova nel mondo reale
Per verificare se il loro biomarcatore si generalizzasse oltre il gruppo iniziale, i ricercatori lo hanno testato su due coorti indipendenti provenienti dagli Stati Uniti e dall’Italia, ciascuna con propri dispositivi di registrazione e caratteristiche dei pazienti. Come prevedibile su dati realmente nuovi, l’accuratezza è diminuita modestamente, attestandosi intorno al 60–70%, ma il modello ha comunque mostrato prestazioni molto superiori al caso, suggerendo che il segnale catturato è robusto. Il team ha inoltre dimostrato che i clinici possono regolare la soglia decisionale: abbassandola si aumenta la sensibilità (identificando più futuri declinanti a fronte di più falsi allarmi), mentre alzandola si aumenta la specificità (meno falsi positivi ma più casi mancati). Questa flessibilità consente di adattare lo strumento alle diverse priorità cliniche.
Cosa significa per pazienti e clinici
In termini semplici, questo lavoro suggerisce che una breve registrazione EEG indolore — utilizzando solo pochi elettrodi sulla fronte — può contribuire a individuare anziani che oggi appaiono normali ma che presentano un alto rischio di declino cognitivo nei prossimi anni. Pur necessitando di studi più ampi e di confronti con altri biomarcatori, l’approccio è economico, non invasivo e ripetibile, il che lo rende interessante per screening diffusi, specialmente in contesti dove imaging avanzato o analisi del liquido cerebrospinale sono impraticabili. Se ulteriormente convalidati, biomarcatori EEG di questo tipo potrebbero aiutare i medici a intervenire prima, monitorare la progressione della malattia e selezionare partecipanti per trial clinici proprio nella fase in cui i trattamenti hanno maggiori possibilità di produrre un effetto durevole.
Citazione: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Parole chiave: previsione precoce della demenza, onde cerebrali EEG, declino cognitivo soggettivo, biomarcatore con apprendimento automatico, rischio di Alzheimer