Clear Sky Science · it
Classificazione dei globuli bianchi tramite rete neurale profonda personalizzata e visualizzazione delle caratteristiche delle immagini con heatmap
Perché test ematici più intelligenti sono importanti
Un esame del sangue di routine può rivelare segnali precoci di infezione, allergia o persino tumore—ma oggi gran parte di queste informazioni dipendono ancora dall’ispezione attenta degli esperti al microscopio. Questo processo è lento, costoso e non sempre disponibile in cliniche più piccole o ospedali rurali. L’articolo descritto qui presenta un sistema d’intelligenza artificiale compatto in grado di riconoscere con precisione diversi tipi di globuli bianchi a partire da immagini al microscopio, potenzialmente portando analisi del sangue più rapide e affidabili a molti più pazienti.
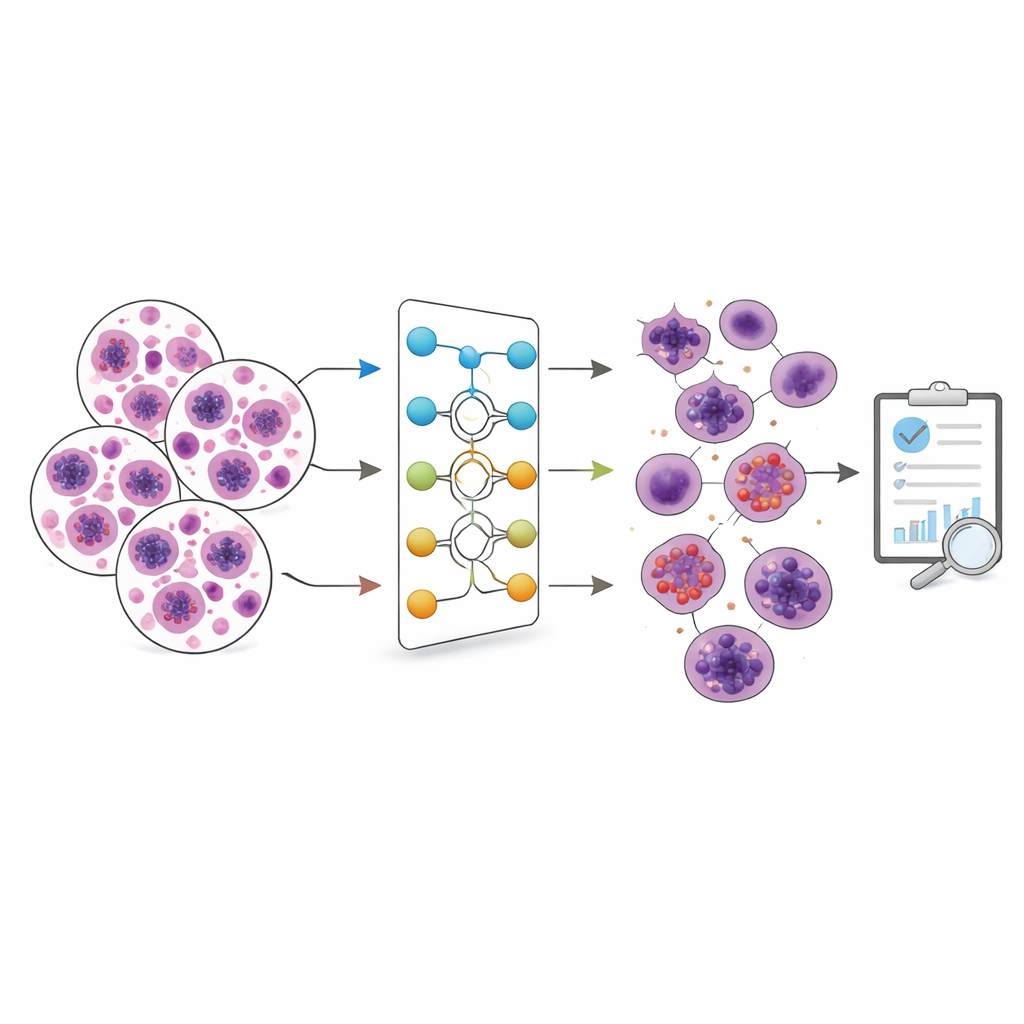
I piccoli difensori del corpo
I globuli bianchi sono le prime linee di difesa del corpo contro germi e altre minacce. Ci sono diverse varianti principali, ognuna con un ruolo diverso: alcuni attaccano batteri, altri combattono parassiti, rispondono alle allergie o contribuiscono a coordinare l’immunità a lungo termine. I medici osservano spesso sia il numero sia il tipo di queste cellule per diagnosticare malattie e monitorare i trattamenti. Oggi questo viene fatto comunemente o tramite conteggio manuale al microscopio—un compito che richiede abilità e tempo—o tramite grandi macchine automatizzate che molti laboratori più piccoli non possono permettersi.
Dal conteggio manuale agli “occhi” digitali
Nell’ultimo decennio i ricercatori si sono rivolti alla visione artificiale e al machine learning per automatizzare l’identificazione dei globuli bianchi. Programmi di base possono misurare forme e colori, mentre sistemi più avanzati usano l’apprendimento profondo, che è in grado di apprendere pattern complessi direttamente dalle immagini. Tuttavia, molti modelli di deep learning potenti sono enormi, richiedono notevole potenza di calcolo e memoria, e possono soffrire di problemi di addestramento come lo “svanimento” dei segnali all’interno della rete. Questo ne limita l’uso in cliniche piccole, dispositivi sanitari mobili o ospedali con risorse informatiche modeste.
Un microscopio digitale snello ma potente
Gli autori introducono un modello di deep learning snello che chiamano rete neurale profonda personalizzata, o CDNN. È progettato specificamente per riconoscere i globuli bianchi nelle immagini al microscopio. Il modello è stato addestrato e testato su due dataset popolari di immagini di cellule del sangue: uno grande e leggermente sbilanciato (Raabin WBC) con cinque tipi di globuli bianchi, e un altro più piccolo ma bilanciato (BCCD) con quattro tipi. Prima dell’addestramento, tutte le immagini sono state ridimensionate, normalizzati i livelli di luminosità e quindi leggermente alterate—ruotate, riflesse e shearate—per imitare la variazione naturale e ridurre l’overfitting, che si verifica quando un modello memorizza gli esempi di training invece di apprendere pattern generali.
Dentro il “processo di pensiero” del modello
CDNN è costruito da una serie di blocchi costitutivi che gli permettono di apprendere in modo efficace mantenendo la compattezza. Questi blocchi includono connessioni “residuali” che consentono alle informazioni di bypassare alcuni strati, evitando che i segnali di addestramento si affievoliscano mentre attraversano la rete. Il modello aumenta gradualmente il numero di filtri interni man mano che le immagini lo attraversano, catturando sia dettagli fini sia forme più ampie del nucleo cellulare e del materiale circostante. Nonostante abbia molti meno parametri rispetto a modelli di immagini noti come VGG16 o ResNet-50, CDNN raggiunge un’accuratezza molto elevata: circa il 98% sul dataset Raabin e quasi il 99,6% sul dataset BCCD, superando molte metodologie di stato dell’arte più grandi.
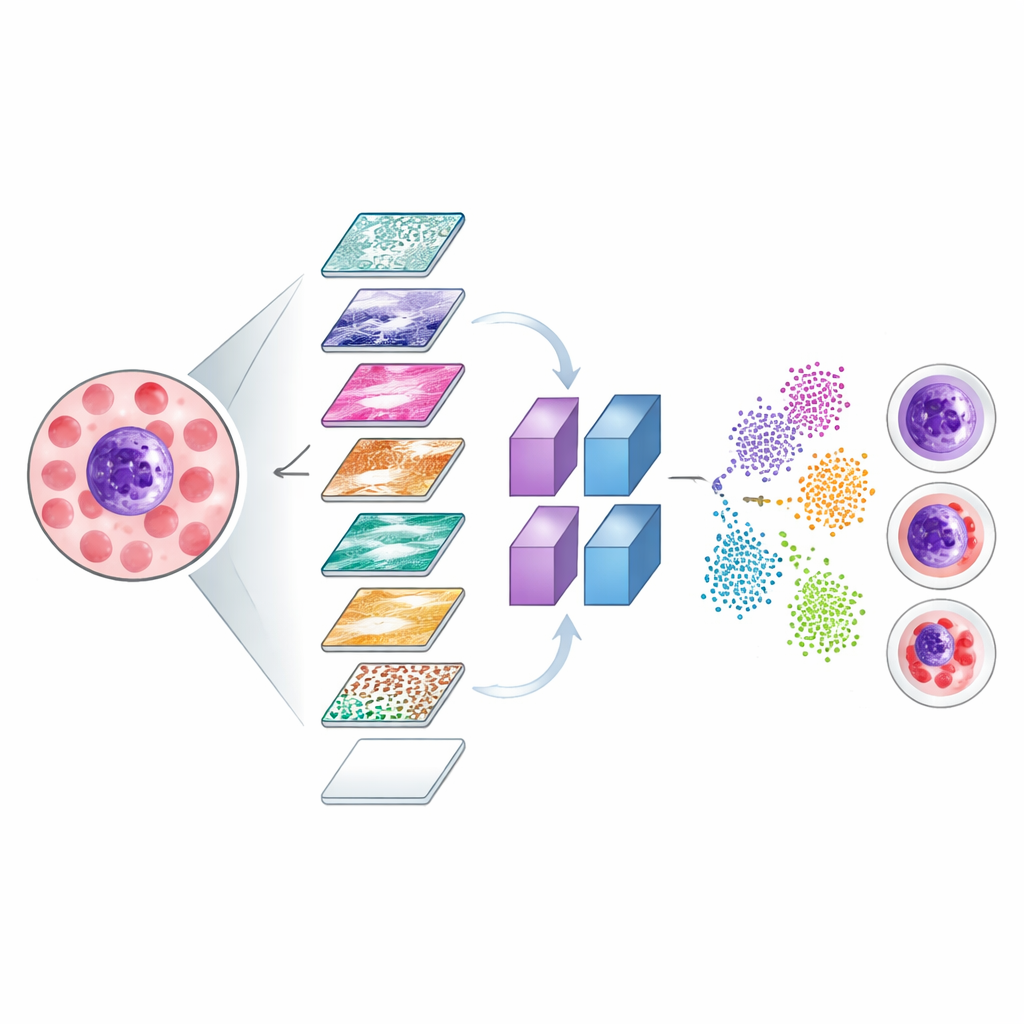
Rendere visibili decisioni invisibili
Per assicurarsi che il sistema si concentri sulle parti delle immagini con valore medico, i ricercatori hanno usato due strumenti di visualizzazione, noti come Grad-CAM e LIME. Questi metodi generano mappe di calore colorate che evidenziano quali regioni di un’immagine cellulare hanno influenzato maggiormente le decisioni del modello. Le zone luminose in queste mappe tendevano ad allinearsi con strutture cruciali come il nucleo della cellula e il citoplasma circostante, piuttosto che con lo sfondo irrilevante. Il team ha inoltre esplorato come la rete separa internamente i diversi tipi cellulari proiettando i suoi segnali interni in una mappa bidimensionale, dove le cellule correttamente classificate formano cluster chiari e i casi mal classificati possono essere esaminati per capire dove il modello incontra difficoltà.
Cosa può significare per i pazienti
In termini semplici, questo lavoro dimostra che un modello di intelligenza artificiale ben progettato e relativamente piccolo può classificare i globuli bianchi da immagini al microscopio con un’accuratezza pari o superiore a molti sistemi grandi e complessi. Poiché il modello è compatto ed efficiente, è più adatto per l’uso in laboratori più piccoli, dispositivi point-of-care o persino apparecchiature portatili, portando potenzialmente analisi del sangue di alta qualità più vicino ai pazienti. Sebbene siano necessari ulteriori test in contesti clinici reali, questo approccio indica strumenti più rapidi, accessibili e trasparenti che possono assistere i patologi nella diagnosi delle malattie e nella rilevazione precoce dei problemi.
Citazione: Karaddi, S.H., Bitra, H., Bairaboina, S.S.R. et al. White blood cell classification using custom deep neural network and visualizing features of the images using heatmaps. Sci Rep 16, 9311 (2026). https://doi.org/10.1038/s41598-026-35138-9
Parole chiave: globuli bianchi, imaging medico, apprendimento profondo, diagnostica del sangue, reti neurali