Clear Sky Science · it
Progettazione e analisi delle prestazioni di un FET nanosheet gate‑all‑around impilato verticalmente con nanocavità incorporata per applicazioni di biosensing
Sensor più piccoli per avvisi più precoci
Individuare il cancro in fase precoce dipende spesso dalla rapidità e dalla precisione con cui riusciamo a rilevare tracce minute di malattia nel sangue o in altri fluidi corporei. Questo articolo esplora un nuovo tipo di sensore elettronico ultrasmall—realizzato con la stessa tecnologia usata nei chip avanzati—capace di rilevare molecole legate al cancro con sensibilità molto superiore rispetto a molti dispositivi esistenti, consumando al contempo pochissima energia.
Trasformare un transistor in un rilevatore di cancro
Al centro dello studio c’è un transistor riprogettato, l’elemento di commutazione fondamentale nell’elettronica. Gli autori partono da un dispositivo all’avanguardia chiamato nanosheet FET, già adottato dai principali produttori per processi a 3 nm. Lo riutilizzano come biosensore ricavando piccole cavità vuote, o nanocavità, attorno al gate isolato che controlla il flusso di corrente. Quando biomolecole associate al cancro—come cellule di tumori colorettali o renali, filamenti di DNA o proteine gelatinose—si depositano in queste cavità, cambiano leggermente il modo in cui la carica elettrica si muove all’interno del dispositivo. Il transistor “percepisce” questa variazione come uno spostamento di corrente, convertendo un evento biochimico in un segnale elettrico misurabile.
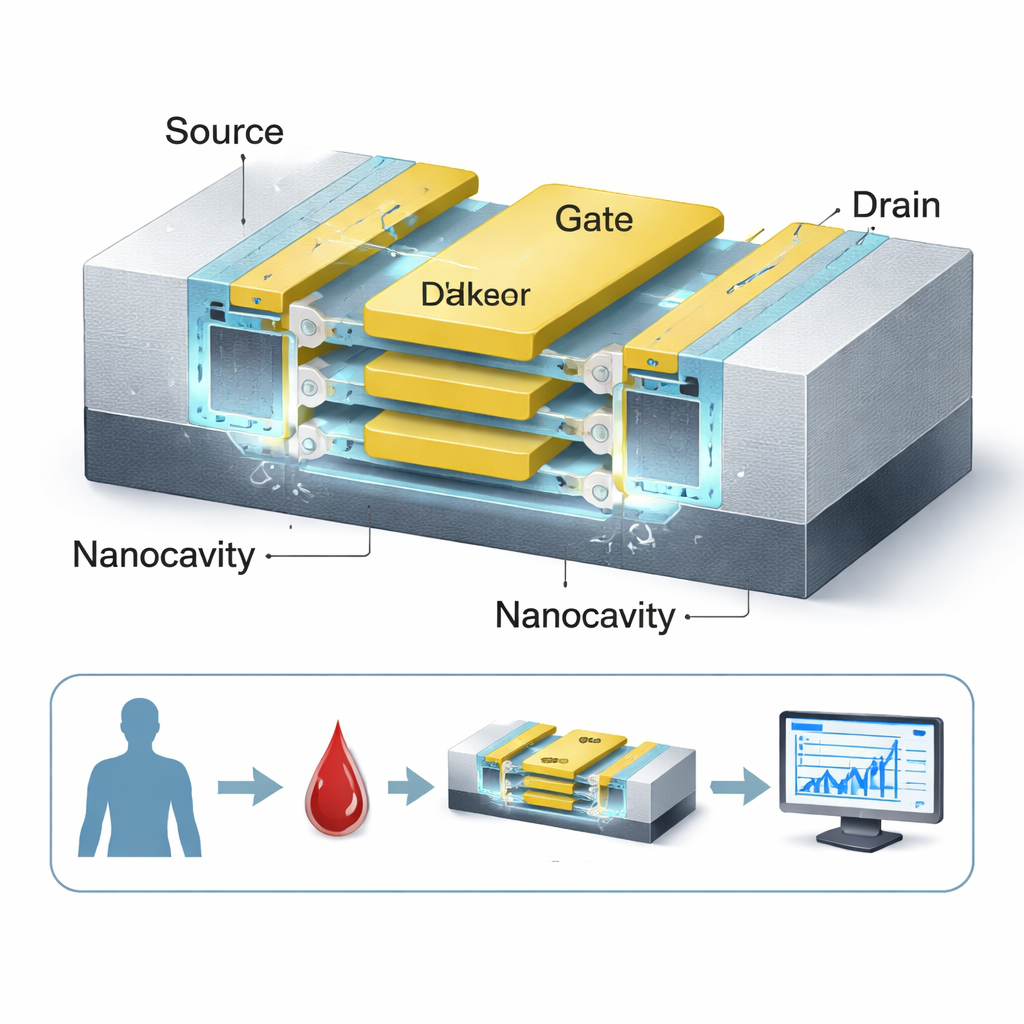
Impilare strati per segnali più intensi
Una soluzione chiave del progetto è che il canale sensibile non è un singolo filo ma tre fogli sottilissimi di silicio impilati verticalmente, tutti avvolti da un gate comune. Questa struttura gate‑all‑around conferisce al gate un controllo molto più stretto sul canale rispetto ai tradizionali transistor piatti, rendendo più netta la commutazione on/off e amplificando la variazione misurabile quando sono presenti biomolecole. Due nanocavità sono posizionate ai lati di uno strato isolante high‑k (HfO₂), massimizzando la regione in cui le molecole possono interagire con il campo elettrico. Poiché il canale è “senza drogaggio”, cioè evita elevate impurità chimiche, la risposta del sensore è più uniforme e meno vulnerabile alle variazioni di fabbricazione—un vantaggio per test medici affidabili.
Regolare nanocavità minime per una risposta massima
Usando dettagliate simulazioni al calcolatore (TCAD), i ricercatori regolano sistematicamente la geometria delle cavità: lunghezza, spessore e il grado di riempimento con molecole. Cavità più corte e sottili mettono il gate e il canale in un contatto elettrostatico più ravvicinato, aumentando la corrente di on e riducendo il cosiddetto subthreshold swing—una misura di quanto bruscamente il dispositivo si attivi. Nel loro progetto ottimale, il sensore raggiunge un bassissimo swing di circa 28 millivolt per decade, ben al di sotto del limite di 60 mV/dec dei transistor standard. Ciò significa che il dispositivo risponde in modo deciso a variazioni di tensione molto piccole, tratto cruciale per individuare concentrazioni basse di biomolecole. Mostrano inoltre che, all’aumentare della frazione di volume della cavità occupata—o quando le molecole si posizionano più vicino al punto in cui inizia la corrente—il segnale cresce, chiarendo come affollamento e posizionamento dei bersagli influenzino le prestazioni.
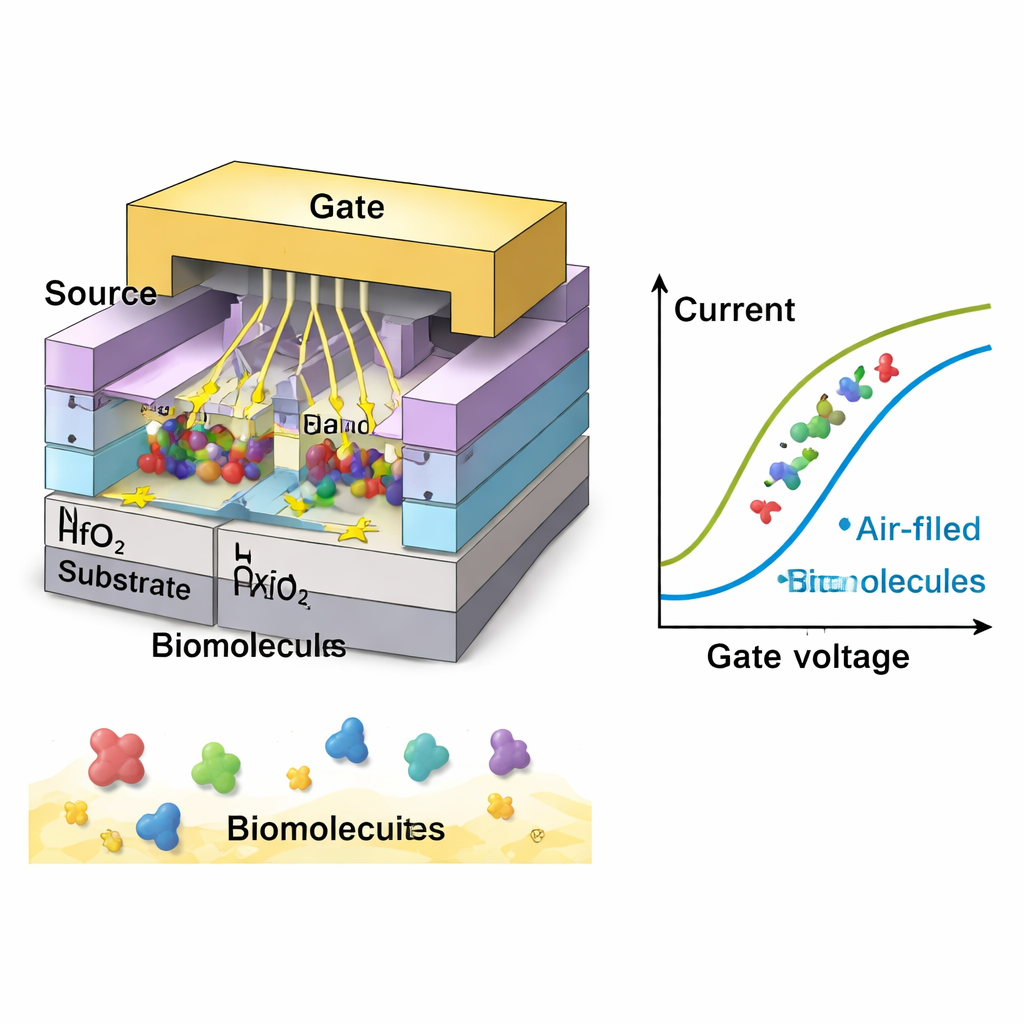
Leggere gli indizi del cancro nei segnali elettrici
Il team esplora poi come diversi tipi di biomolecole si manifesterebbero elettricamente. Specie neutre con permittività intrinseca più alta (una proprietà elettrica legata alla polarizzazione in un campo) provocano maggiori variazioni di corrente e migliore sensibilità, con la risposta più forte a valori tipici della gelatina e di alcuni tessuti biologici densi. Molecole cariche, come il DNA o certe superfici cellulari, possono amplificare ulteriormente il segnale. Nelle simulazioni, le biomolecole cariche negativamente producono lo spostamento di corrente più grande, seguite da quelle positive e infine dalle neutrali. In condizioni ottimali, il dispositivo ottiene una sensibilità di corrente oltre 3.000 volte superiore rispetto al valore di base e oltre 9.000 per cariche fortemente negative—superando diversi sensori basati su nanosheet precedenti. Il sensore mostra anche tempi di risposta rapidi, funzionamento stabile vicino alla temperatura ambiente e buona specificità, cioè la capacità di distinguere le molecole target da altre simili ma indesiderate.
Verso test pratici per il cancro a livello di chip
Per verificare la praticabilità del concetto, gli autori descrivono un flusso di fabbricazione che segue da vicino l’attuale produzione avanzata di chip, impiegando wafer silicon‑on‑insulator standard, strati noti di ossido e metallo e passaggi di incisione comuni per formare le nanocavità. Poiché la struttura rimane compatta e compatibile con i processi CMOS mainstream, potrebbe, in linea di principio, essere integrata in array densi su un singolo chip. In termini semplici, il risultato è che questo lavoro avvicina i biosensori a base di transistor a dispositivi lab‑on‑a‑chip pratici che un giorno potrebbero eseguire screening per marcatori del cancro rapidamente, con alta sensibilità e senza necessità di marcatori o chimiche complesse, utilizzando tecnologie molto simili a quelle già alla base dell’elettronica moderna.
Citazione: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Parole chiave: biosensore per il cancro, FET nanosheet, lab‑on‑a‑chip, sensore a nanocavità, rilevazione precoce