Clear Sky Science · it
La fosfatasi a doppia specificità 6 interferisce con l’attività repressiva di forkhead box O1 nei confronti di CYP4A11 che media l’accumulo di lipidi nel fegato
Perché il grasso nel fegato è importante
Un eccesso di grasso nel fegato, spesso chiamato steatosi epatica, è sempre più comune con le diete moderne ricche di zuccheri e grassi. Se molti conoscono il colesterolo o la glicemia, sono invece pochi a sapere che piccoli interruttori molecolari all’interno delle cellule epatiche decidono se il grasso venga bruciato o immagazzinato. Questo studio esamina tre di questi interruttori — proteine chiamate DUSP6, FOXO1 e CYP4A11 — e svela come la loro lotta di potere possa spingere le cellule epatiche a accumulare grasso in eccesso. Capire questo sistema di controllo nascosto potrebbe indicare nuove vie terapeutiche per la steatosi epatica e i problemi metabolici correlati.
Un controllore del traffico nascosto nelle cellule del fegato
I ricercatori si sono concentrati su una proteina chiamata DUSP6, nota soprattutto per spegnere una via di segnalazione cellulare chiamata via ERK. Studi precedenti hanno mostrato che i topi privi di DUSP6 risultavano sorprendentemente resistenti alla steatosi indotta dalla dieta e presentavano livelli più bassi di enzimi CYP4A, coinvolti nell’elaborazione dei lipidi. Qui il gruppo ha chiesto quale sia il ruolo di DUSP6 in cellule umane derivate dal fegato e come possa influenzare una versione umana di questi enzimi, CYP4A11. Hanno usato due linee cellulari tumorali epatiche standard, HepG2 e HuH‑7, come sostituti delle cellule epatiche umane e le hanno trattate con una miscela di acidi grassi (palmitico e oleico) per simulare un ambiente ricco di grassi. 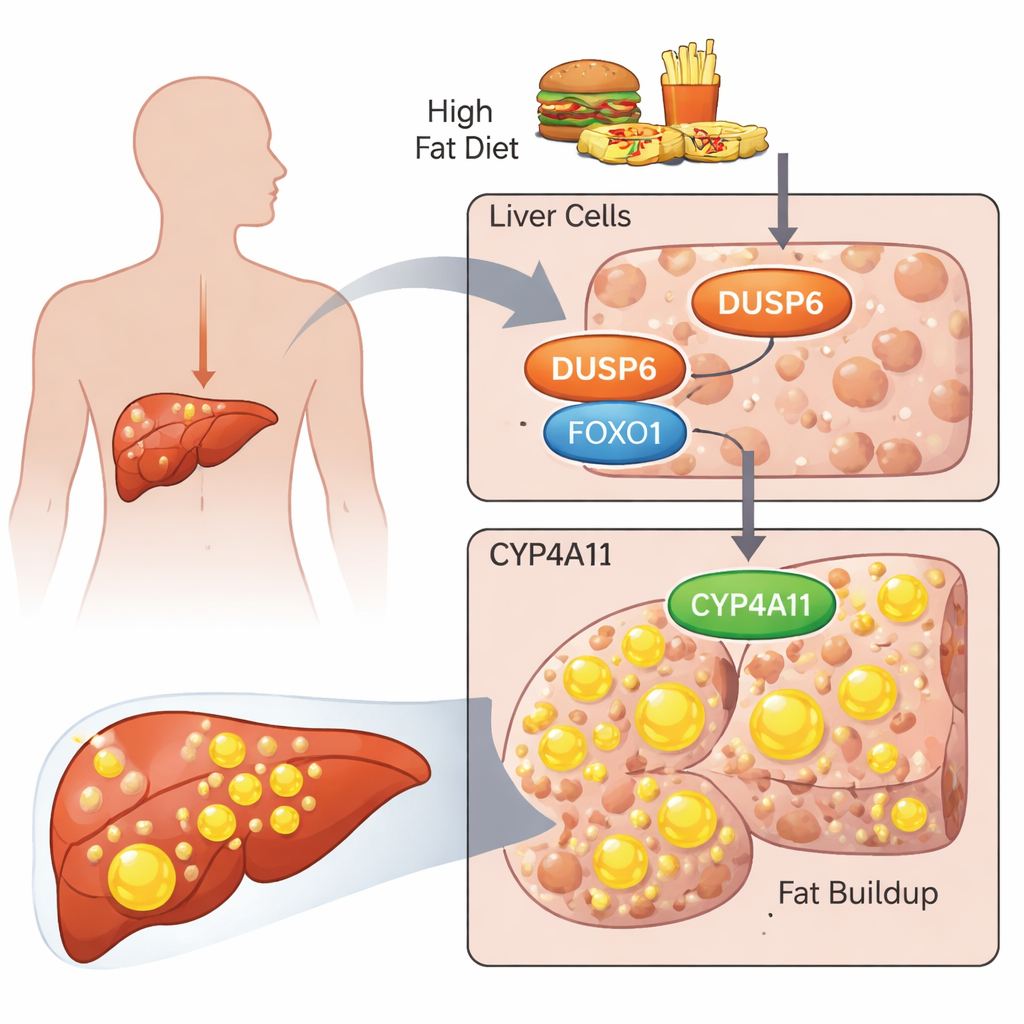
Dagli acidi grassi a una cellula piena di grasso
Quando le cellule sono state esposte a questi acidi grassi, hanno accumulato visibilmente goccioline di grasso, che gli scienziati hanno colorato e quantificato. Contemporaneamente sono aumentati i livelli di DUSP6 e CYP4A11, insieme alle forme attivate di due proteine di segnalazione principali, AKT e FOXO1. L’abbattimento di DUSP6 mediante RNA mirati ha invertito questo schema: le cellule hanno immagazzinato meno grasso, i livelli di CYP4A11 sono diminuiti, ma ERK, AKT e FOXO1 attivati sono aumentati. Bloccare solo la via ERK ha paradossalmente peggiorato l’accumulo di grasso, mentre inibire solo AKT lo ha ridotto. Quando sono state inibite insieme ERK e AKT, l’accumulo di grasso è diminuito e i livelli di CYP4A11 sono scesi. Questi esperimenti hanno collegato strettamente CYP4A11 alla quantità di grasso accumulato e suggeriscono che l’attività di AKT sia particolarmente importante nel promuovere l’immagazzinamento lipidico.
Un freno sui geni che promuovono il grasso
Un altro attore chiave, FOXO1, è un fattore di trascrizione — una proteina che può entrare nel nucleo cellulare e attivare o spegnere geni. FOXO1 è noto per agire come un freno su diversi membri della stessa famiglia enzimatica di CYP4A11. Il team ha scoperto che ridurre i livelli di FOXO1 ha portato le cellule ad accumulare più grasso e ad aumentare CYP4A11, mentre aumentare direttamente CYP4A11 ha reso le cellule ancora più grasse. Al contrario, forzare l’espressione di FOXO1 ha ridotto sia CYP4A11 sia l’accumulo di grasso. Un farmaco che blocca l’attività di CYP4A11 (HET0016) ha ridotto l’eccesso di grasso causato dalla carenza di FOXO1, sostenendo l’idea che CYP4A11 non sia mero spettatore ma fattore attivo nell’accumulo lipidico. Test chimici hanno mostrato che HET0016 abbassa i livelli di 20‑HETE, un prodotto di CYP4A11 collegato a stress ossidativo e infiammazione, collegando ulteriormente questa via al danno epatico.
Come DUSP6 disarma il freno
Per capire come FOXO1 controlli CYP4A11, gli scienziati hanno esaminato la regione di DNA davanti al gene CYP4A11 e hanno individuato sequenze dove FOXO1 può legarsi. Usando un saggio di immunoprecipitazione della cromatina, hanno dimostrato che FOXO1 — in particolare la sua forma non fosforilata — si lega direttamente al promotore di CYP4A11, coerente con un ruolo repressivo su questo gene. Esperimenti di co‑immunoprecipitazione hanno rivelato che DUSP6 interagisce fisicamente con FOXO1 ma non con la sua forma fosforilata. Studi di frazionamento e microscopia hanno mostrato che DUSP6 si trova nel citoplasma cellulare e, quando presente, mantiene più FOXO1 fuori dal nucleo. Quando DUSP6 è stato ridotto, più FOXO1 è migrato nel nucleo, dove può legare il DNA e sopprimere CYP4A11. In pratica, DUSP6 funge da ancora, sequestrando FOXO1 nel citoplasma e impedendogli di svolgere il suo ruolo di freno su CYP4A11. 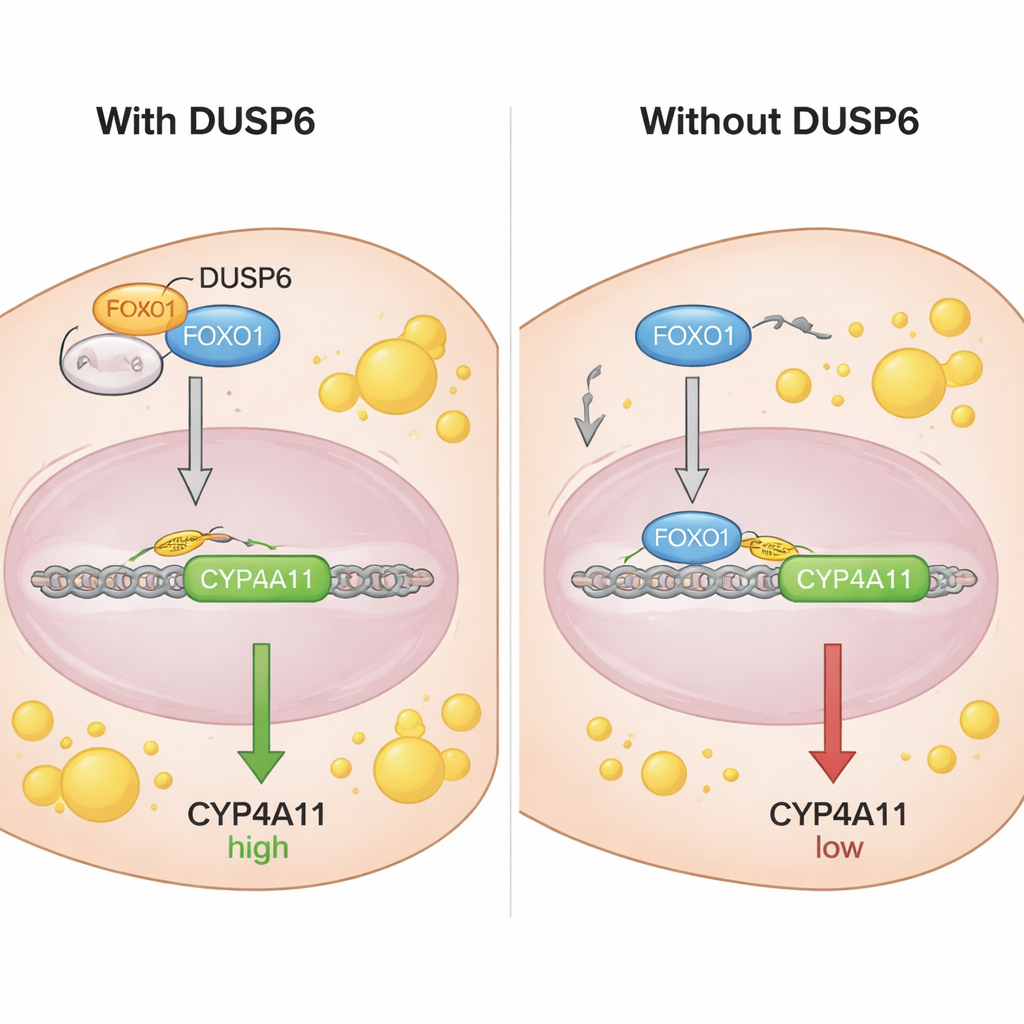
Cosa significa per la steatosi epatica e oltre
In termini semplici, questo lavoro mappa una catena di eventi all’interno delle cellule del fegato: DUSP6 trattiene FOXO1 nel citoplasma, indebolendo la capacità di FOXO1 di spegnere il gene CYP4A11. Con FOXO1 messo da parte, CYP4A11 diventa più attivo, favorendo l’immagazzinamento di grasso e la produzione di molecole come 20‑HETE che possono promuovere stress ossidativo e infiammazione. Pur essendo questi risultati ottenuti in cellule derivate dal fegato in coltura e non in tessuto epatico umano sano, evidenziano DUSP6 e CYP4A11 come potenziali nuovi bersagli terapeutici per la malattia epatica steatosica associata a disfunzione metabolica. Terapie che riducano l’attività di DUSP6 o attenuino gli effetti di CYP4A11 potrebbero, in teoria, ripristinare la funzione frenante di FOXO1 e contribuire a mantenere sotto controllo il grasso epatico.
Citazione: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Parole chiave: steatosi epatica, DUSP6, FOXO1, CYP4A11, metabolismo epatico