Clear Sky Science · it
Una rete neurale grafica informata dalla fisica per approssimare l’affinità di legame basata su docking per DYRK2 nel riposizionamento di farmaci per l’Alzheimer
Perché è importante per l’Alzheimer
La malattia di Alzheimer è in aumento nel mondo, ma la maggior parte dei farmaci attuali allevia solo i sintomi anziché bloccare la malattia. Testare nuovi medicinali in laboratorio è lento e costoso, specialmente per proteine cerebrali poco studiate che potrebbero avere un ruolo nella memoria e nella salute neuronale. Questo studio esplora una scorciatoia intelligente: usare un modello di intelligenza artificiale consapevole della fisica per prevedere quanto bene farmaci già esistenti per l’Alzheimer potrebbero legarsi a una proteina poco esplorata chiamata DYRK2, aprendo potenzialmente nuove vie per il trattamento.
Un nuovo modo di guardare ai vecchi farmaci
Invece di progettare nuovi composti da zero, i ricercatori si concentrano sul riposizionamento dei farmaci—trovare nuovi usi per medicinali già approvati e noti per essere relativamente sicuri. Esaminano quattro farmaci noti per l’Alzheimer (brexpiprazolo, donepezil, galantamina e rivastigmina) e valutano quanto strettamente ciascuno potrebbe legarsi a DYRK2, una chinasi proteica coinvolta nella crescita e nella funzione delle cellule nervose. DYRK2 è stato studiato poco nella malattia di Alzheimer, ma prove preliminari lo collegano a sinapsi, assoni e memoria, rendendolo un bersaglio interessante che potrebbe integrare le terapie attuali.
Trasformare le molecole in reti
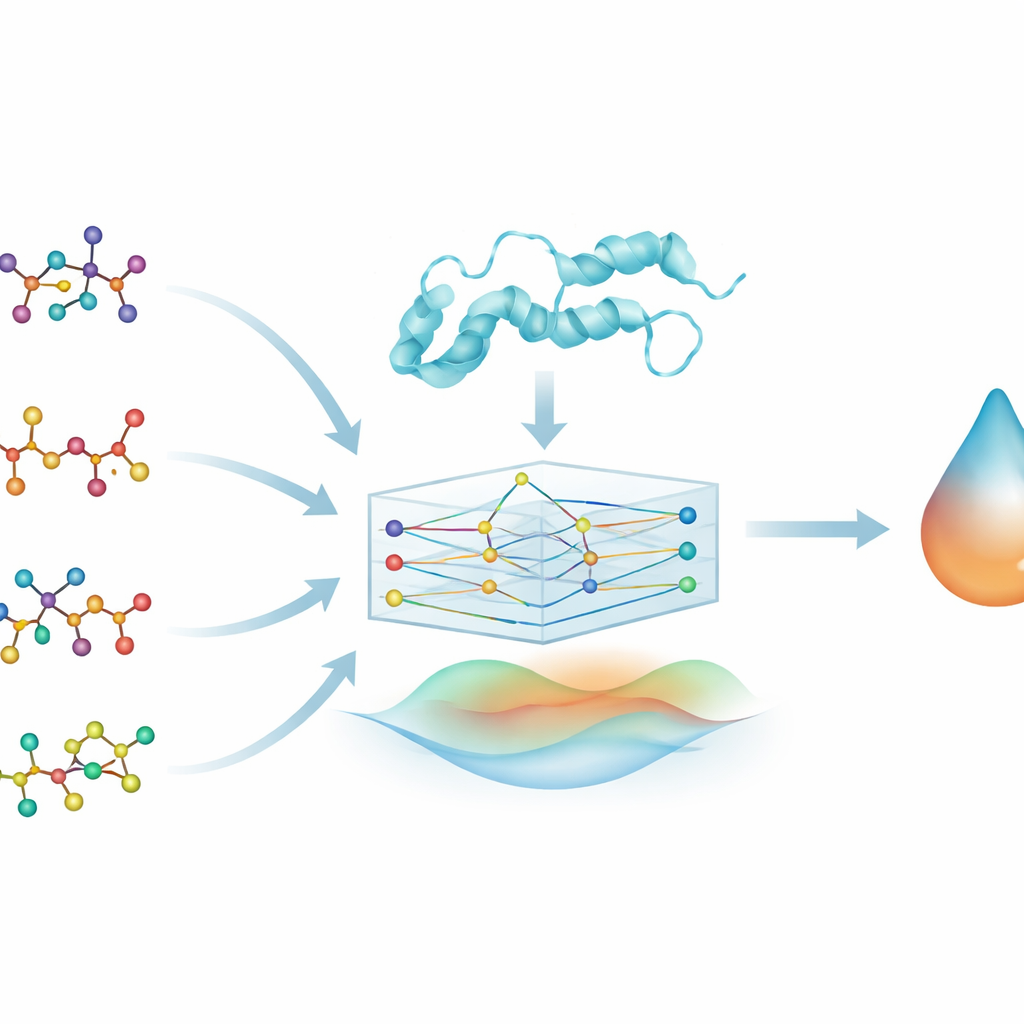
Per esplorare queste relazioni farmaco–proteina, il team trasforma ogni molecola di farmaco in un grafo: gli atomi diventano nodi e i legami chimici diventano archi che li connettono. Si procede in modo simile per la proteina DYRK2, rappresentando la sua sequenza di amminoacidi come una catena di unità connesse. Un tipo di modello di apprendimento automatico chiamato rete neurale grafica (GNN) può lavorare naturalmente con questi input a forma di grafo, passando informazioni lungo le connessioni per apprendere schemi nella forma e nella chimica. Questo permette al modello, chiamato PhysDual‑GCN, di “leggere” sia il farmaco sia DYRK2 come reti interagenti piuttosto che come semplici stringhe o liste di caratteristiche.
Fondere la fisica con l’intelligenza artificiale
La maggior parte degli strumenti di deep learning nella scoperta dei farmaci apprende solo dai dati, il che può rendere difficile interpretare il loro funzionamento interno. Qui gli autori integrano deliberatamente concetti fisici di base su come interagiscono gli atomi. Accanto alle caratteristiche grafiche apprese, PhysDual‑GCN calcola due termini energetici classici: uno che cattura l’attrazione e la repulsione elettrica tra cariche parziali e un altro che descrive le forze di van der Waals. Queste energie basate sulla fisica sono combinate con la rappresentazione interna della GNN prima che il modello produca una previsione della forza di legame. In pratica, il modello è addestrato a imitare il comportamento dei programmi di docking standard—in particolare AutoDock Vina e strumenti correlati—ma in modo più veloce, rimanendo ancorato a principi fisici noti.
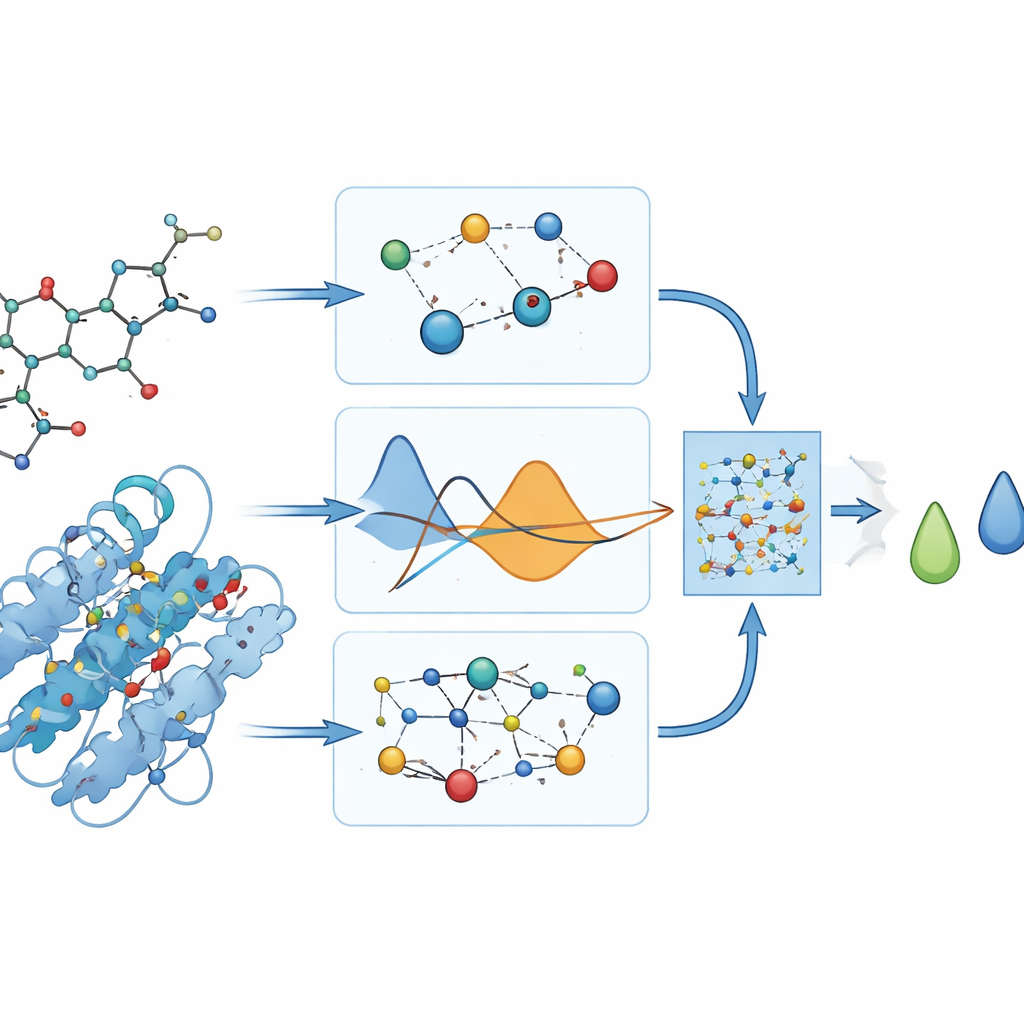
Cosa prevede effettivamente il modello
Poiché non esistono misure sperimentali su quanto fortemente questi farmaci si leghino a DYRK2, gli autori si affidano a programmi di docking per ottenere punteggi di legame “di riferimento” espressi in unità di energia. Evitano con cura di utilizzare questi punteggi nel processo di addestramento e li impiegano solo in seguito per giudicare quanto bene PhysDual‑GCN abbia appreso. Per i quattro farmaci per l’Alzheimer, il modello riproduce i valori di docking con errori medi ridotti (circa un terzo di chilocaloria per mole) e classifica correttamente i composti: donepezil e brexpiprazolo risultano i leganti più forti, mentre galantamina e rivastigmina appaiono più deboli ma comunque ragionevolmente stabili. Questi risultati mostrano che la GNN informata dalla fisica può fungere da surrogato computazionale per corse di docking più lente.
Promesse e limiti dell’approccio
Nonostante questi numeri incoraggianti, gli autori sottolineano che lo studio ha confini ben definiti. Sono stati esaminati solo quattro farmaci e tutte le valutazioni si basano su altri programmi informatici piuttosto che su esperimenti biochimici reali. La proteina DYRK2 è modellata principalmente come un grafo sequenziale unidimensionale, non come una struttura tridimensionale completa, quindi il modello non può ancora tener conto della forma dettagliata delle tasche di legame. Le energie fisiche stesse sono semplificate, usando parametri standard di campi di forza e cutoff. Di conseguenza, il lavoro va inteso come una prova di principio: dimostra che reti neurali grafiche guidate dalla fisica possono seguire da vicino i punteggi di docking classici in un contesto con pochi dati, ma non prova ancora che le previsioni corrispondano alla realtà in provetta o in clinica.
Cosa significa per la ricerca futura sull’Alzheimer
Per i non specialisti, il messaggio principale è che algoritmi intelligenti e consapevoli della fisica possono aiutare gli scienziati a esplorare nuovi bersagli per l’Alzheimer come DYRK2 molto più rapidamente rispetto ai metodi tradizionali da soli. Evidenziando donepezil e brexpiprazolo come potenziali leganti di DYRK2 e offrendo un modo trasparente per approssimare i risultati del docking, PhysDual‑GCN fornisce un punto di partenza per studi di laboratorio più approfonditi. Con librerie di farmaci più ampie, informazioni proteiche 3D più ricche e validazione sperimentale, questo tipo di modello potrebbe diventare uno strumento pratico per lo screening di farmaci candidati e per guidare gli sforzi di riposizionamento volti a rallentare o modificare il corso della malattia di Alzheimer.
Citazione: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
Parole chiave: malattia di Alzheimer, riposizionamento di farmaci, reti neurali grafiche, legame proteina–ligando, chinasi DYRK2