Clear Sky Science · it
Struttura cristallina della cistatina B di Echinococcus multilocularis rivela una caratteristica nuova nelle stefine classiche
Perché l’arma segreta di un parassita epatico conta
L’echinococcosi alveolare è un nome difficile per un’infezione da piccolo verme a nastro che si comporta molto come un tumore a crescita lenta nel fegato. Spesso è letale; i farmaci attuali funzionano poco e possono avere effetti collaterali seri. Questo studio esamina una specifica molecola prodotta dal parassita, una proteina chiamata EmCystatin-B, per capire come potrebbe aiutare il verme a eludere le nostre difese—e come un giorno potrebbe diventare un bersaglio per nuovi trattamenti.
Un pericoloso verme che cresce come un tumore
La malattia è causata dallo stadio larvale del verme a nastro Echinococcus multilocularis. Le persone si infettano ingerendo accidentalmente uova del parassita, per esempio con cibi o acqua contaminati. Una volta nell’organismo, le larve si insediano principalmente nel fegato e crescono come molte piccole tasche piene di liquido che infiltrano i tessuti circostanti, si estendono a organi vicini come la milza e talvolta raggiungono sedi distanti come polmoni o cervello. In assenza di un trattamento efficace, più di 9 pazienti su 10 muoiono entro 10–15 anni. L’intervento chirurgico combinato con terapie antiparassitarie a lungo termine è attualmente la migliore opzione, ma la diagnosi precoce è difficile e i farmaci non garantiscono la guarigione. Perciò è cruciale capire come il parassita interagisce con il corpo umano a livello molecolare.
Una proteina parassitaria che disarma enzimi taglienti
Molti animali, compresi gli esseri umani, producono una famiglia di proteine chiamate cistatine che funzionano come blocchi di sicurezza su potenti enzimi digestivi noti come proteasi a cisteina. Questi enzimi possono degradare altre proteine e sono importanti per processi come la rimozione di parti cellulari vecchie e l’attivazione delle risposte immunitarie. I parassiti hanno imparato a produrre proprie proteine simili alle cistatine per interferire con gli enzimi e il sistema immunitario dell’ospite. In questo lavoro i ricercatori hanno identificato una proteina simile alla cistatina di E. multilocularis e l’hanno chiamata EmCystatin-B. Hanno riscontrato che il gene di EmCystatin-B è molto più attivo nelle teste larvali mature del parassita (protoscolex) rispetto al tessuto cistico circostante, e che la proteina è presente nel citoplasma e nel nucleo delle cellule del parassita, in particolare nelle cellule germinative “simili a staminali” in divisione. Test di laboratorio hanno mostrato che EmCystatin-B può bloccare fortemente l’attività della cathepsina B umana, una proteasi a cisteina importante nell’immunità e nel rimodellamento tissutale.
Una forma familiare con una sorpresa inattesa
Per vedere esattamente come è costruita EmCystatin-B, il team ha cristallizzato la proteina purificata e ha usato la cristallografia a raggi X per risolverne la struttura tridimensionale a risoluzione quasi atomica. Come altri membri della famiglia delle cistatine, ogni unità di EmCystatin-B ha una forma caratteristica: un segmento elicoidale centrale sostenuto da diversi filamenti piatti a nastro, formando una cuneo che normalmente si incastra nel sito attivo di una proteasi. In base alla sequenza e all’assenza di un evidente peptide segnale per la secrezione, EmCystatin-B appartiene al sottogruppo delle “stefine”, che sono solitamente proteine piccole, intracellulari e prive di legami disolfuro stabilizzanti. Sorprendentemente, la struttura ha rivelato che sebbene ogni unità di EmCystatin-B presenti il ripiegamento previsto, il modo in cui queste unità si associano tra loro è insolito e specifico della specie rispetto alla controparte umana, la cistatina B.
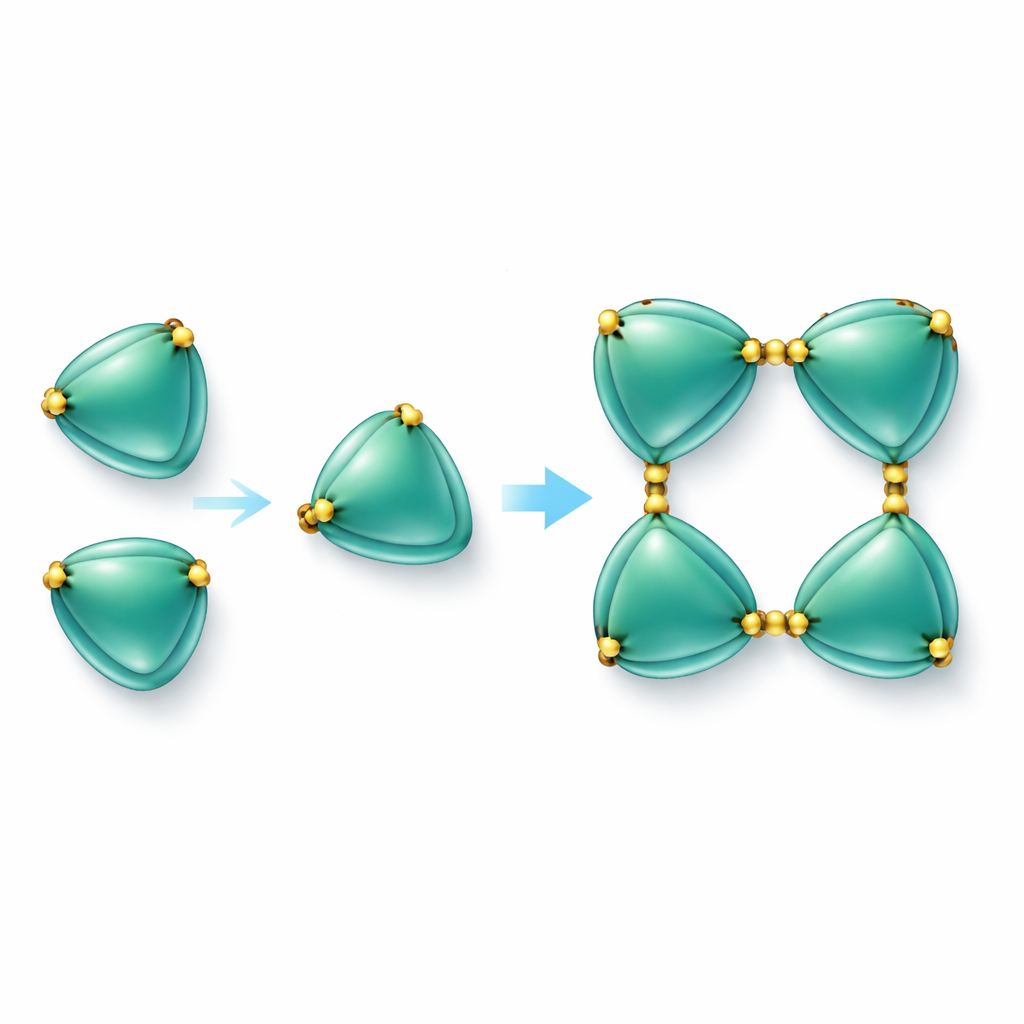
Costruire catene proteiche con legami di zolfo
La scoperta più evidente è che le molecole di EmCystatin-B non stazionano semplicemente come unità singole. Possono invece unirsi in modo progressivo per formare dimeri (coppie) e poi tetrameri (gruppi di quattro). Due meccanismi diversi favoriscono la formazione dei dimeri iniziali. In uno, una parte di una molecola si sposta e completa la struttura del vicino, un fenomeno noto come domain swapping. Nell’altro, coppie di molecole sono legate tra loro da ponti disolfuro—forti legami chimici tra aminoacidi contenenti zolfo (cisteine). In EmCystatin-B, la cisteina in posizione 4 di una molecola si lega alla cisteina in posizione 76 di una molecola partner. Quattro di questi legami incrociati stabilizzano poi il tetramero. L’uso di molteplici ponti disolfuro intermolecolari è del tutto nuovo per le stefine classiche, che tipicamente ne sono prive. Quando i ricercatori hanno sostituito queste cisteine chiave con un altro aminoacido, la proteina non è più riuscita ad assemblarsi efficacemente in complessi di ordine superiore e la sua capacità di inibire la cathepsina B è diminuita drasticamente.
Cosa significa per la lotta all’infezione
Per chi non è specialista, il messaggio è che il parassita ha evoluto una versione appositamente “rimarchiata” di una famiglia proteica comune, usando rivetti chimici aggiuntivi per bloccare più unità inibitorie insieme. Questa forma oligomerica sembra importante per spegnere un enzima dell’ospite che altrimenti contribuirebbe a controllare l’infezione. Svelando l’architettura precisa di EmCystatin-B e i suoi unici assemblaggi legati da disolfuro, lo studio amplia la nostra comprensione di come le proteine cistatine possano essere modulate tra le specie. A lungo termine, queste intuizioni potrebbero guidare la progettazione di farmaci che o bloccano l’effetto protettivo di EmCystatin-B sul parassita o ne imitano le proprietà immunoregolatorie per trattare malattie infiammatorie.
Citazione: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Parole chiave: echinococcosi alveolare, Echinococcus multilocularis, cistatina B, struttura proteica, modulazione immunitaria